应用无创呼吸支持治疗新生儿呼吸窘迫综合 征(neonatal respiratory distress sydrome,NRDS)一 直是新生儿领域临床研究的重点。《NRDS 的管理 -欧洲共识指南 2010 版》[1] 推荐“气管插管 - 表面 活性物质 - 拔管无创通气”(Intubate-SurfactantExtubate,INSURE)治疗,提倡对于病情稳定的早 产 NRDS 患儿,在气管插管给予肺表面活性物质 (pulmonary surfactant,PS)后应尽快(或早期) 拔出气管插管,改为无创的通气方式,如经鼻 间 歇 正 压 通 气(nasal intermittent positive pressure ventilation,NIPPV)和经鼻持续气道正压通气(nasal continuous positive airway pressure,NCPAP)。目前, 国内多选用 NCPAP 作为 NRDS 的初始呼吸支持模 式[2],对有自主呼吸的 NRDS 患儿,NCPAP 可在 整个呼吸周期提供持续的气道正压,减少呼吸做 功,避免肺泡塌陷。然而,在早产儿中枢性呼吸 衰竭、频繁呼吸暂停、呼吸动作微弱等通气不足 情况下,NCPAP 就不足以支持患儿的呼吸功能。 NIPPV 的无创呼吸支持模式,不管患儿有无自主 呼吸,呼吸机均按预置的压力、频率等呼吸参数 进行辅助通气,其在 NCPAP 的基础上增加了设置 频率的间歇吸气相正压,可提高平均气道压力, 增加潮气量和每分通气量,支持肺泡扩张,增加 气体交换,较 NCPAP 具有更强的呼吸支持作用[3], 已在国外新生儿重症监护病房得到高度重视并逐 渐推广,用于 NRDS 呼吸支持治疗的初始模式[4]。 但目前国内对 NIPPV 的研究较少,本研究于 2011 年 1 月至 2013 年 6 月,采用随机对照研究的方法, 比较 NIPPV 或 NCPAP 在初始治疗早产儿 NRDS 中 的临床有效性及安全性,探索合适的转换 NIPPV 呼吸支持时机和参数的初始设置。临床取得了较 好疗效,现报告如下。 1 资料与方法 1.1 研究对象
入选标准:(1)胎龄≥30 周而≤34 周, 适于胎龄儿;(2)由本院产科出生,生后 30 min 内转入新生儿重症监护病房;(3)满足 NRDS 诊 断标准[5],排除出生后需要立即应用气管插管行 机械通气治疗的情况;(4)除外气胸、复杂性先 天性心脏病、其它先天畸形等所致的呼吸衰竭; (5)除外重度窒息,严重宫内感染、出血性疾 病或出血倾向、严重贫血及循环衰竭;(6)排 除住院未满 72 h 者。共 100 例新生儿,随机分为 NIPPV 组 50 例和 NCPAP 组 50 例。本研究获得医 院伦理委员会的批准及家属知情同意。 1.2 无创呼吸支持方法 由新生儿科医师参与所有小于 34 周早产儿 的出生初始复苏。不论生后何时,一旦出现呼吸 急促、三凹征、呻吟、需氧(FiO2>0.21)等有可 能是 NRDS 的症状,即开始使用 NIPPV 或 NCPAP 呼吸支持,选择合适的鼻塞及妥善的固定,给予 必要的安抚、镇静,正确的体位,保持呼吸道通 畅等以保持有效正压。在初始无创通气的 30 min 内,根据新生儿的呼吸状态调整呼吸机参数,使 其短时间内符合新生儿的呼吸生理状态。并行动 脉血气分析,申请胸部 X 线,尽早明确诊断是否 为 NRDS;两组患儿于无创通气下,至少 CPAP 为 6 cm H2O 时,若持续 FiO2>40%,或 FiO2有逐渐增 加趋势,或有 NRDS 进展的其它证据,均于明确 诊断为 NRDS 后,尽早行气管插管,气管内给予 首剂足量 PS(猪肺磷脂混悬液 200 mg/kg);对拔 除气管插管的早产儿,使用至少 6 cm H2O 的呼气 末压(positive end-expiratory pressure,PEEP);密 切监测各项生命体征指标及血液动力学改变,若 出现呼吸困难加重或生命体征不稳定等,如重症 呼吸性酸中毒 [PaCO2>65 mm Hg,FiO2>0.6]、严重 或频繁呼吸暂停、消化道出血、新生儿肺出血、 休克、心跳呼吸骤停等,及时予气管插管机械通气, 必要时给予第 2 剂、第 3 剂 PS(100 mg/kg)。 1.3 无创呼吸支持设备及参数设置
NIPPV 组采用双鼻塞密闭环路方式,使用 Drager Babylog 8000(德国)呼吸机,吸气峰压 (peak inspiratory pressure,PIP)15~25 cm H2 O, PEEP 5~10 cm H2O,FiO2根据维持经皮氧饱和度 在 85%~93% 调节,范围为 0.21~0.60,呼吸频率 (RR)一般在20~60 min,吸气时间(Ti)0.30~0.45 s。 当参数降至 RR ≤ 20 次 /min,平均气道压(MAP) ≤ 8 cm H2O,FiO2 ≤ 0.3 时可转成 CPAP 并渐次 至撤机。NCPAP 组同样采用双鼻塞方式,使用 Drager Babylog 8000(德国)CPAP 模式,压力为 5~10 cm H2O。 当 参 数 降 至 CPAP ≤ 4 cm H2O, FiO2=0.21 时可撤机。 1.4 PS 给予方法
2 组患儿均经家属同意后应用猪肺磷脂混悬液 (固尔苏,意大利凯西制药公司)200 mg/kg,治 疗后呼吸机辅助通气 1 h,生命体征稳定的早产儿 拔管,NIPPV 组继续予 NIPPV 模式,而 NCPAP 组 继续予 NCPAP 模式。 1.5 观察指标
患儿一般情况(胎龄、出生体重、给予 初始呼吸支持日龄、性别、Apgar评分、首 剂PS 使用时间);动脉血气分析,氧合指数 (OI)=MAP×FiO2×100/PaO2(mm Hg);需再次 气管插管行机械通气率、再次使用 PS 率、有创辅 助呼吸支持时间、FiO2>0.21 时间;呼吸暂停、呼 吸机相关肺炎、肺气漏和腹胀发生率。 1.6 统计学分析
以 SPSS 13.0 软件对数据进行统计学处理,计 量资料以均数 ± 标准差(x±s)表示,组间比较 采用t检验;计数资料以率(%)表示,组间比较 采用X2检验。P<0.05 为差异有统计学意义。 2 结果 2.1 两组临床资料的比较
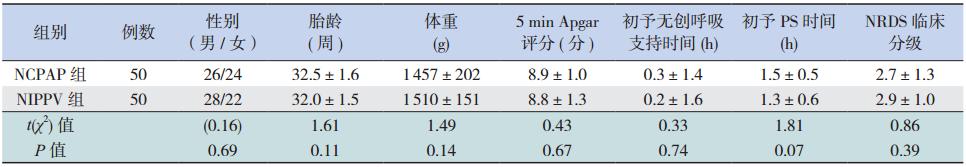
NIPPV 组和 NCPAP 组患儿在胎龄、出生体重、 性别、5 min Apgar 评分、初始给予无创呼吸支持 时间、第一剂 PS 给予时间及 NRDS 的临床分级等 一般临床资料间的比较,差异均无统计学意义(均 P>0.05)。见表 1。
| 表1 12 两组患儿临床资料比较 (例,x±s) |
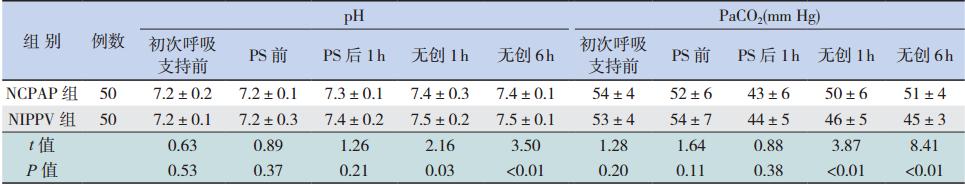
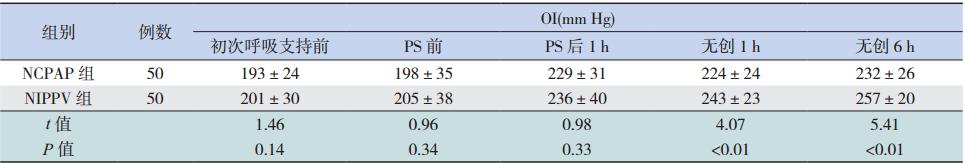
初予呼吸支持前、PS 治疗前(气管插管前) 与 PS 治疗后 1 h(呼吸机通气 1 h 拔管时)两组 患儿的 pH、PaCO2、OI 差异无统计学意义(均 P>0.05);但改为不同无创通气模式后,NIPPV 组 PaCO2较 NCPAP 组下降,OI 和 pH 值较 NCPAP 组 升高(均P<0.05),提示 NIPPV 组在减轻 CO2潴留、 改善氧合时优于 NCPAP 组。见表 2。
| 表 2 两组治疗前后动脉血气及 OI 的比较 (x±s) |
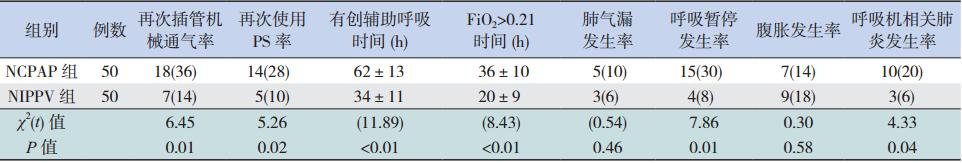
NCPAP 组再次插管机械通气率、再次使用 PS 率、有创辅助呼吸时间和 FiO2>0.21 时间均明显 高于 NIPPV 组(均P<0.05);NIPPV 可明显减少 呼吸暂停发生次数及呼吸机相关肺炎的发生(均 P<0.05);肺气漏和腹胀发生率在两组间差异无统 计学意义(均P>0.05)。见表 3。
| 表 3 两组临床各指标比较 [ 例(%)或x±s] |
NRDS 是早产儿常见的呼吸急症,起病急,进 展快,病情危重。良好的呼吸管理是 NRDS 治疗 成功的关键,也是决定早产儿近远期预后的重要 因素。对于早产儿,一旦怀疑为 NRDS,应早期给 予呼吸支持,应用无创呼吸支持治疗 NRDS 一直 是新生儿领域临床研究的重点,早期给予适当的 无创呼吸支持不仅可缩短用氧时间还可减少机械 通气的可能性[6]。NCPAP 因可以提供整个呼吸周 期持续的气道正压,降低呼吸做功,避免肺泡塌陷, 是目前国内应用较多的主要无创辅助通气模式。 但是,对于一些自主呼吸浅弱、频繁呼吸暂停的 NRDS 患儿,NCPAP 就不足以提供必需的呼吸支持。 而 NIPPV 不论患儿有无自主呼吸,均可按照预设 的呼吸参数提供一定频率、压力的辅助通气,在 NCPAP 基础上增加了设置频率的间歇吸气相正压, 可提高平均气道压,改善氧合,具有更强的呼吸 支持作用。 已在国外新生儿重症监护病房应用并 逐渐推广,除用于NRDS 呼吸支持的初始模式之外, 还被用于 NRDS 治疗拔管和撤离呼吸机的过程, 治疗呼吸暂停等[7]。
本研究应用前瞻性随机对照研究的方法, 比较 NIPPV 与 NCPAP 在初始治疗 NRDS 中的疗 效。结果显示:NIPPV 初始治疗 NRDS 的成功率 显著高于 NCPAP,能显著提高 INSURE 治疗拔管 后的成功率,减少 NRDS 患儿机械通气的比例, 减少有创呼吸支持时间,减少需氧时间,并可减 少早产儿呼吸暂停次数。分析原因:(1)NIPPV 降低 CO2潴留、改善氧合、减少需氧时间的作用 较 NCPAP 强。给予 PS 拔管后 1 h 及 6 h,NIPPV 组的 PaCO2下降,OI 及 pH 值增高均优于 NCPAP 组,这与 NIPPV 可提供设置频率的吸气相峰压, 提供高于 NCPAP 的 MAP 支持,从而减少患儿的 呼吸做功,减少呼吸肌的疲劳,降低 PS 和能量的 消耗相关;(2)NIPPV 组需要再次气管插管进行 机械通气的比例为 14%,明显低于 NCPAP 组的 36%,与 Sai 等 [8] 在 28~34 周 早 产 儿 NRDS 的 最 新临床观察:NIPPV 组及 NCPAP 组再次气管插管 行机械通气的比例分别为 13.5%、35.9% 一致。而 且,即使那些需要气管插管机械通气的 NIPPV 组 患儿,其有创机械通气时间也可以缩短,本研究 显示 NIPPV 组及 NCPAP 组有创通气时间均值分 别为 34 h、62 h,这与 NIPPV 可提供更强的呼吸 支持作用,NRDS 进展的患儿可耐受较晚再次插 管及较快再次脱离有创通气相关。然而,目前尚 无判断 NIPPV 与有创呼吸支持之间相互转换最佳 时机的临床指南。本课题组的经验是,当患儿有 创通气的参数降至 MAP ≤ 10 cm H2O,FiO2≤ 0.4 时可转成NIPPV;而NIPPV的参数降至RR ≤ 20 次 /min,MAP ≤ 8 cm H2O,FiO2≤ 0.3 时可 转成 NCPAP 并渐次至撤机。而且在初始无创呼吸 支持时,不管是在 NCPAP 组还是在 NIPPV 组,临 床倾向初始给予较高的 PEEP 支持,PEEP 可常规 设置于 5~10 cm H2O [9]。
多数研究显示 NIPPV 具有显著疗效而无严重 并发症[10, 11]。本研究亦显示使用 NIPPV 并未增加 肺气漏、腹胀等的发生率,可能与选择合适鼻塞 及妥善的固定、给予必要的安抚、镇静,保持正 确的体位,保持呼吸道通畅,并给予呼吸支持患儿常规留置胃管,必要时持续或间断减压等相关。 目前,NIPPV 的临床使用中尚有以下问题需要注 意:(1)由于 NIPPV 并不形成一个完全封闭的通 气系统,所提供的 PIP 与预设的 PIP 数值不能保持 完全一致,在治疗过程中平均气道压力往往存在 变化,从而可能由于跨肺压力增加而导致肺过度 扩张[12];(2)目前大部分国内国外 NICU 临床使 用的 NIPPV 装置不含流量监测探头,并不能提供 设置触发和实时监测肺功能[13];(3)任何一种无 创辅助通气都不可能完全取代有创呼吸支持,当 NRDS 患儿明显呼吸衰竭,需要进行气管插管时应 当机立断,毫不犹豫,及时转为“有创”通气, 以免延误治疗,影响近远期预后。
总之,NIPPV作为新的无创呼吸支持技 术,在 NRDS 的治疗中显示了广阔的前景。但是 NIPPV 在早产儿和足月儿、早产儿不同胎龄和体 重、不同基础疾病的临床治疗作用、临床如何保 持及监测气道有效正压以及临床治疗的远期疗效 方面等,均尚需大规模的临床多中心进一步的研 究。
| [1] | 孙秀静, 王丹华. 新生儿呼吸窘迫综合症的管理—欧洲共识指南2010版[J].中国新生儿杂志, 2010, 25(6): 378-380. |
| [2] | Bancalari E, Claure N. Non-invasive ventilation of the preterm infant [J]. Early Hum Dev, 2008, 84(12): 815-819. |
| [3] | Lampland AL, Meyers PA, Worwa CT, et al. Gas exchange and lung inflammation using nasal intermittent positive-pressure ventilation versus synchronized intermittent mandatory ventilation in piglets with saline lavage-induced lung injury: an observational study[J]. Crit Care Med, 2008, 36(1): 183-187. |
| [4] | Davis PG, Morley CJ, Owen LS. Noninvasive respiratory support of preterm neonates with respiratory distress:continuous positive airway pressure and nasal intermittent positive pressure ventilation[J]. Semin Fetal Neonatal Med, 2009, 14(1): 14-20. |
| [5] | 金汉珍,黄德珉,官希吉.实用新生儿学[M].第3版.北京:人民卫生出版社, 2003: 421-427. |
| [6] | Sandri F, Ancora G, LanzoniA, et al. Prophylactic nasal continuous positive airways pressure in newborns of 28-31 weeks gestation: multicentre randomised controlled clinical trial[J]. Arch Dis Child Fetal Neonatal Ed, 2004, 89(5): F394-F398. |
| [7] | Ramanathan R. Nasal respiratory support through the nares: its time has come[J]. Perinatol, 2010, 30 Suppl: S67-S72. |
| [8] | Sai Sunil Kishore M, Dutta S, Kumar P. Early nasal intermittent positive pressure ventilation versus continuous positive airway pressure for respiratory distress syndrome[J]. Acta Paediatr, 2009, 98(9): 1412-1415. |
| [9] | Sankaran K, Adegbite M. Noninvasive respiratory support in neonates: a brief review[J].中国当代儿科杂志, 2012, 14(9): 644-652. |
| [10] | 高薇薇, 谭三智, 陈运彬, 等. 鼻塞式同步间歇指令通气和持续气道正压通气在早产儿呼吸窘迫综合征中的应用比较[J].中国当代儿科杂志, 2010, 12(7): 524-526. |
| [11] | 唐仕芳, 赵锦宁, 沈洁, 等. 经鼻间歇和持续气道正压通气治疗新生儿呼吸窘迫综合征的Meta分析[J].中国循证儿科杂志, 2011, 6(4): 255-263. |
| [12] | Owen LS, Morley CJ, Davis PG. Neonatal nasal intermittent positive pressure ventilation:what do we know in 2007?[J]. Arch Dis Child Fetal Neonatal Ed, 2007, 92(5): 414-418. |
| [13] | Owen LS, Morley CJ, Davis PG. Pressure variation during ventilator generated nasal intermittent positive pressure ventilation in preterm infants[J]. Arch Dis Child Fetal. Neonatal.Ed, 2010, 95(5): F359-F364. |
 2014, Vol. 16
2014, Vol. 16