呼吸暂停是早产儿的常见并发症之一。胎龄越小、出生体重越轻,发生率越高。研究报道,胎龄小于34 周的早产儿中呼吸暂停发生率约为85%[1, 2]。反复发生的呼吸暂停可引起神经系统预后不良,若未能及时发现及处理,还可能导致患儿猝死[1, 3, 4, 5]。因此,呼吸暂停的控制是早产儿呼吸管理的重要内容之一。现有对呼吸暂停的处理手段主要为触觉刺激、药物干预及辅助通气;而临床最常用的药物为甲基黄嘌呤类药物,包括氨茶碱及枸橼酸咖啡因[3, 6, 7]。目前我国仍主要采用氨茶碱防治早产儿呼吸暂停。氨茶碱的治疗剂量与中毒剂量较为接近,现行推荐的维持治疗剂量范围较广,为1~2 mg/kg[6, 7]。国外研究显示,氨茶碱在早产儿体内的代谢过程具有较大差异[8]。故临床治疗时需进行治疗药物监测(therapeutic drugmonitoring,TDM),实施个体化给药,以保证患儿用药安全。本研究采用氨茶碱常规TDM 数据,探索不同维持剂量氨茶碱在不同胎龄、不同体重及不同日龄极低出生体重儿中药代动力学和药效学特点,为临床用药提供参考。
1 资料与方法 1.1 研究对象选取2011~2012 年我院新生儿科中有呼吸暂停症状,需使用氨茶碱治疗的极低出生体重儿40 例为研究对象。
根据《实用新生儿学( 第4 版)》[6],呼吸暂停定义为呼吸停止>20 s,并伴有心率减慢(<100 次/min)或出现青紫、血氧饱和度降低和肌张力低下。
排除标准:严重肝肾功能损害者;既往接受氨茶碱治疗或治疗过程中需调整剂量者;合并使用其他可能影响氨茶碱药物浓度如苯巴比妥、乳糖酸红霉素及西咪替丁者。
本研究获得我院伦理委员会批准及监护人的知情同意。
1.2 氨茶碱治疗方法选用氨茶碱注射液(0.25 g/10 mL,天津金耀氨基酸公司)。患儿在接受负荷剂量(5 mg/kg)静脉注射后,随机分为2 个不同维持剂量组,一组患儿维持剂量为1 mg/kg,每8 h 给药一次(1 mg/kg 组,n=20),另一组患儿的维持治疗剂量为2 mg/kg,每8 h 给药一次(2 mg/kg 组,n=20)。氨茶碱的输注时间均为20 min。所有患儿在接受氨茶碱治疗后8 h、3 d、7 d 采集外周静脉血1 mL 监测血药浓度及肝肾功能,开始用药7 d 内记录呼吸暂停发作情况、血糖、心率及腹胀情况。在维持治疗后连续5 d 未观察到呼吸暂停者可停止用药。
1.3 氨茶碱血药浓度测定将血样以1 000×g 离心10 min,采用ADVIACentaur CP 茶碱2 直接化学发光法检测氨茶碱血药浓度。茶碱测定试剂盒购自Siemens HealthcareDiagnosis Inc.。该测定法的最低检测浓度为0.5 μg/mL,检测范围上限为40 μg/mL。日间及日内氨茶碱检验变异系数 <5%。
1.4 药代动力学分析根据本课题组前期建立的氨茶碱药代动力学分析过程,运用一室模型,采用药代动力学软件MW/Pharm3.6(Mediware,Groningen,TheNetherlands)进行分析,分别将体重、校正胎龄及生后日龄与血药浓度行拟合曲线制定药代动力学方程[9]。所用的药代动力学参数包括:血浆清除率(CL)、表观分布容积(Vd)及半衰期(t1/2)。
1.5 统计学分析采用SPSS 19.0 软件进行统计学分析,计量资料以均数± 标准差(x±s)或中位数(四分位数)[M(P25,P75)] 表示,组间比较采用t 检验或秩和检验;计数资料以率(%)表示,组间比较采用卡方检验;相关性分析采用直线相关分析。P<0.05为差异有统计学意义。
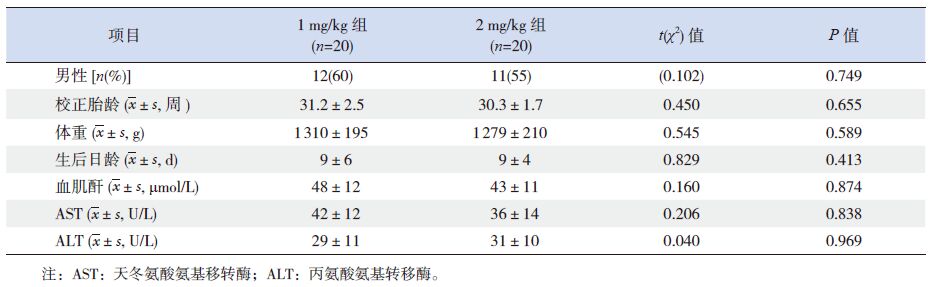
2 结果 2.1 临床特征40名患儿中,两组性别构成比、用药时的校正胎龄、体重及生后日龄等的差异无统计学意义;同时两组患儿的血肌酐、转氨酶水平的差异亦无统计学意义(表 1)。
|
|
表 1 两组患儿的临床特征 |
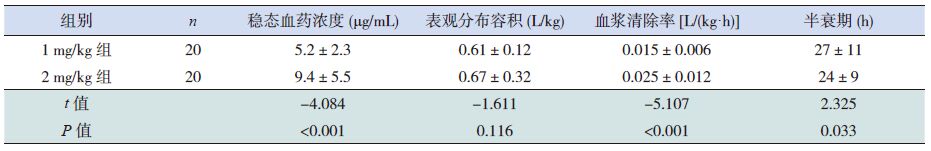
2mg/kg 组的稳态血药浓度、血浆清除率明显高于1 mg/kg 组,半衰期低于1 mg/kg 组,差异有统计学意义(P<0.05);而两组患儿的表观分布容积差异无统计学意义(表 2)。
|
|
表 2 两组患儿的药代动力学参数 (x±s) |
Pearson 相关分析的结果显示,1 mg/kg 和2 mg/kg 两组患儿的氨茶碱血浆清除率与生后日龄(r 分别为0.782 及0.826,均P<0.05)及校正胎龄(r 分别为0.351 及0.841,均P<0.05)均呈正相关(图 1~2);而与体重无相关性(r 分别为0.144及0.027,均P>0.05)。
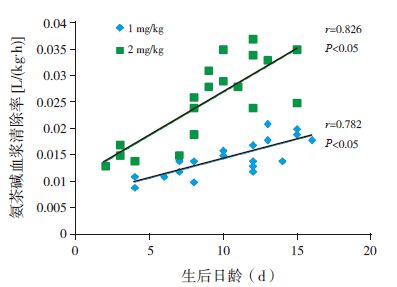
|
图 1 氨茶碱血浆清除率与生后日龄的相关图 |
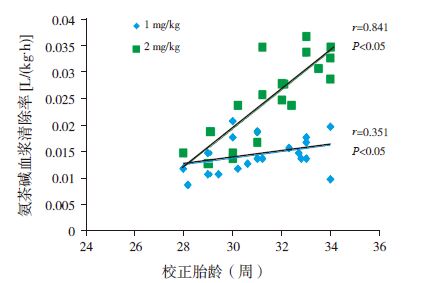
|
图 2 氨茶碱血浆清除率与校正胎龄的相关图 |
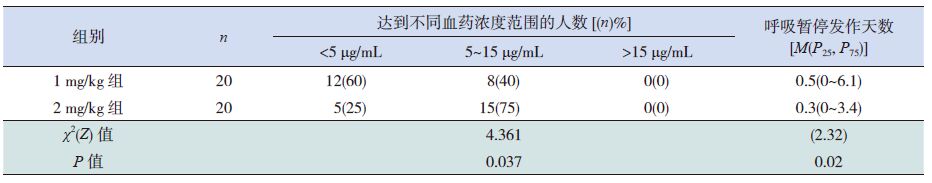
2mg/kg 组中75% 的患儿稳态血药浓度达到5~15 μg/mL,明显高于1 mg/kg 组(40%)(χ2=4.361,P=0.037);2 mg/kg 组生后7 d 内发生呼吸暂停天数也明显少于1 mg/kg 组(Z=2.32,P=0.02)(表 3)。
|
|
表 3 中文两组患儿的药效学比较标题 |
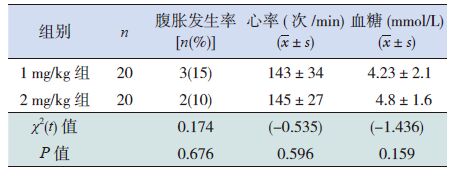
两组患儿腹胀的发生率差异无统计学意义,而且用药1 h 后心率和血糖水平的差异也均无统计学意义(表 4)。
|
|
表 4 两组患儿的不良反应发生情况比较 |
呼吸暂停是早产儿的常见并发症之一,控制呼吸暂停是早产儿呼吸管理的重要内容。临床用于防治呼吸暂停的药物主要为甲基黄嘌呤类药物[6, 7]。甲基黄嘌呤类药物为非选择性腺苷受体拮抗剂,通过拮抗腺苷的中枢呼吸抑制作用,刺激呼吸化学感受器,增加中枢呼吸驱动;增加机体对CO2的敏感性;增加每分钟通气量;并促进膈肌的收缩和呼吸肌功能,从而起到防治呼吸暂停的作用[2, 10, 11]。自20 世纪70 年代开始,甲基黄嘌呤药物被用于防治早产儿呼吸暂停,临床主要使用的是氨茶碱及枸橼酸咖啡因,二者在防治早产儿呼吸暂停的效果是相当的[3, 12]。
氨茶碱为茶碱与乙二胺的复盐,其药理作用主要来自于茶碱,乙二胺使其水溶性增强。在成人,氨茶碱85%~90% 主要在肝脏内代谢清除,其代谢依赖于细胞色素P450 同工酶CYP1A2 及CYP2E1[9, 13]。而由于新生儿肝内CYP1A2 极低,仅约40% 氨茶碱在肝内代谢,另约50% 通过肾脏以原型形式清除[8, 9]。本课题组前期研究发现,由于极低出生体重儿与成年人氨茶碱的代谢特点不同使得其药代动力学参数同成年人比具有较大差异,其表观分布容积大、清除率小、半衰期长[9]。氨茶碱的治疗剂量与中毒剂量较为接近,现行的指南中推荐的维持治疗剂量范围较广,为1~2 mg/kg[6, 7]。
MW/Pharm 3.6 是荷兰Mediware 公司开发的药代动力学软件,是较为主流的药代动力学软件之一[14]。国外研究显示,该软件采用的两步迭代贝叶斯拟合法同其他群体药代动力学模型如标准两步法(STS)、非线性混合效应模型(NONMEM)及全面两步法(GST)具有良好的可比性[15]。本课题组前期研究也证实了使用该软件能成功预测患儿血药浓度- 时间曲线[9]。
本研究显示,不同氨茶碱维持剂量的稳态血药浓度、血浆清除率及半衰期存在差异,2 mg/kg组患儿稳态血药浓度、血浆清除率明显高于1 mg/kg 组,半衰期低于1 mg/kg 组,这与氨茶碱在体内代谢时其消除与剂量呈非线性关系的特点有关[16]。两组患儿的氨茶碱血浆清除率均显示出与患儿的生后日龄及校正胎龄呈正相关,这与新生儿肾小球滤过率随生后日龄增加而增加这一规律相符,也与本课题组前期研究结果一致[9]。此外,氨茶碱本身能增加肾血流量及肾小球滤过率,从而起到利尿的作用[11]。本研究显示2 mg/kg 组患儿的血浆清除率高于1 mg/kg 组,且半衰期较短,可能与氨茶碱的利尿作用增加了药物清除有关。
现行的指南提出氨茶碱防治呼吸暂停的有效血药浓度为5~15 μg/mL[6, 7]。本研究显示,2 mg/kg组中75% 的患儿稳态血药浓度达到5~15 μg/mL,明显高于1 mg/kg 组(40%);而且2 mg/kg 组患儿7 d 内呼吸暂停发生的天数明显少于1 mg/kg 组,说明2 mg/kg 的治疗效果优于1 mg/kg。研究认为当血药浓度超过20 μg/mL 可能出现惊厥等严重不良反应[13]。本研究中两组患儿均未发现血药浓度高于15 μg/mL 者;另外,两组患儿腹胀发生率无显著差异,且两组患儿用药后1 h 的心率、血糖亦无显著差异,提示2 mg/kg 的维持剂量并不会增加不良反应的发生。
患儿对氨茶碱的反应并不仅仅取决于血药浓度,是否合并感染、严重颅内出血、内环境紊乱等也会影响治疗效果。合并用药尚可能影响早产儿对甲基黄嘌呤药物的清除,如大环内酯类抗生素可降低其代谢,而苯巴比妥可增加甲基黄嘌呤类药物的清除、西咪替丁可减少其清除[9, 13, 16]。尚有研究提示腺苷受体的基因多态性与甲基黄嘌呤类的治疗应答密切相关[10]。本研究显示,在使用氨茶碱防治极低出生体重儿呼吸暂停时,2 mg/kg的维持剂量效果均优于1 mg/kg,且不良反应的发生并未增加。但极低出生体重儿不同维持剂量氨茶碱药代动力学及药效学参数具有较大差异,并不能将血药浓度水平是否达到推荐范围与治疗是否有效相等同。本研究结果提示氨茶碱的药代动力学参数与校正胎龄及生后日龄呈正相关,且维持剂量高者相关性越强,故在进行剂量调整时应考虑患儿的校正胎龄及生后日龄,同时需进行常规血药浓度监测。
综上,在使用氨茶碱防治极低出生体重儿呼吸暂停时,推荐使用2 mg/kg 的维持剂量,但需同时进行常规的血药浓度监测以指导临床用药。
| [1] | Schmidt B, Roberts RS, Davis P, et al. Caffeine therapy for apnea of prematurity[J]. N Eng J Med, 2006, 354(20): 2112-2121. |
| [2] | Zhao J, Gonzalez F, Mu DZ. Apnea of prematurity: from cause to treatment[J]. Eur J Pediatr, 2011, 170(9): 1097-1105. |
| [3] | Armanian AM, Badiee Z, Afghari R, et al. Prophylactic aminophylline for prevention of apnea at higher-risk preterm neonates[J]. Iran Red Crescent Med J, 2014, 16(8): e12559. |
| [4] | Schmidt B, Roberts RS, Davis P, et al. Long-term effects of caffeine therapy for apnea of prematurity[J]. N Eng J Med, 2007, 357(19): 1893-1902. |
| [5] | Butler TJ, Firestone KS, Grow JL, et al. Standardizing documentation and the clinical approach to apnea of prematurity reduces length of stay, improves staff satisfaction, and decreases hospital cost[J]. Jt Comm J Qual Patient Saf, 2014, 40(6): 263-269. |
| [6] | 叶鸿瑁. 呼吸暂停[M]//邵肖梅, 叶鸿瑁, 丘小汕. 实用新生儿学. 第4版. 北京: 人民卫生出版社, 2011: 245-247. |
| [7] | 中华医学会儿科学分会新生儿学组. 早产儿管理指南[J]. 中国当代儿科杂志, 2005, 77(1): 1-7. |
| [8] | Lowry JA, Jarrett RV, Wasserman G, et al. Theophylline toxicokinetics in premature newborns[J]. Arch Pediatr Adolesc Med, 2001, 155(8): 934-939. |
| [9] | 石晶, 陈大鹏, 熊英, 等. 极低出生体质量儿氨茶碱药代动力学研究[J]. 四川大学学报(医学版), 2013, 44(2): 291-294. |
| [10] | Kumral A, Tuzun F, Yesilirmak DC, et al. Genetic basis of apnoea of prematurity and caffeine treatment response: role of adenosine receptor polymorphisms: genetic basis of apnoea of prematurity[J]. Acta Paediatr, 2012, 101(7): e299-e303. |
| [11] | 王薇. 氨茶碱的临床应用与用药安全[J]. 中国现代药物应用, 2010, 4(8): 140-141. |
| [12] | Henderson-Smart DJ, Steer PA. Caffeine versus theophylline for apnea in preterm infants[J]. Cochrane Database Syst Rev, 2010, (1): CD000273. |
| [13] | 陈世才,刘宪军. 氨茶碱和常用抗菌药物的相互作用[J]. 合理用药, 2008, 6(2): 24-28. |
| [14] | Proost JH, Meijer DK. MW/Pharm, an integrated software package for drug dosage regimen calculation and therapeutic drug monitoring[J]. Comput Biol Med, 1992, 22(3): 155-163. |
| [15] | Bennett JE, Wakefield JC. A comparison of a Bayesian population method with two methods as implemented in commercially available software[J]. J Harmacokinet Biopharm, 1996, 24(4): 403-432. |
| [16] | 陈瑞玲, 张艳梅, 赵志刚. 228例氨茶碱血药浓度监测分析[J]. 中国医院用药评价与分析, 2009, 9(3): 214-215. |
 2015, Vol. 17
2015, Vol. 17