2. 福建医科大学附属第二医院儿科, 福建 泉州 362018;
3. 福建医科大学附属泉州第一医院 ICU, 福建 泉州 362000;
4. 温州医科大学附属育英儿童医院呼吸科, 浙江 温州 325027
支气管哮喘是儿童最常见的慢性呼吸道疾病。近十余年来,随着儿童生活环境的巨大变化,哮喘患病率明显升高,给家庭和社会带来了沉重的负担[1]。研究表明,长期坚持使用吸入性糖皮质激素(inhaled corticosteroid,ICS)有利于哮喘控制,减少因哮喘发作导致的急诊和住院治疗[2]。然而,由于糖皮质激素对生长的抑制作用,在哮喘儿童中广泛应用ICS 也引起了家长和临床医生的担忧。虽然ICS 极大地降低了糖皮质激素的系统副作用,但对于儿童生长和身高的影响一直存在争议。由于儿童在各阶段的生长并非呈单纯线性,因此,中短期的研究对终身高的评估价值有限[3]。当前国内外还没有研究针对成年终身高的Meta 研究,本文拟通过系统评价和Meta 分析的方法更加准确地对儿童哮喘、ICS 治疗与成年终身高的关系作出定性和定量评价,为儿童哮喘治疗的安全性提供依据。
1 资料与方法 1.1 文献检索在PubMed、BCI、EMbase、Web of Science、中国知网和万方数据库中以“asthma*”、“height”、“stature*”、“growth”、“child*”、“infan*”、“adolescen*”、“pediatr*”或其对应的中文词目为检索词,全面检索截止于2014 年10 月公开发表的有关儿童哮喘和ICS 治疗与成年终身高的相关文献,不限制语种。同时,人工检索相关研究的参考文献以寻找到更多的相关报道。各项研究间若出现样本重叠,则纳入最新的或者最完整的报道。
1.2 哮喘对成年终身高影响相关文献的纳入和排除标准(1)纳入标准:①研究对象为成年人;②暴露因素为儿童期哮喘发病史;③对照组为无哮喘病史的健康人;④结局变量为成年终身高;⑤研究类型为观察性研究。
(2)排除标准:①会议摘要、病例报告未被纳入本次研究;②研究对象未达到成年终身高;③研究中未设立对照组。
1.3 ICS 治疗对哮喘患者成年身高影响相关文献的纳入和排除标准(1)纳入标准:①研究对象为成年人,且在儿童期患有轻到中度持续性哮喘;②暴露因素为成年前的ICS 治疗史;③对照为成年前未接受ICS治疗的哮喘患者或无哮喘病史的健康人或自身的预期身高;④结局变量为成年终身高;⑤研究类型为观察性研究或实验性研究。
(2)排除标准:①会议摘要、病例报告未被纳入本次研究;②研究对象未达到成年终身高。③研究中未设立对照组;④同时包含系统性糖皮质激素和ICS,且两者数据未分开描述的研究也被剔除;⑤研究未对性别进行分组分析。
1.4 质量评价文献的质量评价根据研究类型不同而采用相应的标准,分别由两名作者独立进行评价,结果不一致时由第3 名作者裁决。其中,队列研究采用Newcastle-Ottawa 量表,而横断面研究采用美国卫生保健质量和研究机构的推荐标准来进行评价,该量表一共11 个条目,分别用“是”、“否”及“不清楚”作答,这种方式不利于文献之间的比较,因此,对于达到条目标准的记为1 分,而未达到标准或未描述清楚的记为0 分,方便比较。
1.5 数据提取每篇文献由两名作者独立进行数据的提取,当提取的数据不一致时由第3 名作者裁决。提取的信息包括:第一作者、发表时间、研究地点、研究设计类型、样本量以及研究对象年龄、性别、哮喘发病年龄、成年身高和对照组来源及校正因素等。
1.6 统计学分析采用STATA 12.1 统计软件对数据进行分析,各项研究间的异质性使用Q 和I 2 检验,当Q 统计量的P<0.1 时,认为存在异质性;当I 2 ≥ 25%、50% 和75% 时,则认为分别存在轻度、中度和高度的异质性。然后,使用随机效应模型合并各项研究提供的均数差及其标准误。若研究未提供标准误,则使用其相应的95%CI 或标准差来计算。本研究采用三种比较方法来评估ICS 治疗对成年终身高的影响,分别为ICS 治疗组和非ICS 治疗组身高的加权均数差,ICS 治疗组和健康对照组身高的加权均数差以及ICS 治疗组和其相应的目标终身高的加权均数差。最后,以文献逐一排除的敏感性分析方法评价Meta 分析结果的稳定性。除特殊说明,P<0.05 为差异有统计学意义。
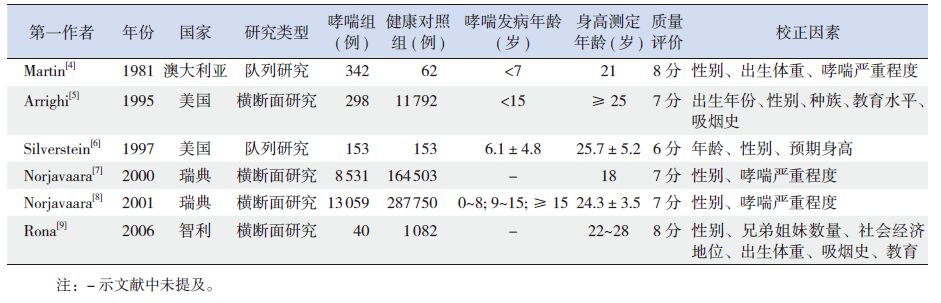
2 结果 2.1 纳入文献的基本情况和质量评价初检出相关文献4 554 篇,根据既定的纳入和排除标准,分别进行标题、摘要和全文阅读进行筛查后,剔除了4 544 篇,最终有10 篇研究纳入本次系统评价和Meta 分析,全部来源于英文数据库。其中,儿童哮喘与成年终身高的相关研究共6 项,发表时间为1981 年到2006 年,总共包括22 423名哮喘患者、465 342 名健康对照,其中包括2 项队列研究,质量评分分别为8 分和6 分,4 项横断面研究,平均评分 7.25 分;儿童ICS 治疗与成年终身高的相关研究共4 项,发表时间为1999 年到2012 年,总共包括562 名使用ICS 的哮喘患者、793 名使用其他治疗的哮喘患者、187 名健康对照,其中包括2 项队列研究,质量评分分别为8 分和9分,2 项横断面研究,评分分别为8 分和10 分。纳入文献的基本情况和质量评价见表 1~2。
|
|
表 1 儿童期哮喘和成年终身高关系的相关研究基本情况和质量评价 |
|
|
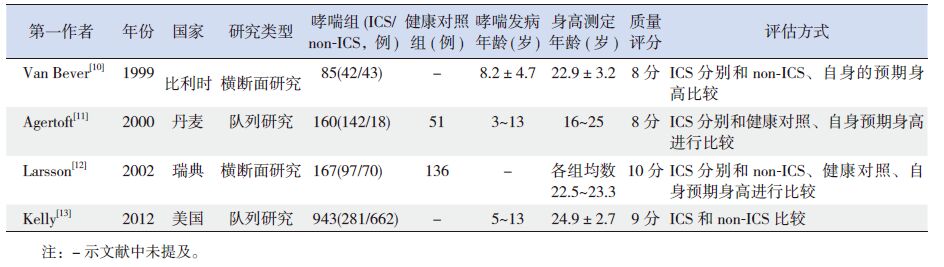
表 2 儿童期哮喘应用ICS 和成年终身高关系的相关研究基本情况和质量评价 |
纳入系统评价的6 篇相关研究由于分组方法和分析方式不同,不适合进行Meta 分析。这6 项研究分布于1981 年到2006 年的成年人,期间跨越了哮喘治疗方式的转变(由其他治疗手段转向ICS 治疗),因此,各项研究中,哮喘患者接受的治疗并不一致,即使在同一项研究的不同人群,其治疗方式也有所转变[7]。这些研究中,3 项研究(哮喘患者/ 对照样本量分别为342/62、153/153、40/1 082) 显示儿童期哮喘对成人终身高无影响[4, 6, 9];Norjavaara 等[7] 利用服役体检报告(8 531 名哮喘患者/164 503 名对照)和妊娠妇女入院资料(13 059 哮喘患者/287 750 名对照)[8] 进行了两项研究,结果表明,总体上哮喘对成年终身高有轻微影响(分别降低0.7 cm 和0.2 cm),且和哮喘严重程度相关;1 项由Arrighi 等[5] 进行的研究(哮喘患者298 名/ 对照11 792 名)仅在没有接受高等教育的黑人女性哮喘患者(黑人哮喘患者34 名/ 对照1 308 名)中发现了成年终身高的下降(1.85 英寸≈ 4.7 cm),其他亚组并无影响。
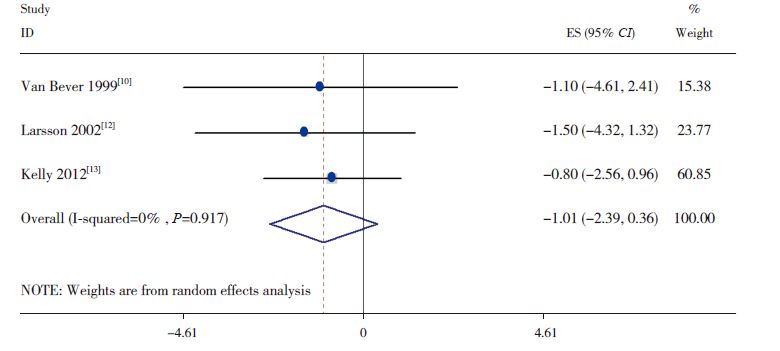
2.3 ICS 治疗对哮喘患者成年终身高影响的Meta分析和系统评价 2.3.1 哮喘患者ICS 治疗与其他治疗方案对成年身高的影响有三项报道[10, 12, 13] 设立了其他药物或安慰剂为对照组进行研究,其中在男性的研究间无显著异质性(I 2=0%,P=0.917)(图 1);而在女性的研究间存在中度异质性(I 2=67.4%,P=0.047),三项研究不适宜行数据合并。使用ICS 治疗的男性哮喘患者比使用其他治疗方法的哮喘患者的成年期平均身高低1.01 cm(95%CI:-2.39~0.36),敏感性分析显示,剔除任一项研究并不影响结果;在女性的三项研究结果中显示了不同的趋势,其中两项研究显示ICS 治疗趋向于降低成年终身高,而一项显示ICS 治疗趋向于增加成年终身高,但是这三项研究结果均没有统计学意义。
|
图 1 男性ICS 治疗组和非ICS 治疗组成年终身高的加权均数差 |
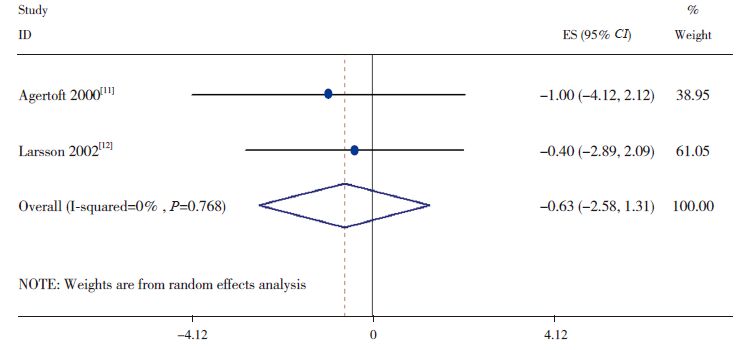
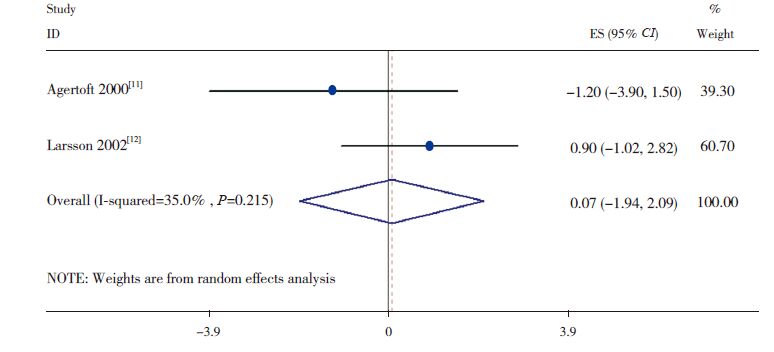
仅有两项研究[11, 12] 报告了这方面的结果,其中在男性的研究间无显著异质性(I 2=0%,P=0.768)(图 2),而在女性的研究中存在轻度异质性(I 2=35.0%,P=0.215)( 图 3)。使用ICS 的男性哮喘患者比健康对照组的终身高降低0.63 cm(95%CI:-2.58~1.31),在女性则升高了0.07 cm(95%CI:-1.94~2.09),且在男性和女性的敏感性分析中均显示了相似的结果。
|
图 2 男性ICS 治疗组和健康对照组成年终身高的加权均数差 |
|
图 3 女性ICS 治疗组和健康对照组成年终身高的加权均数差 |
有三项研究[10, 11, 12] 使用父母的身高预测了患者的终身高,并比较两者的差距。结果在男性和女性的研究中分别显示了高度(I 2=79.4%,P=0.008)和中度的异质性(I 2=52.5%,P=0.122),不适宜行数据合并。在男性和女性中,三项研究均表明接受过ICS 治疗的患者仍然可以达到预期终身高,甚至有超过预期身高的趋势。
3 讨论通过本项研究结果得出,儿童轻度哮喘对成年终身高并不会造成影响,中到重度哮喘可能会对成年终身高造成轻微影响,但并不具有临床意义。而在儿童哮喘患者中使用ICS 治疗,还是能达到预期的成年终身高,且和使用其他治疗方案的哮喘患者和健康对照之间,并不存在统计学上的显著性差异,因此,具有较好的安全性。
虽然哮喘对身高会造成影响的观点已经提出了几十年,但是由于哮喘本身疾病进展的复杂性以及治疗手段的发展和多样性,使得确切地研究哮喘对成人终身高的影响产生了一定的难度,因此,虽然本研究在多个中英文数据库进行了全面检索,但相关的研究却非常少,且在研究对象、研究方法上均表现出较大的不一致性。通过本研究的系统评价,可以发现,重度哮喘患者还是应该引起临床医生的密切关注。哮喘对于身高增长的影响,主要是通过抑制生长激素- 类胰岛素样生长因子(GH-IGF-1)轴的功能及延迟了青春期发生和骨骼成熟实现的[14],因此,虽然中短期观察会注意到生长抑制,但是随后会出现生长追赶,最后达到正常成人身高[4]。所以只有通过评价成年终身高,才能真实地反映哮喘对身高的影响。
目前,国内外最新的儿童哮喘诊治指南均将ICS 作为哮喘长期治疗的首选药物,建议使用最低剂量维持治疗来降低ICS 带来的不利影响[15, 16]。2014 年8 月最新发布的GINA 指南中,要求儿童哮喘患者每年至少要监测1 次身高情况[15]。一项44 周的随机双盲对照试验显示,和安慰剂组相比,在每日应用ICS 的哮喘患儿出现线性生长的降低(1.1±0.3 cm)[17]。另一项最近的Meta 分析也发现,一年的ICS 治疗会出现线性生长率的下降(0.48 cm/ 年),其后几年这种下降相对不明显[18]。但最近一项长期随访观察发现,生长抑制只出现在开始ICS 治疗后的前一两年,其后身高差距并没有拉大,而是维持至成年[13]。也有研究表明和色甘酸钠治疗组比较,ICS 治疗6 个月会出现生长抑制(2 cm/ 年),其后这种抑制消失,且若在7~18 月使用安慰剂后,还会出现生长追赶[19]。因此,和哮喘本身对身高影响一样,只有对成年终身高进行评价,才能准确和真实地评价ICS 对于儿童哮喘患者身高的影响。本研究表明,虽然ICS治疗和非ICS 治疗相比,有降低身高的趋势,但并没有显著性差异。然而,非常有意思的是,ICS和预期身高相比,反而有增加趋势。这种矛盾可以用青春期延迟来解释。因此,总体上,从本研究结果来看,ICS 治疗并不会明显影响到哮喘儿童的成年终身高。
本研究主要的优势是使用了成年终身高作为结局事件,因此能够确切地评价儿童哮喘和ICS治疗对身高的影响,并且通过ICS 治疗和非ICS 治疗、健康对照、自身预期身高进行全面比较,可以更好地反映ICS 治疗对终身高的影响,而且纳入ICS 治疗对身高影响的相关研究均有较高的研究质量。不过,本研究本身也有一定缺陷。首先,由于研究性质问题,纳入的研究均为观察性研究;其次,有些亚组分析中存在较大的异质性,不能通过Meta 分析合并数据;最后,根据纳入条件和排除条件进行筛选文献后,获得的研究数量较少。因此,关注哮喘和ICS 治疗对身高的长期影响是十分必要的。
综上,儿童哮喘不会或者仅轻微降低成年终身高,由于哮喘严重程度和身高呈负相关,对于严重哮喘患者要给予更多关注。目前的证据不足以表明哮喘儿童的ICS 治疗会明显影响成年终身高,但这需要更多和更严格设计的研究来证实。
| [1] | 全国儿科哮喘协作组, 中国疾病预防控制中心环境与健康相关产品安全所. 第三次中国城市儿童哮喘流行病学调查[J]. 中华儿科杂志, 2013, 51(10): 729-735. |
| [2] | 中国哮喘儿童家长知信行调查项目组. 中国大陆29个城市哮喘患儿病情控制状况及影响因素[J]. 中华儿科杂志, 2013, 51(2): 90-95. |
| [3] | 宗心南, 李辉. 中国儿童身高与体重的生长模式及简单数学模型的建立[J]. 中华儿科杂志, 2009, 47(5): 371-375. |
| [4] | Martin AJ, Landau LI, Phelan PD. The effect on growth of childhood asthma[J]. Acta Paediatr Scand, 1981, 70(5): 683-688. |
| [5] | Arrighi HM, Boyd BK, Casty FE. Childhood asthma and adult height: Data from NHANES II[J]. Pediatr Asthma Allergy Immunol, 1995, 9(3): 157-163. |
| [6] | Silverstein MD, Yunginger JW, Reed CE, et al. Attained adult height after childhood asthma: effect of glucocorticoid therapy[J]. J Allergy Clin Immunol, 1997, 99(4): 466-474. |
| [7] | Norjavaara E, Gerhardsson De Verdier M, Lindmark B. Reduced height in swedish men with asthma at the age of conscription for military service[J]. J Pediatr, 2000, 137(1): 25-29. |
| [8] | Norjavaara E, Gerhardsson de Verdier M, Lindmark B. Adult height in women with childhood asthma--a population-based study[J]. Pharmacoepidemiol Drug Saf, 2001, 10(2): 121-125. |
| [9] | Rona RJ, Smeeton NC, Vargas C, et al. Untreated asthma, final height and sitting height/leg length ratio in Chile[J]. Respiratory Medicine, 2006, 100(5): 911-917. |
| [10] | Van Bever HP, Desager KN, Lijssens N, et al. Does treatment of asthmatic children with inhaled corticosteroids affect their adult height?[J]. Pediatric Pulmonology, 1999, 27(6): 369-375. |
| [11] | Agertoft L, Pedersen S. Effect of long-term treatment with inhaled budesonide on adult height in children with asthma[J]. N Engl J Med, 2000, 343(15): 1064-1069. |
| [12] | Larsson L, Gerhardsson de Verdier M, Lindmark B, et al. Budesonide-treated asthmatic adolescents attain target height: a population-based follow-up study from Sweden[J]. Pharmacoepidemiol Drug Saf, 2002, 11(8): 715-720. |
| [13] | Kelly HW, Sternberg AL, Lescher R, et al. Effect of inhaled glucocorticoids in childhood on adult height[J]. N Engl J Med, 2012, 367(10): 904-912. |
| [14] | Giannini C, Mohn A, Chiarelli F. Growth abnormalities in children with type 1 diabetes, juvenile chronic arthritis, and asthma[J]. Int J Endocrinol, 2014, 2014: 265954. |
| [15] | Global Strategy for Asthma Management and Prevention. 2014 Global Initiative for Asthma[R/OL]. http://www.ginasthma.org/. |
| [16] | 中华医学会儿科学会呼吸学组, 《中华儿科杂志》编辑委员会. 儿童支气管哮喘诊断与防治指南[J]. 中华儿科杂志, 2008, 46(10): 745-753. |
| [17] | Martinez FD, Chinchilli VM, Morgan WJ, et al. Use of beclomethasone dipropionate as rescue treatment for children with mild persistent asthma (TREXA): a randomised, double-blind, placebo-controlled trial[J]. The Lancet, 2011, 377(9766): 650-657. |
| [18] | Zhang L, Prietsch SO, Ducharme FM. Inhaled corticosteroids in children with persistent asthma: effects on growth[J]. Evid Based Child Health, 2014, 9(4): 829-930. |
| [19] | Turpeinen M, Nikander K, Pelkonen AS, et al. Daily versus as-needed inhaled corticosteroid for mild persistent asthma (The Helsinki early intervention childhood asthma study)[J]. Arch Dis Child, 2008, 93(8): 654-659. |
 2015, Vol. 17
2015, Vol. 17