支气管哮喘是以呼吸道慢性炎症和气道高反 应性为特征的变态反应性疾病,是儿童最常见的 慢性呼吸道疾病之一,严重影响儿童身心健康及 生活学习。全国儿科哮喘协作组曾先后三次进行 全国规模的儿童哮喘患病率调查,提示我国儿童 哮喘的患病率呈显著上升趋势[1]。全球哮喘防治创 议(GINA)推荐将吸入糖皮质激素(ICS)与长效 β2 受体激动剂(LABA)联合治疗作为持续哮喘 患者的首选治疗方案[2]。而儿童处于生长发育期, 长期吸入ICS 是否对生长发育产生严重不良影响, 是临床医师及家长非常担心的问题。本研究随访 观察哮喘患儿持续或间断吸入沙美特罗替卡松治 疗1 年,观察其临床疗效及对身高增长速率、体 质指数(BMI)的影响,以期指导临床对哮喘患儿 的治疗。 1 资料与方法 1.1 研究对象
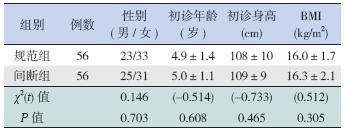
选取2012 年9 月至2013 年10 月于我院哮喘 门诊诊断并随访的支气管哮喘患儿112 例为研究 对象,其中男48 例,女64 例,初诊年龄4~8 岁, 均符合全国儿童哮喘防治协作组制定的儿童哮喘 诊断标准[3]。根据随访情况,将持续吸入药物的 患儿纳入规范化治疗组(规范组,n=56),间断 吸入药物的患儿纳入非规范化治疗组(间断组, n=56),治疗前两组患儿在性别、年龄、身高、 BMI 等方面比较差异均无统计学意义,具有可比性, 见表 1。
| 表 1 一般情况比较 [例或(x±s)] |
沙美特罗替卡松干粉剂( 生产批号: R541320,葛兰素史克),每掀含沙美特罗(SM)50 μg、丙酸氟替卡松(FP)100 μg。 1.3 检测方法及仪器
肺功能检测采用德国耶格公司MasterScope 肺 功能检测仪,观察指标包括一秒用力呼气容积 (FEV1)和呼气峰流速(PEF);BMI= 体重(kg)/ 身高2(m2)。 1.4 治疗方法
规范组患儿按GINA 方案给予吸入沙美特罗 替卡松的阶梯式治疗,初始剂量为100 μg/ 次, 2 次/d,后按随访情况维持并逐渐减量。间断组 因依从性差和/ 或担心长期吸入激素副作用等原 因,自行仅在有临床症状发作后短期内使用药物, 连续使用时间最长不超过1 个月,吸入剂量为 100 μg/ 次,2 次/d。在观察期间患儿有哮喘发作, 均予以相应对症药物治疗。治疗后6 个月、1 年时 临床随访评估患儿临床症状评分、肺功能主要指 标、身高增长速率及BMI 变化情况。 1.5 疗效判定方法
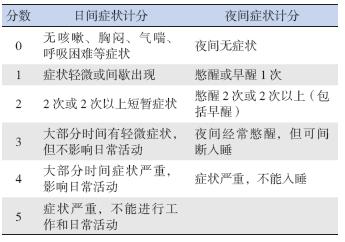
哮喘日间和夜间临床症状评分标准[3] 见表 2。
| 表 2 哮喘临床症状评分表 |
应用SPSS 20.0 统计软件对数据进行统计学分 析,正态分布计量资料采用均数± 标准差(x±s) 表示,两组间比较采用t 检验;非正态分布计量资 料采用中位数(四分位间距)[P50(P25,P75)] 表示, 组间比较采用秩和检验。计数资料采用例数表示, 两组间比较采用卡方检验。P<0.05 为差异有统计 学意义。 2 结果 2.1 两组治疗前后疗效比较
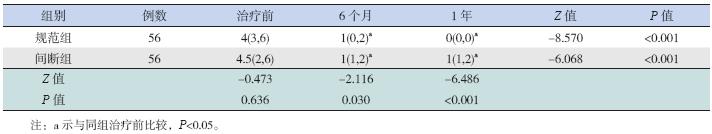
治疗前,规范组与间断组临床症状评分差异 无统计学意义(P>0.05);规范组、间断组治疗 6 个月、1 年后临床症状评分分别较治疗前减少 (P<0.01);随访6 个月及1 年后,规范组临床症 状评分较间断组明显减少(P<0.05)。见表 3。
| 表 3 哮喘患儿治疗前后临床症状评分 [P50(P25,P75)] |
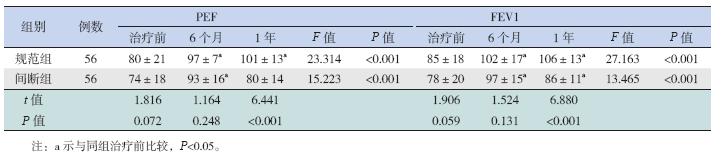
治疗前,PEF%、FEV1% 在规范组和间断组 间差异无统计学意义(P>0.05)。规范组PEF%、 FEV1% 在治疗6 个月、1 年后比治疗前明显增高 (P<0.05);间断组FEV1% 在治疗6 个月、1 年 后比治疗前增高,PEF% 在治疗6 个月时比治疗前 增高(P<0.05),但PEF% 在治疗1 年后与治疗 前比较差异无统计学意义(P>0.05);治疗1 年后, 规范组PEF% 和FEV1% 均高于间断组(P<0.01)。 见表 4。
| 表 4 哮喘患儿治疗前后肺功能情况 (x±s,%) |
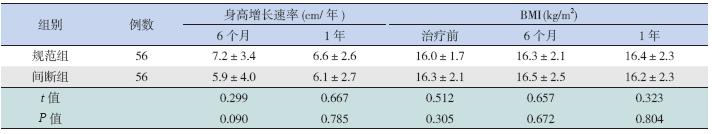
两组患儿随访期间身高增长速率差异无统计 学意义(P>0.05),且治疗后身高增长均在正常儿 童增长范围内(5~7 cm/ 年)[4];两组患儿治疗前 后BMI 值差异均无统计学意义(P>0.05),且在 正常儿童范围内[4]。见表 5。
| 表 5 治疗期间身高增长速率及BMI 变化情况 (x±s) |
GINA 方案指出儿童支气管哮喘作为一种慢 性疾病需要正确选择药物及疗程进行规范治疗。 近年来,随着健康教育的推广,大多数医务人员 意识到规范治疗的正确性,但患儿家长的认识程 度尚不足。GINA 推荐持续吸入激素与长效β2 受 体激动剂联合治疗为哮喘患者的首选治疗方案。 SM 为长效β2 受体激动剂,与气道平滑肌细胞 β2 受体结合后,产生持久的舒张支气管作用,且能降低气道高反应性和炎症介质的释放[5]。而FP 为ICS,能抑制炎症细胞的活化与迁移,还能启 动β2 受体基因,增强人体肺组织细胞膜上β2 肾 上腺素能受体转录和呼吸道黏膜上β2 受体蛋白 的合成,逆转β2 受体的下调[6]。黄英等[7] 观察了 145 名中重度哮喘患儿,发现沙美特罗替卡松能有 效改善患儿PEFam 及临床症状,且临床应用安全, 不良反应发生率仅1. 4%。Barnes 等[8] 也发现予以 沙美特罗替卡松联合治疗持续性哮喘比单用FP 在 改善PEF 及临床症状上有更好的效果。
本研究发现,规范组在6 月、1 年随访时, 临床症状评分较前明显减少,且PEF、FEV1 有显 著提高。间断组在治疗6 个月、1 年后随访时,临 床症状评分较前虽有减少,FEV1%也有提高,但 PEF%仅在6 个月时有提高,1 年时较前无显著改 善。临床随访观察1 年,规范组临床症状评分明 显低于间断组,且肺功能各指标也高于间断组。 说明吸入沙美特罗替卡松能改善哮喘患儿临床症 状及提高肺功能,且规范吸入药物能更好的控制 临床症状,使肺功能维持在较好水平。
哮喘患儿需长期吸入激素治疗,吸入ICS 对 儿童生长发育,尤其是身高、体重的影响是医生 及家长重点关注和担心的问题。本研究结果提示, 规范或间断吸入激素后6 个月、1 年时对患儿身高 增长速率及BMI 无明显影响,且两组患儿身高增 长速率均在儿童正常增长范围。
Guilbert 等[9] 观察了285 名有哮喘高危因素的 儿童,吸入FP 治疗两年后,吸入组平均身高增长 比安慰剂组少1.1 cm,停药后1 年,平均身高增 长比安慰剂组少0.7 cm。提示吸入激素有潜在降 低哮喘儿童身高增长速率的可能。但本研究给予 哮喘儿童吸入沙美特罗替卡松治疗1 年,发现患 儿身高增长速率同正常儿童,并未发现对患儿身 高增长有影响。且Kelly 等[10] 对入组儿童哮喘管 理计划研究小组(CAMP)的1 041 例受试者中的 943 例(90.6%)患儿的成年后身高进行了测量, 与安慰剂组相比,布地奈德治疗组平均成年身高 降低了1.2 cm,说明即使长期吸入ICS 治疗儿童哮 喘,对儿童的最终身高也不会造成显著的影响, 与本研究结论一致。
ICS 可造成脂代谢异常,测量BMI 能监测ICS 对患儿体型的影响。Kostic 等[11] 观察100 例7~ 18 岁的哮喘患儿使用吸入激素治疗1 年,患儿 BMI 基本正常。国内王涛等[12] 研究显示予以89 例 哮喘患儿吸入FP 治疗(按规律减药)1 年,治疗 前后BMI 差异无统计学意义。上述研究与本研究 结论一致,提示吸入ICS 对患儿体型无明显影响。
根据本研究结果可知,规范吸入沙美特罗替 卡松比间断用药能更好的控制临床症状,改善肺 功能,提高患儿的生活质量。吸入药物1 年对患 儿身高增长速率及BMI 无明显影响,所以短期吸 入沙美特罗替卡松治疗儿童哮喘是安全有效的。
| [1] | 全国儿科哮喘协作组. 第三次中国城市儿童哮喘流行病学调 查[J]. 中华儿科杂志, 2013, 51(10): 729-735. |
| [2] | 陈育智. 2006 年全球哮喘防治创议(GINA)解读[J]. 中国 实用儿科杂志, 2007, 22(9): 643-649. |
| [3] | 中华医学会儿科学分会呼吸学组, 《中华儿科杂志》编辑委 员会. 儿童支气管哮喘诊断与防治指南[J]. 中华儿科杂志, 2008, 46(10): 745-753. |
| [4] | 李辉, 季成叶, 宗心南, 等. 中国0-18 岁儿童、青少年身高、 体重的标准化生长曲线[J]. 中华儿科杂志, 2009, 47(7): 487- 492. |
| [5] | Baraniuk JN, Ali M, Brody D, et al. Glucocorticoids induce beta2-adrenergic receptor function in human nasal mucosa[J]. Am J Respir Crit Care Med, 1997, 155(2): 704-710. |
| [6] | Barnes PJ. Scientific rationale for inhaled combination therapy with long-acting beta 2-agonists and corticosteroids[J]. Eur Respir J, 2002, 19(1): 182-191. |
| [7] | 黄英, 李艳, 刘恩梅, 等. 沙美特罗替卡松联合治疗儿童中 重度哮喘的临床研究[J]. 重庆医科大学学报, 2005, 30(1): 132-135. |
| [8] | Barnes NC, Jacques L, Goldfrad C, et al. Initiation of maintenance treatment with salmeterol/fluticasone propionate 50/100 microg bd versus fluticasone propionate 100 microg bd alone in patients with persistent asthma: integrated analysis of four randomized trials[J]. Respir Med, 2007, 101(11): 2358-2365. |
| [9] | Guilbert TW, Morgan WJ, Zeiger RS, et al. Long-term inhaled corticosteroids in preschool children at high risk for asthma[J]. N Engl J Med, 2006, 354(19): 1985-1997. |
| [10] | Kelly HW, Sternberg AL, Lescher R, et al. Effect of inhaled glucocorticoids in childhood on adult height[J]. N Engl J Med, 2012, 367(10): 904-912. |
| [11] | Kostic G, Ilic N, Petrovic M, et al. Body mass index in asthmatic children before and after one year inhaled glucocorticosteroids therapy BMI[J]. Med Pregl, 2010, 63(5-6): 409-413. |
| [12] | 王涛, 李云, 叶义言, 等. 吸入糖皮质激素对哮喘儿童骨龄 及生长发育的影响[J]. 中国当代儿科杂志, 2012, 14(5): 359- 361. |
 2015, Vol. 17
2015, Vol. 17