近年来,由于抗生素的广泛应用,导致医院 内感染率,尤其是术后耐药菌的感染率逐年增加, 其中预防性应用抗生素是其中的危险因素之一[1]。 基于这个原因,我国近年来加强了对抗生素的管 理力度,国内各级医院抗生素的应用日趋规范, 尤其围手术期预防性使用抗生素,得到了有效控 制,已成为衡量一个医院抗生素应用是否合理和 规范的重要评价依据。我院以往术前抗生素的预 防性使用也比较普遍,但自2013 年进行“三甲复 审”以来,医院强化了抗生素的管理,进行了抗 生素专项整治活动,清洁刀口围手术期预防性使 用抗生素受到严格限制,介入治疗按清洁刀口执 行。这样一来,虽然抗生素的使用率明显下降了, 但医生们心中不免有些担忧:术后院内感染是否 会增加?尤其人体重要器官,如心脏、大脑、眼 等的介入手术,虽然很清洁,但一旦发生感染, 后果将不堪设想。目前国内外有很多关于介入手 术预防性使用抗生素是否必要的研究,但针对小 儿先心病介入治疗方面的研究却很少,缺乏很成 熟的经验可以遵循。因此,不预防性使用抗生素 对儿科医生介入治疗先心病将是一个很大的挑战。 我院小儿内科自2013 年始,对经导管介入治疗的 先心病患儿均未预防性使用抗生素。本研究针对 术前不应用抗生素,是否会增加院内感染的机会, 与2012 年病例做了一个回顾性的对比分析,发现 近期术后感染无明显增加趋势。虽然不是同期对 照,可比性方面存在一定的不足,但我院近两年 介入的病种、导管室的无菌条件、仪器设备、进 行介入操作的技术人员以及使用的介入器材等没 有发生明显变化,具有一定可比性。 1 资料与方法 1.1 研究对象
2012 年1~12 月我院小儿内科经导管介入治 疗的先心病患儿118 例作为抗生素使用组(对照 组)。患儿年龄4 个月至12 岁;男65 例,女53 例; 房间隔缺损18 例,室间隔缺损47 例,动脉导管 未闭33 例,肺动脉狭窄20 例,使用介入器材除 弹簧圈及Balt 球囊外,均为国产封堵器。预防应 用抗生素的时间均为术前半小时。所用抗生素为 国产头孢呋辛,剂量为60 mg/(kg·次),溶于0.9% 氯化钠50 mL 中静脉滴注,30 min 滴入。如果手 术持续3 h 以上,则按原剂量追加1 次。
2013 年1~12 月我院小儿内科经导管介入治 疗的先心病患儿125 例作为未用抗生素组(试验 组)。患儿年龄4 个月至12 岁;男69 例,女56 例; 房间隔缺损19 例,室间隔缺损50 例,动脉导管 未闭35 例,肺动脉狭窄21 例。所用介入器材与 对照组相同。术前均未预防性使用抗生素。我院 近两年介入治疗的病种、导管室的无菌条件及人 员配备、仪器设备配置、进行介入操作的技术人 员以及使用的介入器材等没有发生明显变化,两 组间不存在显著性差异。 1.2 统计学分析
采用SPSS 17.0 统计软件进行数据分析。两组 间计数资料的比较采用卡方检验,P<0.05 为差异 有统计学意义。 2 结果
对照组介入术后发生院内感染11 例(9.3%), 其中5 例为急性上呼吸道感染,2 例肺炎,1 例泌 尿系感染,1 例急性胃肠炎,2 例不明原因发热。 血培养均阴性。复查心脏超声心内膜光滑,无赘 生物形成,排除感染性心内膜炎。以上病例发生 感染的时间在术后1~5 d 不等,均经抗感染、对症 处理后3~7 感染完全控制。
试验组介入术后发生院内感染13 例(10.4%), 其中7 例为急性上呼吸道感染,3 例肺炎,3 例不 明原因发热。血培养均阴性。复查心脏超声心内 膜光滑,无赘生物形成,排除感染性心内膜炎。 以上病例发生感染的时间亦在术后1~5 d 不等,均 经抗感染、对症处理后3~7 d 感染完全控制。
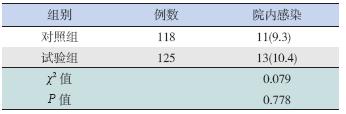
两组患儿出院后随访1~2 年,均无一例远期 介入相关感染病例发生。卡方检验显示,两组术 后院内感染的发生率差异无统计学意义(P>0.05), 见表 1。
| 表 1 两组介入术后院内感染发生率的比较 [例(%)] |
随着抗生素的广泛应用,细菌耐药明显增加, 多重感染显著增多,临床医生选择抗生素的难度 也就越来越大[2]。因此,如何最大限度地不预防性 使用抗生素,防患于未然,防止和减少耐药菌的 出现,是临床上公认的一个难题,也是每个临床 医生义不容辞的责任。
一般认为,预防介入术后院内感染的重点环 节有:(1)加强导管室的管理,使手术操作间 环境严格无菌无尘[3];(2)缩短病人手术前的住 院时间;(3)手术者严格无菌操作,提高技术水 平,缩短手术时间;(4)严格手术器械消毒灭菌。 (5)预防使用抗生素。基于上述原因,在国家集 中整顿抗生素应用活动前,国内各级医院普遍存 在抗生素应用比例过高、不规范的现象;特别是 外科系统预防性使用抗菌药物的问题尤为严重, 有的医院甚至超过内科系统治疗性应用比例,把 应用抗生素看成预防术后感染最有力、最有效的 手段。为有效地遏制抗生素滥用现象,国家卫生 部于2004 年下发了关于“抗菌药物临床应用指导 原则”的通知,该文件对抗菌药物应用的规范提 出了明确的规定,也收到了良好的效果。在此基 础之上,2009 卫生部又发布了“卫办医政发38 号 文件”,对外科手术预防性使用抗菌药物作出了 明确而具体的规定:医疗机构要重点加强Ⅰ类切 口(清洁切口)手术预防使用抗菌药物的管理和 控制。Ⅰ类切口手术一般不预防使用抗菌药物, 确需使用时,要严格掌握适应证,仅在以下情况 时可考虑预防用药:(1)手术范围大、时间长; (2)手术涉及重要脏器,一旦发生感染将造成严 重后果者,如头颅手术、心脏手术、眼内手术等; (3)异物植入手术,如人工心脏瓣膜植入、永久 性心脏起搏器放置;(4)高龄或免疫缺陷者等高 危人群。介入手术按Ⅰ类切口管理。目前国内学 者对心脏介入手术的患者,是否预防性使用抗生 素,所持观点不一,多数认为因涉及人体重要器官, 应用是很有必要的[4];但总的趋势是抗生素使用越 来越规范,应用的时间短、剂量小、强度低、价格廉、 对可能的病原体更有针对性,而且相对于预防院 内感染的众多举措来讲,越来越居次要位置。有 研究认为,心脏介入患者的医院感染是可以预防 控制的,增强医护人员感染防范意识,建立有效 的感染防控制度,严格无菌技术操作是减少心血 管介入患者医院感染的关键[5]。另有研究认为,介 入手术不预防性使用抗生素,不会增加血管介入 术后院内感染的发生率[6];不合理地预防应用抗菌 药物,不但达不到预防感染的目的,反而造成机 体菌群失调和耐药菌的出现,增加感染机会,故 有学者认为患者进行介入前要进行临床综合分析, 既要注意到用药的针对性和在组织中的浓度,又 要考虑到不良反应等不利因素,全面权衡,结合 临床治疗效果和药敏试验选择预防用药[7]。美国的 Ryan 等[8] 认为,没有随机样本的临床试验证实院 内感染的有效控制源于预防性使用抗生素,是否 所有的心血管介入手术都不预防性使用仍需进一 步论证。爱尔兰医生Beddy 等[9] 报告,心血管介入病人的术后感染几率很低,有很少的证据说明 预防性使用抗生素能有效地预防感染,反而会增 加机体产生抗药性的危险,他们认为手术过程和 手术技巧是术后感染的主要因素,应从这个角度 着手预防感染;美国的Covey 等[10] 通过对植入静 脉通道装置的病人观察发现,未预防性应用抗生 素者术后早期感染的发生率小于1%,因此他们认 为此类介入手术抗生素的预防性应用是不被推荐 的。
本研究显示,不预防性使用抗生素并未增加 介入患儿术后感染率,而且患儿出现的院内感染 多数为上呼吸道感染,无一例为穿刺部位感染及 感染性心内膜炎等严重并发症,提示只要严格把 握好医院感染的各个环节,抗生素的预防应用对 于心脏介入手术不是必需的。本研究试验组未预 防性使用抗生素,并未增加心脏介入手术后医院 感染率,我们的体会是:(1)我院对抗生素的管 理非常严格;(2)医护人员积极配合,无菌观念 及无菌操作技术过硬;(3)我院拥有心脏介入专 用导管室,管理非常规范;(4)所有介入器材均 使用一次性的,不给医院感染留下任何缝隙。但 是,必须说明的是:(1)心脏介入术所用材料的 包装、运输、消毒等环节均由厂家负责,医院无 法控制这些环节;(2)全国导管室的条件不一; (3)导管室人员的消毒、无菌执行程度不一; (4)对于心血管内介入性操作,一旦发生感染, 后果不仅是发生心内膜炎,还有可能发生败血症、 脑脓肿等迁徙性脓肿、栓塞或死亡,如果该用而 未用抗生素,后果是很可怕的。加之本研究随访 的时间相对较短,病例数相对有限,所得结果不 一定具有普遍性意义,在可行性方面仍需要更严 谨的前瞻性的研究结果,仍有待于全国多中心、 大样本、长期随访的随机对照研究来获得更有说 服力的循证医学证据,以得出更为可靠的结论。
| [1] | 刘建华, 刘新锋, 帅金凤, 等. 儿童产超广谱β- 内酰胺酶菌 株感染危险因素分析[J]. 中国当代儿科杂志, 2011, 13(12): 959-961. |
| [2] | 单玉霞, 崔振泽, 黄燕. 儿童感染性肺不张的临床分析[J]. 中 国当代儿科杂志, 2014, 16(8): 856-859. |
| [3] | 时芳莉. 介入导管室的管理与预防感染[J]. 中华医院感染学 杂志, 2011, 21(12): 2599. |
| [4] | 周娟华, 葛琴芬. 心血管患者介入诊断治疗医院感染发生率 及预防管理措施[J]. 中华医院感染学杂志, 2012, 22(8): 1614- 1615. |
| [5] | 崔杨文, 胡必杰, 马坚, 等. 政策干预对9808 例心脏介入 操作抗菌药物预防性应用的影响[J]. 中华医院感染学杂志, 2012, 23(7): 1673-1675. |
| [6] | 曹军, 刘洪强, 何阳, 等. 血管介入治疗预防性应用抗菌药 物对术后感染发生率影响的临床研究[J]. 临床和试验医学杂 志, 2013, 12(12): 924-925. |
| [7] | 赵雪芳, 狄韵漫. 心脏介入术后血管相关性血流感染因素分 析及干预对策[J]. 中华医院感染学杂志, 2012, 22(7): 1359- 1350. |
| [8] | Ryan JM, Ryan BM, Smith TP. Antibiotic prophylaxis in interventional radiology[J]. Vasc Interv Radiol, 2004, 15(6): 547-556. |
| [9] | Beddy P, Ryan JM. Antibiotic prophylaxis in interventional radiology—anything new?[J]. Tech Vasc Interv Radiol, 2006, 9(2): 69-76. |
| [10] | Covey AM, Toro-Pape FW, Thornton RH, et al. Totally implantable venous access device placement by interventional radiologists: are prophylactic antibiotics necessary?[J]. J Vasc Interv Radiol, 2012, 23(3): 358-362. |
 2015, Vol. 17
2015, Vol. 17