近几年来,异基因造血干细胞移植术(allo-HSCT)在儿童血液病,如难治性及复发的白血病、重型再生障碍性贫血(AA)等的应用逐渐增多且日趋成熟,但是移植后的造血功能恢复及移植物反应仍然是影响移植成功的关键。目前针对急性移植物抗宿主病(aGVHD)的治疗比如激素、免疫抑制剂及各种单抗的应用仅可使部分aGVHD患儿达到缓解,间充质干细胞(MSC)的出现为aGVHD的治疗提供了一种新的方法,其安全性及有效性亦逐渐被认可[1, 2]。本研究中10例血液病患儿allo-HSCT后出现aGVHD,在激素加免疫抑制剂治疗效果不佳的基础上予人脐带间充质干细胞(hUC-MSC)输注治疗,10例患儿aGVHD症状均达到不同程度的缓解,现报道如下。 1 资料与方法 1.1 研究对象
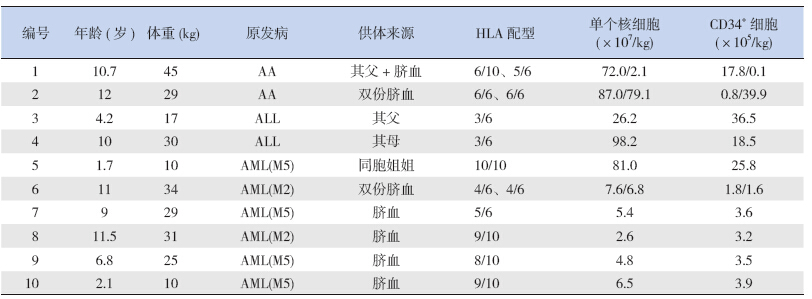
研究对象为2011年4月至2014年4月10例行allo-HSCT的血液病患儿,10例患儿的基本情况见表 1。病例1、2为AA患儿,其中病例1存在血小板输注无效,且常规环孢素免疫抑制及其他促造血药物治疗效果不佳;病例2两次抗淋巴细胞球蛋白/抗胸腺细胞球蛋白冲击治疗血象不升。病例3系急性淋巴细胞性白血病(ALL)复发患儿。病例4系ALL高危组患儿,化疗过程中微小残留白血病(MRD)有升高趋势,提示复发可能。病例5~10为急性髓性白血病(AML)患儿,均为二次化疗才达到缓解,部分初诊时即存在中高危的指标。故以上病例均符合MSC移植的指征。
| 表 1 患儿基本情况 |
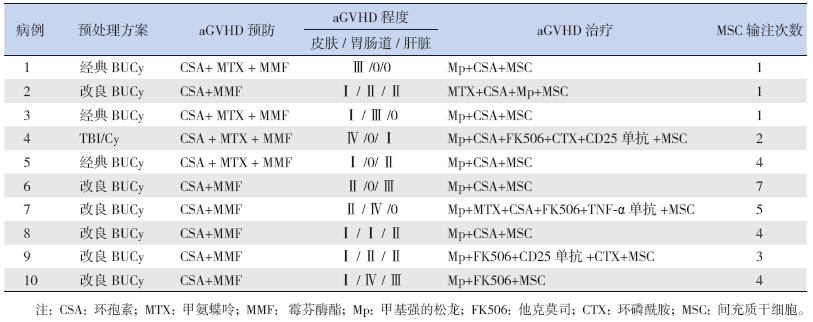
根据儿童身体状况、原发病及化疗反应,采用的预处理方案也有所不同。病例1、3、5采用经典BUCy预处理方案(马利兰+环磷酰胺+阿糖胞苷),病例4采用TBI /Cy 方案预处理(全身照射放疗+马利兰+环磷酰胺+阿糖胞苷化疗),病例2、6、7、8、9、10采用改良BUCy预处理(氟达拉宾+马利兰+环磷酰胺+阿糖胞苷)。其中病例1、2、6、8 HLA抗体阳性,加用利妥昔单抗预处理。aGVHD的预处理方案见表 2。
| 表 2 aGVHD的预防与治疗 |
10例患儿中,病例1、3、4、5行亲缘异基因造血干细胞移植,余行无关脐血异基因造血干细胞移植。HLA配型上既有半相合也有全相合,输注的骨髓单个核细胞(MNC)数及CD34阳性细胞数目见表 1。 1.4 aGVHD的预防、程度及治疗
脐血移植患儿采用环孢素+霉芬酶酯预防aGVHD,亲缘移植采用环孢素+甲氨蝶呤+霉芬酶酯预防aGVHD。按照aGVHD诊断标准[3, 4],将患儿aGVHD程度分为Ⅱ至Ⅳ度不等。在甲基强的松龙(Mp)、环孢素(CSA)抗aGVHD治疗的前提下加用甲氨蝶呤(MTX)、CD25单克隆抗体、环磷酰胺(CTX)、TNF-α单抗治疗,每位患儿根据aGVHD程度不同,加用的抗aGVHD药物亦不同,在治疗效果不佳(>3 d)时加用MSC治疗(表 2)。 1.5 MSC的制备过程
MSC由苏州大学附属第一医院卫生部血栓与止血重点实验室制备,已经过相关部门伦理批准,并且获脐带捐献者亲属的同意,hUC-MSC接受者签署了MSC治疗同意书。MSC具体制备步骤如下:取出生理盐水浸泡的一段无菌脐带组织,打开经高压蒸汽灭菌的脐血包(内含弯盘两个、组织剪一把、无齿镊一把),将脐带置于含aMEM弯盘中,用组织剪将脐带一段一段剪碎,加入0.25%Ⅳ型胶原酶消化处理后,37℃震荡2 h,离心取沉淀的细胞用aMEM多次洗涤,接种于T-75 cm2培养瓶中,内含10%胎牛血清、1%双抗的aMEM培养液。显微镜下观察细胞形态,待成纤维样贴壁细胞贴满瓶壁时可进行胰酶消化传代培养。传至第3代,进行流式细胞仪( BD FACScalibur 型)检测,结果显示,第3代MSC 均高表达CD44、CD90、CD73、CD105抗原(>95%),不表达CD31、CD45、HLA-DR及CD34 抗原(<5%)。用第3代的经鉴定的MSC细胞用于临床研究。 1.6 MSC的管理
MSC输注前予患儿1 mg/kg甲基强的松龙静脉滴注,根据患儿体重,每次予患儿静脉输注MSC的量为1~5单位(1单位=1×106 MSC)不等,MSC平均输注量8.68×105/kg,输注时间>1 h,患儿输注MSC结束后仍继续观察2 h。MSC单次输注效果不明显者予多次输注,输注间隔1~2周。
MSC治疗有效性的判断:aGVHD的所有症状及体征消失为“完全缓解”;aGVHD减少至少一个级别为“部分缓解”;aGVHD症状无改善为“无效”[5]。
MSC治疗的安全性评估:分析MSC输注后的1周内患儿外周血常规及生化检查结果有无异常变动,记录MSC输注后30 d内的不良反应。 2 结果
10例患儿移植后出现Ⅱ~Ⅳ度aGVHD,出现时间平均为33 d(+20 d ~ +66 d),累及皮肤、肝脏、胃肠道,其中10例出现皮肤aGVHD,7例患儿出现移植相关的肝脏损害,6例出现胃肠道aGVHD,见表 2。
在糖皮质激素加用环孢素/他克莫司治疗后,病例1、2、3、5、6、8、10 aGVHD症状无明显改善(>3 d),遂予MSC输注支持治疗。MSC输注治疗后病例1获部分缓解;病例10为重度aGVHD患儿,4次MSC输注结束后肠道aGVHD始终无改善。病例2、3、5、6、8经MSC输注后所有aGVHD症状均可达到缓解。
病例4、7、9为中重度aGVHD(Ⅱ~Ⅳ),移植后基础治疗为甲基强的松龙+环孢素/他克莫司。病例4移植后+32 d出现肝脏损害,移植后+38 d出现 90%全身体表皮肤剥脱伴大量水疱形成,加用环磷酰胺、保肝药物、他克莫司、CD25单抗治疗后,肝功能及皮肤损害无改善,于+50 d首次应用MSC(3 u)输注治疗,肝功能+54 d即恢复正常,皮肤水疱较前略减少,间隔10 d后再次应用MSC(3 u)输注治疗,患儿+66 d皮肤水疱消失,逐渐愈合。病例7移植后存在肝脏损害同时胃肠道反应较重,单次应用MSC(2 u)5 d后肝功能好转,但患儿仍腹泻如前,后他克莫司与TNF-α单抗各应用一次,1周后患儿肠道反应仍无减轻,而后MSC(2 u)每1~2周予患儿输注一次,患儿腹泻次数逐渐减少,至最后一次MSC输注结束,患儿大便成形,次数1~2次/d,量正常,未再诉腹痛。病例9皮肤、胃肠道及肝脏均有aGVHD表现,CD25单抗治疗无效后,经过3次输注MSC(2 u)后所有aGVHD症状缓解。
综上,MSC输注治疗后8例aGVHD达到完全缓解,2例(病例1、10)达到部分缓解,总有效率(完全缓解+部分缓解)为100%。MSC输注起效时间平均为移植后59 d(+28 d ~ +93 d),其中所有肝脏aGVHD患儿在MSC治疗后肝脏损害均可达到完全缓解,肝脏损害平均开始改善时间为输注后+12 d(+6 d ~ +20 d);10例皮肤aGVHD患儿中,病例1经MSC治疗后可控制,余9例达完全缓解;6例肠道aGVHD患儿中,病例10为重度aGVHD患儿,经MSC治疗后症状无缓解,余5例肠道aGVHD患儿可完全缓解,该5例肠道aGVHD平均缓解时间为输注后+41 d(+10 d ~ +60 d)。中位随访时间为385 d(60~1 095 d)时,2例死亡,其中病例1移植后+97 d死于感染性脑炎,病例2移植后约23个月死于慢性移植物抗宿主病,余8例患儿存活。该10例患儿在随访时间内未出现aGVHD复发,且均未出现药物毒副反应。 3 讨论
allo-HSCT为恶性血液病提供了根治手段,但其常见的主要并发症aGVHD严重影响着患者的生存质量与存活率,其相关病死率占移植后死亡的50% 以上,是目前导致造血干细胞移植后患者死亡的主要原因[6]。根据患者年龄、所患疾病种类及状况、移植前状态、HLA配型结果等[7],患儿移植后可出现0 ~Ⅳ度不等的aGVHD,部分进展为激素耐药性aGVHD,对基本抗排斥药物治疗效果不佳,MSC的应用为激素耐药性aGVHD提供了新的治疗手段。MSC为一群不具有免疫特异原性的细胞,对allo-HSCT后的aGVHD有治疗作用[1]。研究报道MSC主要通过以下几个方面治疗aGVHD: (1)MSC通过与T细胞的接触,既可抑制CD4+T细胞亦可抑制CD8+ T细胞,其抑制作用并不靶向抗原特异性的T细胞[2, 8];(2)MSC通过与调节性T细胞共培养的方式增加调节性T细胞数目,调节性T细胞具有潜在免疫调节作用,可抑制自身免疫和免疫耐受[9];(3)Th1/Th2比例的调节,MSC 可抑制引起炎症因子释放的Th1细胞比例下降,而促进具抗炎作用的Th2细胞增多[10]。综上,MSC细胞可以通过抑制T细胞增殖及炎性细胞因子的产生、增加调节性T细胞、纠正Th1/Th2的平衡来达到免疫系统的正常化[6]。
首先将MSC应用于临床aGVHD治疗的是Le Blanc 等人[11],2004年LeBlanc 等报道9岁的ALL患儿行不相关的HLA匹配的HSCT后出现Ⅳ度aGVHD,常规的治疗药物包括激素、利妥昔单抗、霉芬酶酯等治疗无效,经两次输注来自于患儿母亲的MSC后,aGVHD完全缓解。2006年Ringden等[12]报道MSC用于治疗8名成年人移植后出现的激素耐药性aGVHD,5例达到完全缓解,1例部分缓解,2例治疗效果不佳,后死于aGVHD。LeBlanc等[13]于2008年将MSC应用于激素耐药的55例成人患者,治疗有效率达70%,Prasad等[14]报道MSC成功治疗重度aGVHD儿童,部分MSC来源于HLA不相合的供者,所有患儿经MSC治疗后均可达不同程度的缓解,治疗过程中未出现输注不良事件。MSC的取材来源有人骨髓间充质干细胞(hBM-MSC)与hUC-MSC,二者具有相同的免疫表型而且都具备低免疫原性及体外免疫抑制功能。与hBM-MSC相比,hUC-MSC取材方便,易于分离,且体外扩增能力更强[15]。本研究中MSC均取自正常足月产胎儿脐带,经体外扩增鉴定后应用于常规抗排斥药物治疗效果不佳的10例aGVHD患儿,加用MSC输注治疗后均达到不同程度的缓解,且未出现MSC相关的不良反应发生,与相关文献报道一致[11, 12]。本研究10例肝脏aGVHD患儿经MSC治疗后肝脏损害均可达到完全缓解,肠道aGVHD患儿中,有1例经MSC输注治疗后无改善,且经MSC治疗后肠道排斥反应改善时间较肝脏aGVHD改善时间要久,这可能与aGVHD程度差异及个体差异有关,是否能说明MSC对治疗肝脏aGVHD要优于肠道aGVHD仍需要进一步累积更多的样本、更深入的研究才能做出正确的评价。
综上,免疫抑制剂等常规抗排斥药物仅可治愈部分aGVHD,hUC-MSC输注为aGVHD提供了一种新的治疗手段。本研究成功制备了hUC-MSC并用于治疗10例aGVHD患儿,该10例患儿均达到不同程度的缓解,且均未出现MSC相关毒副反应,提示hUC-MSC输注治疗具备良好的有效性与安全性。
| [1] | 陈广华, 杨婷, 田竤, 等. 脐带间充质干细胞治疗糖皮质激素耐药的严重型急性移植物抗宿主病19 例分析[J]. 中华血液学杂志, 2012, 33(4): 303-306. |
| [2] | Maitra B, Szekely E, Gjini K, et al. Human mesenchymal stem cells support unrelated donor hematopoietic stem cells and suppress T-cell activation[J]. Bone Marrow Transplant, 2004, 33(6): 597-604. |
| [3] | Rowlings PA, Przepiorka D, Klein JP, et al. IBMTR severity index for grading acute graft-versus-host disease: retrospective comparison with Glucksberg grade[J]. Br J Haematol, 1997, 97(4): 855-864. |
| [4] | 张之南, 沈悌. 移植物抗宿主病[M]. 血液病诊断及疗效标准, 北京: 科学出版社, 2007: 268-271. |
| [5] | Introna M, Lucchini G, Dander E, et al. Treatment of graft versus host disease with mesenchymal stromal cells: a phase I study on 40 adult and pediatric patients[J]. Biol Blood Marrow Transplant., 2014, 20(3): 375-381. |
| [6] | Robin M, Porcher R, De Castro Araujo R, et al. Risk factors for late infections after allogeneic hematopoietic stem cell transplantation from a matched related donor[J]. Biol Blood Marrow Transplant, 2007, 13(11): 1304-1312. |
| [7] | 江华, 缪艳, 陈静, 等. 异基因造血干细胞移植治疗儿童高危急性髓系白血病28例疗效分析[J]. 中国实用儿科杂志, 2013, 28(8): 601-605. |
| [8] | Amorin B, Alegretti AP, Valim V, et al. Mesenchymal stem cell therapy and acute graft-versus-host disease: a review[J]. Human Cell, 2014, 27(4): 137-150. |
| [9] | Taylor PA, Lees CJ, Blazar BR. The infusion of ex vivo activated and expanded CD4+CD25+ immune regulatory cells inhibits graft-versus-host disease lethality[J]. Blood, 2002, 99(10): 3493-3499. |
| [10] | Amir AL, Hagedoorn RS, van Luxemburg-Heijs SA, et al. Identification of a coordinated CD8 and CD4 T cell response directed against mismatched HLA Class I causing severe acute graft-versus-host disease[J]. Biol Blood Marrow Transplant, 2012, 18(2): 210-219. |
| [11] | Le Blanc K, Rasmusson I, Sundberg B, et al. Treatment of severe acute graft-versus-host disease with third party haploidentical mesenchymal stem cells[J]. Lancet, 2004, 363(9419): 1439-1441. |
| [12] | Ringden O, Uzunel M, Rasmusson I, et al. Mesenchymal stem cells for treatment of therapy-resistant graft-versus-host disease[J]. Transplantation, 2006, 81(10): 1390-1397. |
| [13] | Le Blanc K, Frassoni F, Ball L, et al. Mesenchymal stem cells for treatment of steroid-resistant, severe, acute graft-versus-host disease: a phase II study[J]. Lancet, 2008, 371(9624): 1579-1586. |
| [14] | Prasad VK, Lucas KG, Kleiner GI, et al. Efficacy and safety of ex vivo cultured adult human mesenchymal stem cells (ProchymalTM) in pediatric patients with severe refractory acute graft-versus-host disease in a compassionate use study[J]. Biol Blood Marrow Transplant, 2011, 17(4): 534-541. |
| [15] | Kern S, Eichler H, Stoeve J, et al. Comparative analysis of mesenchymal stem cells from bone marrow, umbilical cord blood, or adipose tissue[J]. Stem Cells, 2006, 24(5): 1294-1301. |
 2015, Vol. 17
2015, Vol. 17