2. 华北理工大学附属唐山市妇幼保健院放射科, 河北 唐山 063000
轻微的脑炎/脑病伴可逆性胼胝体压部病变综合征(mild encephalitis/encephalopathy with a reversible splenial lesion,简称MERS)是近几年提出的基于影像学表现特征的临床综合征。临床表现为以头颅MRI检查弥散加权成像(DWI)发现胼胝体压部有可逆性的高信号病变为特征[1]。这类临床-影像学综合征具有轻微脑炎/脑病的临床表现,可出现抽搐、意识障碍、视觉障碍等神经系统症状,但恢复较快。早期的病例报告大多认为预后良好。MERS可发生于各年龄人群,但以儿童多见。本研究对我院经MRI检查发现胼胝体压部有DWI高信号,符合MERS诊断标准的8例患儿的临床资料进行分析,现报告如下。
1 资料与方法 1.1 研究对象我院2013年11月至2016年3月确诊的8例MERS患儿为研究对象,其中男5例,女3例。发病年龄10个月至12岁,平均年龄5岁2个月。8例患儿共有9次发病(其中1例患儿复发,以精神不好、抽搐起病)。8例患儿均符合MERS诊断标准[2]:神经精神症状表现为精神行为异常或精神行为异常合并短暂的意识障碍12 h以上,脑脊液没有明显的炎性改变。8例患儿随诊3个月至2年确诊。
2 结果 2.1 临床表现(1)前驱症状:9次发作中起病前均有感染情况,其中发热5例,呕吐4例,腹泻1例, 咳嗽1例。
(2)神经系统症状:以抽搐就诊6例次,其中抽搐1次1例,抽搐2次以上3例,抽搐10次以上2例;以阵发性失明/视物不清就诊3例;伴意识障碍3例。
(3)阳性体征:1例3岁6个月男孩脑膜刺激征阳性,1例12岁女孩双侧巴氏征阳性;口腔黏膜和咽峡部可见疱疹1例, 诊断为疱疹性口炎;肺部听诊有中小水泡音1例,结合实验室结果诊断为支原体肺炎。
(4)实验室检查:9次发作时均进行了外周血白细胞计数检查,其中1例白细胞计数升高,为21.8×109/L,中性粒细胞75.84%,血培养阴性。9次发作时均进行了血生化检查,其中1例血钠降低,为130 mmol/L(参考范围:135~145 mmol/L),无低蛋白血症和酶学检查异常病例;4例进行了肺炎支原体(MP)抗体检测,其中MP抗体滴度≥1:80者3例;1例10个月的患儿以腹泻、呕吐起病,查大便轮状病毒抗原检测结果为阴性。9次发作时脑脊液常规及生化检查均正常。
(5)脑电图检查:9次发作均于住院72 h之内行4 h以上视频脑电图检查(至少包括1个睡眠-觉醒周期),表现为各导联可见广泛1.5~3.5 Hz δ波2例,有癎样放电1例,其余7次正常。
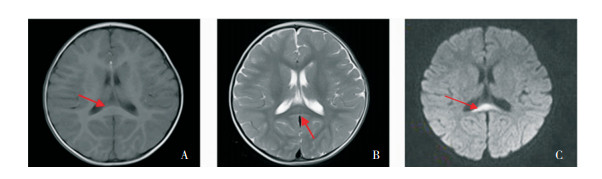
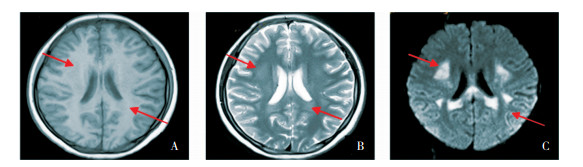
(6)神经影像学特点:患儿颅脑MRI均表现为胼胝体压部片状长T1、长T2信号,DWI高信号(图 1),其中1例同时伴有双侧半卵圆中心、部分颞叶白质对称多发长T1、长T2信号,DWI高信号(图 2),诊断符合MERSⅡ型(余为MERSⅠ型)[3]。
|
图 1 MERS患儿头颅MRI 头颅MRI胼胝体压部长T1(图A)、长T2(图B)、DWI高信号(图C),如箭头所示。 |
|
图 2 MERSⅡ型患儿头颅MRI 头颅MRI胼胝体压部、双侧半卵圆中心、部分颞叶白质长T1(图A)、长T2(图B)、DWI高信号(图C),如箭头所示。 |
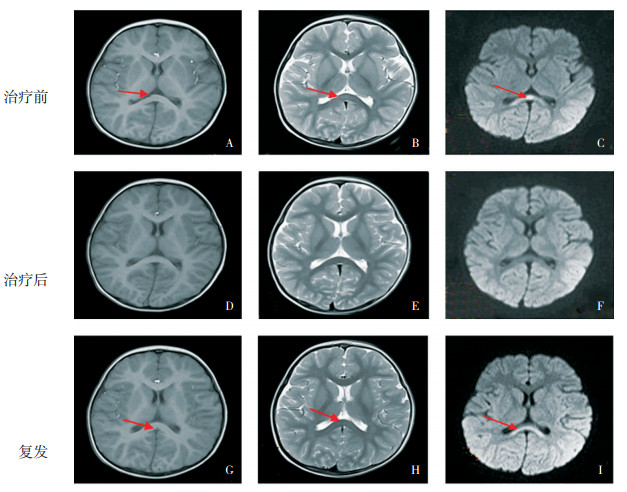
8例患儿9次发作5~30 d后复查头颅MRI,异常信号均消失。其中1例患儿以咳嗽6 d起病伴抽搐2次就诊,头颅MRI表现为胼胝体压部片状长T1、长T2信号,DWI高信号(图 3A~C),脑脊液常规、生化检查正常,抗炎治疗7 d后再次复查头颅MRI恢复正常(图 3D~F)。50 d后该患儿出现呕吐、精神差、睡眠多,1 d后又出现抽搐2次,再次MRI检查又表现为胼胝体压部片状长T1长T2信号,DWI高信号(图 3G~I),再次脑脊液检查常规、生化正常。1个月复查头颅MRI病变消失。
|
图 3 MERS复发病例头颅MRI 治疗前头颅MRI表现为胼胝体压部片状长T1信号(图A),长T2信号(图B),DWI高信号(图C);抗炎治疗7 d后再次复查头颅MRI恢复正常(图D~F)。50 d后复发,MRI检查又表现为胼胝体压部片状长T1信号(图G),长T2信号(图H),DWI高信号(图I)。箭头所示为各异常信号。 |
2.2 治疗及转归
9例次的发作均给予了常规抗炎、抗病毒治疗,同时给予脱水降颅压。7例次给予常规量地塞米松治疗,2例次因疑似脱髓鞘病给予了大剂量甲基泼尼松龙冲击治疗3 d [15 mg/(kg·d)]。3例次同时给予了静脉丙种球蛋白治疗。2例次给予了抗癫癎治疗。随访3个月至2年,神经系统发育无异常。1例复发患儿第一次抗炎治疗7 d后复查MRI恢复正常;50 d后复发,再次抗炎治疗1周,1个月复查头颅MRI病变消失,至今神经、精神发育良好。
3 讨论日本学者Tada等[1]于2004年在脑炎/脑病的病人中,发现了一组临床、影像症候群,头颅MRI检查发现孤立的胼胝体压部损害,损害常逐渐消失,1个月内完全恢复。因此提出这可能是一种新的临床-影像综合征,并把其称为MERS。2014年Kashiwagi等[2]报道了22个伴随发热性疾病的病人23次MRI的DWI检查,发现胼胝体压部的可逆性损害,6例诊断为MERS,并进一步强化了MERS的概念。临床表现有意识障碍、精神行为异常、视觉障碍等,症状持续12 h以上诊断为MERS;对临床症状持续小于12 h的诊断为无脑炎/脑病的可逆性胼胝体压部病变(non-MERS)。随着对本综合征认识的不断深入,有学者发现MERS的病变不仅限于胼胝体压部,有时也可累及到整个胼胝体和(或)白质,并提出了MERS谱系的概念[3],将仅累及胼胝体压部的称其为MERSⅠ型,延伸到整个胼胝体和(或)白质受累的称其为MERSⅡ型。本研究8例MERS患儿中,7例诊断为MERSⅠ型,1例诊断为MERSⅡ型。MERS诊断的重要手段是头颅MRI,胼胝体压部可逆性病变为本综合征的特征性改变。头颅MRI表现最明显的为DWI高信号,部分患儿有稍长T1、长T2信号。病变大多为椭圆形或圆形,没有强化。累及胼胝体以外白质的需要注意与急性播散性脑脊髓炎、后头部可逆性脑病综合征、遗传性白质脑病及遗传代谢病累及白质等疾病进行鉴别。
此临床-影像学综合征常见于儿童,中枢神经系统症状相对较轻、持续时间较短,多在1个月内恢复。国内儿科病例由北京大学第一医院赵立荣等[4]于2014年首次报道。武汉市儿童医院孙丹等[5]于2015年报告8例。MERS发病多数与发热/感染性疾病有关,文献报告可占94%[6],包括呼吸道、消化道、泌尿道感染等。文献报道相关的病原有病毒、细菌、支原体、军团菌等。除发生在感染性疾病过程中,也可发生在非特异性炎症-川崎病的过程中[6-9]。本组8例患儿的9次发作均有前驱感染,伴发热5例,伴呕吐4例。诊断合并疱疹性口炎1例,支原体肺炎1例。1例外周血白细胞计数明显升高,达到了21.8×109/L,且中性粒细胞占75.84%,但细菌培养阴性。在病毒感染性疾病中文献报道比较多的有流感病毒、轮状病毒,此外还有疱疹病毒、腺病毒等[9-12]。本组有1例患儿以腹泻、呕吐起病,但大便轮状病毒抗原阴性。
MERS通常发生在感染后的第1~4天,表现为神经、精神症状和(或)意识障碍。最常就诊原因是神经、精神症状,包括幻视、幻听、情绪变化、无目的运动、冲动等,以往报道占61%[2]。其次是癫癎样发作和意识障碍,分别占33%和35%[1-2]。本组患儿9次发作中伴有神经、精神症状的有3例次,伴有意识障碍3例次;合并有癫癎样发作6例次。癫癎发作大多数发作都在2次以上,有的甚至达10余次,但发作的持续时间都很短暂,多不超过1 min,并且没有持续状态发生。Garcia-Monco等[13]总结报告了113例患者(包括儿童和成人)发病的主要因素中惊厥相关者占49例,可见MERS与癫癎发作关系密切。
目前对MERS的发病机制的认识尚不统一。比较多的学者认为病灶的可逆性变化是由于髓鞘磷脂层炎症反应引起短暂性脑白质髓鞘内细胞毒性水肿所致。由于MERS可发生于抗癫癎药的减量过程中,有人认为抗惊厥药物可能影响血管紧张素和抗利尿激素的浓度,使脑组织的水平衡系统发生紊乱。或者是由于抗惊厥药物的的毒性造成胼胝体压部的髓鞘水肿。也有推测是由于惊厥发作导致异常放电经胼胝体压部神经髓鞘传递、泛化,导致暂时性的能量代谢和钠-钾泵功能下降,限制了水的弥散导致髓鞘细胞毒性水肿[13]。而最近1例发生于新生儿的MERS使得脑白质髓鞘水肿[14]之说遭到质疑,因为新生儿的胼胝体压部髓鞘发育尚不完全。因此日本曾报道MERS合并有抗利尿激素分泌不当综合征,低钠可引起脑渗透压的改变导致脑水肿[14-15]。本组病人除1例血钠稍低外,并未发现明显的低血钠病例。所以这种感染诱发的脑胼胝体及部分白质的特征性“水肿”可能还有其他途径。还有学者通过对川崎病合并MERS的颅脑SPECT发现,本综合症患者发病时脑皮层、丘脑、基底节及双侧边缘系统低灌注,因此推测该综合症的发病可能是脑血管炎或脑血管的脱水导致的低灌注所致[16]。
此综合征常伴随感染和惊厥,是感染导致了胼胝体的病变继而出现惊厥发作还是惊厥发作引起了胼胝体的病变?本组患儿中有1例复发患儿,两次起病的前驱症状不同(第1次以咳嗽6 d起病,第2次以呕吐1 d起病),两次均合并抽搐,头颅MRI都表现为胼胝体压部可逆性DWI高信号,两次均完全恢复。这究竟是感染所致的胼胝体压部的病变导致抽搐,还是抽搐所致胼胝体压部的病变尚不清楚。文献报道该病预后良好,多数于1周至1个月胼胝体MRI改变消失[1]。然而本组病例的经验及最新的文献均提示胼胝体病变可能复发[17],另有文献报道本病可导致胼胝体的神经胶质细胞异常,使胼胝体体积缩小[18]。因此本症的预后还需要积累更多经验和长期追踪研究。
| [1] | Tada H, Takanashi J, Barkovich AJ, et al. Clinically mild encephalitis/encephalopathy with a reversible splenial lesion[J]. Neurology , 2004, 63 (10) : 1854–1858. DOI:10.1212/01.WNL.0000144274.12174.CB |
| [2] | Kashiwagi M, Tanabe T, Shimakawa S, et al. Clinico-radiological spectrum of reversible splenial lesions in children[J]. Brain Dev , 2014, 36 (4) : 330–336. DOI:10.1016/j.braindev.2013.05.007 |
| [3] | Takanashi J, Barkovich AJ, Shiihara T, et al. Widening spectrum of a reversible splenial lesion with transiently reduced diffusion[J]. AJNR Am J Neuroradiol , 2006, 27 (4) : 836–838. |
| [4] | 赵立荣, 吴晔, 郭芒芒, 等. 伴胼胝体压部可逆性病变的轻度脑炎/脑病儿童病例一例并文献复习[J]. 中华儿科杂志 , 2014, 52 (3) : 218–222. |
| [5] | 孙丹, 王芳, 刘智胜, 等. 儿童轻微脑炎/脑病伴可逆性胼胝体压部病变谱系疾病临床-影像分析[J]. 临床儿科杂志 , 2015, 33 (11) : 929–932. |
| [6] | Takanashi J. Two newly proposed infectious encephalitis/encephalopathy syndromes[J]. Brain Dev , 2009, 31 (7) : 521–528. DOI:10.1016/j.braindev.2009.02.012 |
| [7] | Hoshino A, Saitoh M, Oka A, et al. Epidemiology of acute encephalopathy in Japan, with emphasis on the association of viruses and syndromes[J]. Brain Dev , 2012, 34 (5) : 337–343. DOI:10.1016/j.braindev.2011.07.012 |
| [8] | Hibino M, Hibi M, Akazawa K, et al. A case of Legionnaires' pneumonia accompanied by clinically mild encephalitis/encephalopathy with a reversible splenial lesion (MERS) with transient altered mental status and cerebellar symptoms, which responded to treatment by antibiotics and corticosteroid[J]. Nihon Kokyuki Gakkai Zasshi , 2011, 49 (9) : 651–657. |
| [9] | Takanashi J, Shirai K, Sugawara Y, et al. Kawasaki disease complicated by mild encephalopathy with a reversible splenial lesion (MERS)[J]. J Neurol Sci , 2012, 315 (1-2) : 167–169. DOI:10.1016/j.jns.2011.11.022 |
| [10] | Bulakbasi N, Kocaoglu M, Tayfun C, et al. Transient splenial lesion of the corpus callosum in clinically mild influenza-associated encephalitis/encephalopathy[J]. AJNR Am J Neuroradiol , 2006, 27 (9) : 1983–1986. |
| [11] | Ito S, Shima S, Ueda A, et al. Transient splenial lesion of the corpus callosum in H1N1 influenza virus-associated encephalitis/encephalopathy[J]. Intern Med , 2011, 50 (8) : 915–918. DOI:10.2169/internalmedicine.50.4147 |
| [12] | Fuchigami T, Goto K, Hasegawa M, et al. A 4-year-old girl with clinically mild encephalopathy with a reversible splenial lesion associated with rotavirus infection[J]. J Infect Chemother , 2013, 19 (1) : 149–153. DOI:10.1007/s10156-012-0421-8 |
| [13] | Garcia-Monco JC, Cortina IE, Ferreira E, et al. Reversible splenial lesion syndrome (RESLES):What's in a name[J]. J Neuroimaging , 2011, 21 (2) : 1–14. DOI:10.1111/jon.2011.21.issue-2 |
| [14] | Takanashi J, Maeda M, Hayashi M. Neonate showing reversible splenial lesion[J]. Arch Neurol , 2005, 62 (9) : 1481–1482. DOI:10.1001/archneur.62.9.1481 |
| [15] | 张扬, 陈为安, 毕涌, 等. 107例伴有胼胝体压部可逆性病灶的临床症状轻微的脑炎/脑病临床分析[J]. 中华全科医学 , 2014, 12 (6) : 875–876. |
| [16] | 王淑辉, 郭燕军, 周春来, 等. 伴有胼胝体压部可逆性病灶的临床症状轻微的脑炎/脑病1例报道并文献复习[J]. 中国神经免疫学和神经病学杂志 , 2012, 19 (1) : 33–36. |
| [17] | Sato T, Ushiroda Y, Oyama T. Kawasaki disease-associated MERS:pathological insights from SPECT findings[J]. Brain Dev , 2012, 34 (7) : 605–608. DOI:10.1016/j.braindev.2011.09.015 |
| [18] | Kashiwagi M, Tanabe T, Ooba C, et al. Differential diagnosis of delirious behavior in children with influenza[J]. Brain Dev , 2015, 37 (6) : 618–624. DOI:10.1016/j.braindev.2014.09.003 |
 2016, Vol. 18
2016, Vol. 18

