2. 武汉市儿童医院检验科, 湖北 武汉 430016;
3. 武汉市儿童医院内科, 湖北 武汉 430016
胆汁淤积是胆汁从肝细胞到十二指肠过程中肝细胞分泌功能失调和胆管排泄障碍所致的一种临床综合征,表现为黄疸和浅黄色大便,可伴深色尿、瘙痒、不能解释的出血和脂肪泻,生化指标上表现为总胆红素(total bilirubin,TBIL)、直接胆红素(direct bilirubin,DBIL)、γ谷氨酰转移酶(gamma glutamyl transpeptidase,GGT)、碱性磷酸酶(alkaline phosphatase,ALP)和总胆汁酸(total bile acid,TBA)升高[1]。该病是儿童期肝脏疾病就诊住院的首位原因,是婴儿阶段致死或者致残的重要原因之一[2]。国外流行病学资料研究显示,其发病率在出生婴儿为1/2 500~5 000[3]。熊去氧胆酸(ursodexycholic acid,UDCA)为大家公认的治疗婴幼儿及儿童肝内胆汁淤积的有效药物,但约有三分之一的患者对UDCA无效,这部分患者将面临着胆汁淤积肝纤维化、肝硬化、肝功能衰竭需要肝移植的严重后果[4]。
大黄属于蓼科植物范畴,最早《神农本草经》记载了大黄的主治功效,近几十年来,众多的肝脏和胆道疾病常常采用大黄煎剂的单味药物或以大黄为主要药物的复合制剂改善胆汁淤积[5, 6, 7]。中药大黄中的主要活性成分是大黄素(Emodin)。研究中,为了模拟建立符合婴幼儿及儿童期肝内胆汁淤积特点的动物模型,本研究选取的实验研究对象为生后3周离乳后大鼠,参照文献[8, 9]采用一次性灌胃给予每日α-萘异硫氰酸酯(alpha-naphthylisothiocyanate,ANIT)50 mg/kg建立幼龄大鼠肝内胆汁淤积的动物模型,观察不同剂量大黄素对幼龄大鼠肝脏的预防保护效果,为将来临床上合理使用大黄素治疗婴幼儿及儿童肝内胆汁淤积疾病提供新的实验依据。
1 材料与方法 1.1 实验动物SPF级离乳后3周龄Sprague Dawley(SD)大鼠,体重80~100 g,共120只,雌雄各半,购自湖北省疾病预防控制中心(合格证编号:11401300023489)。在华中科技大学同济医学院实验动物学部屏障系统中饲养(设施使用证明编号:132888)。
1.2 药物、试剂与仪器大黄素购自美国Sigma公司(规格:50 mg,批号:043K35051V);ANIT购自美国Alfa Aesar公司(规格:10 g,批号:STBD6070V);花生油购自美国Sigma公司(规格:500 g,批号:SLKD6527V);苏木精、伊红Y、无水乙醇、二甲苯、包埋石蜡、中性树脂胶均购自国药集团化学试剂有限公司;血清TBIL、DBIL、TBA、ALP、GGT、谷丙转氨酶(ALT)、谷草转氨酶(AST)试剂盒均购自南京建成生物工程研究所; 半自动生化仪(型号:PUS-2018N)为北京普朗公司产品。
1.3 剂量设计根据文献[10]中大黄素的急性毒性试验结果,大鼠的半数致死量为每日290 mg/kg,换算出来的中剂量为每日29~58 mg/kg;同时参照文献[11]选取中剂量(每日40 mg/kg)干预治疗方案。课题组前期也进行了预实验[8],按照大黄素剂量分为三组:即大黄素高剂量组(每日80 mg/kg)、大黄素中剂量组(每日40 mg/kg)、大黄素低剂量组(每日20 mg/kg),分别干预动物模型。
1.4 动物模型的制备、分组及处理大鼠适应性喂养3 d后,随机选出24只大鼠,雌雄各半,编为对照组。剩下的大鼠进一步随机分为4组,即模型组、大黄素高剂量组(每日80 mg/kg)、大黄素中剂量组(每日40 mg/kg)、大黄素低剂量组(每日20 mg/kg),每组24只大鼠,雌雄各半。对照组和模型组采用羧甲基纤维素钠溶液灌胃,其余组采用不同剂量大黄素溶液灌胃。大黄素干预开始后第5天,除对照组外,其余4组大鼠予0.5%ANIT(50 mg/kg)溶于花生油溶液灌胃建立肝内胆汁淤积模型[8],并分别于ANIT灌胃24、48、72 h后处死各组8只大鼠。处死前,予禁食12 h。处死当天,予1%戊巴比妥钠 50 mg/kg腹腔注射麻醉,摘眼球取血2 mL,3 000 r/min,离心30 min,分离血清,-20℃保存。
1.5 生化检测采用比色法检测TBIL、DBIL、TBA、ALP、GGT、ALT、AST水平,操作步骤按照各化学试剂盒说明书进行。
1.6 组织形态学检测取肝脏组织块,经固定后常规石蜡包埋,4 μm切片,经二甲苯、各级乙醇脱蜡至水,苏木精染色5 min,水洗后盐酸乙醇分化,经水浸透,再行伊红染色,最后进行常规脱水、透明、封片。
1.7 统计学分析采用SPSS 21.0统计软件对数据进行统计学分析,计量资料采用均数±标准差(x±s)表示,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验,P<0.05为差异有统计学意义。
2 结果 2.1 各组大鼠生活状态各组无死亡动物。对照组大鼠有活力,毛发柔顺有光泽,尿色清亮;模型组大鼠缺乏活力,毛发凌乱、失去光泽,活动及进食均减少,尿色深黄;大黄素高、中、低剂量组大鼠活动及进食均较模型组明显改善,尿色较模型组变浅。
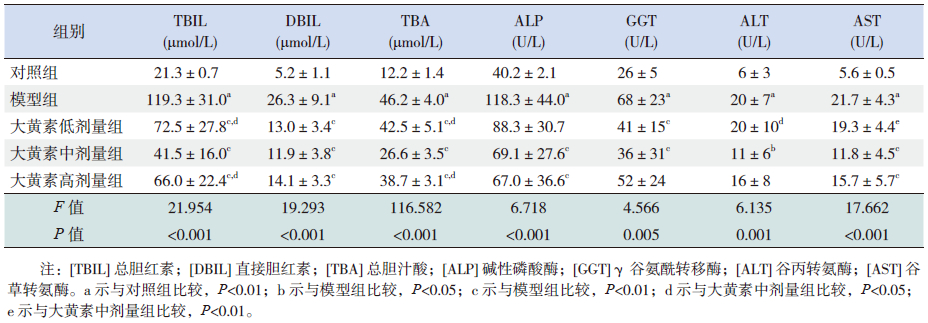
2.2 大黄素对胆汁淤积大鼠造模后24 h生化指标的影响与对照组比较,模型组大鼠血清TBIL、DBIL、TBA、ALP、GGT、ALT、AST水平均显著升高(P<0.01)。与模型组比较,大黄素高、中、低剂量组大鼠血清TBIL、DBIL、TBA水平均有不同程度降低(P<0.05);大黄素低剂量组大鼠血清GGT水平显著降低(P<0.01);大黄素中剂量组大鼠血清ALP、GGT、ALT、AST水平均有不同程度降低(P<0.05);大黄素高剂量组大鼠血清ALP、AST水平显著降低(P<0.01)。与大黄素中剂量组比较,大黄素低剂量组大鼠血清TBIL、TBA、AST、ALT水平有不同程度升高(P<0.05),大黄素高剂量组大鼠血清TBIL、TBA水平明显升高(P<0.01)。见表 1。
| 表 1 大黄素对胆汁淤积大鼠造模后24 h 生化指标的影响 ( x±s,n=8) |
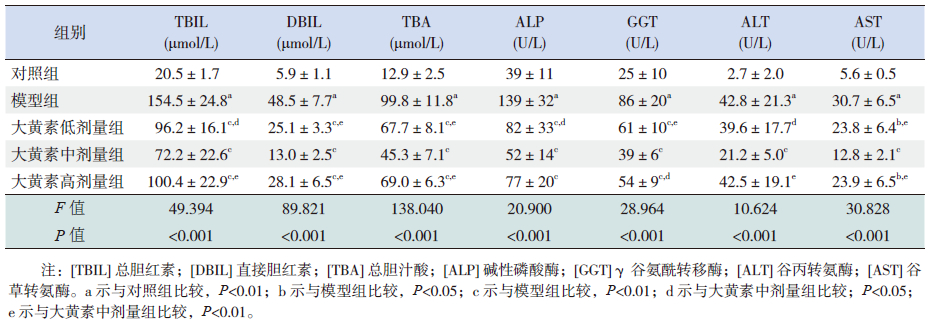
与对照组比较,模型组大鼠血清TBIL、DBIL、TBA、ALP、GGT、ALT、AST水平均明显升高(P<0.01)。与模型组比较,大黄素高、中、低剂量组大鼠血清TBIL、DBIL、TBA、ALP、GGT、AST水平均有不同程度降低(P<0.05),中剂量组大鼠血清ALT水平显著降低(P<0.01)。与大黄素中剂量组比较,大黄素低剂量组大鼠血清TBIL、DBIL、TBA、ALP、GGT、ALT、AST水平均有不同程度升高(P<0.05);大黄素高剂量组大鼠血清TBIL、DBIL、TBA、GGT、ALT、AST水平均有不同程度升高(P<0.05)。见表 2。
| 表 2 大黄素对胆汁淤积大鼠造模后48 h 生化指标的影响 ( x±s,n=8) |
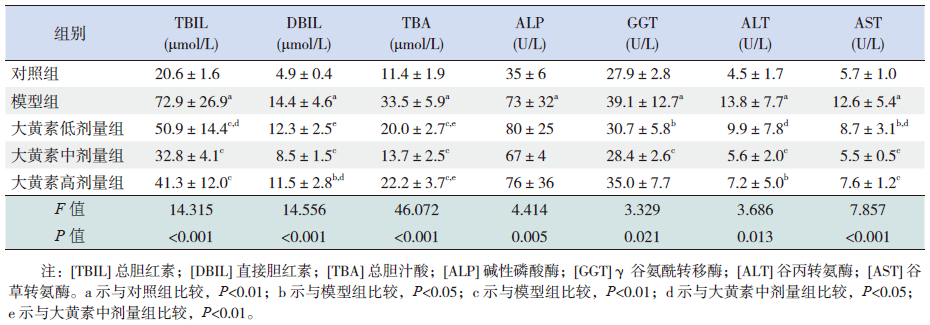
与对照组比较,模型组大鼠血清TBIL、DBIL、TBA、ALP、GGT、ALT、AST水平均明显升高(P<0.01)。与模型组比较,大黄素低剂量组大鼠血清TBIL、TBA、GGT、AST水平有不同程度降低(P<0.05);大黄素中剂量组大鼠血清TBIL、DBIL、TBA、GGT、ALT、AST水平均明显降低(P<0.01);大黄素高剂量组大鼠血清TBIL、DBIL、TBA、ALT、AST水平有不同程度降低(P<0.05)。与大黄素中剂量组比较,大黄素低剂量组大鼠血清TBIL、DBIL、TBA、ALT、AST水平均有不同程度升高(P<0.05);大黄素高剂量组大鼠血清DBIL、TBA水平有不同程度升高(P<0.05)。见表 3。
| 表 3大黄素对胆汁淤积大鼠造模后72 h 生化指标的影响 ( x±s,n=8) |
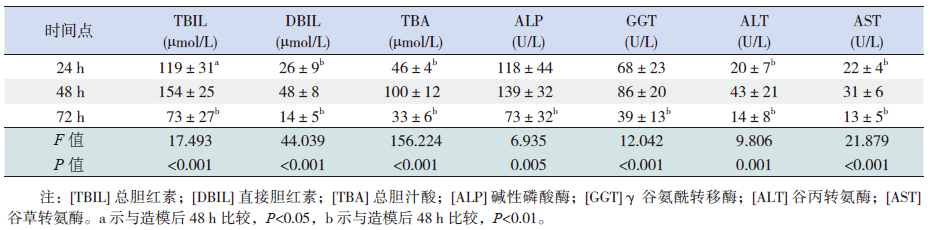
模型组大鼠造模后48 h血清TBIL、DBIL、TBA、ALT、AST水平较造模后24 h均有不同程度升高(P<0.05);血清TBIL、DBIL、TBA、ALP、GGT、ALT、AST水平较造模后72 h均明显升高(P<0.01)。见表 4。
| 表 4 模型组造模后不同时间点生化指标变化比较 ( x±s,n=8) |
不同时间点对照组肝小叶结构完整,可见肝细胞围绕中央静脉索状排列,肝细胞大小较一致。模型组24 h部分区域肝中央静脉缺如,肝小叶结构欠清,肝细胞广泛空泡状变性,并见中性粒细胞浸润;48 h时肝小叶结构异常,似可见假小叶形成,肝细胞肿胀,胞浆疏松,肝细胞核大小不一,核内染色质聚集,核仁粗大浓染,可见多个点状、灶状坏死区,肝脏kupffer细胞增生,较24 h肝细胞病变加重;72 h时见到上述病变减轻,肝小叶结构尚存,但仍可见坏死灶和中性粒细胞浸润。大黄素中剂量组大鼠24 h和72 h肝脏形态与对照组大鼠肝脏形态相近似;造模干预后24、48、72 h,大黄素高剂量、低剂量组大鼠肝组织病理改变均较模型组减轻,中性粒细胞浸润减少。见图 1。
 |
图 1 各组大鼠各时间点肝脏病理学表现(苏木精- 伊红染色,×200) 对照组肝小叶结构完整,肝细胞大小 较一致。模型组24 h 肝小叶结构欠清,肝细胞广泛空泡状变性,并见中性粒细胞浸润(箭头所示);48 h 肝小叶结构异常, 可见多个点状、灶状坏死区(箭头所示);造模72 h 时见到上述病变减轻,但仍可见坏死灶和中性粒细胞浸润(箭头所示)。 大黄素中剂量组大鼠肝脏形态与对照组大鼠肝脏形态相近似;大黄素高剂量、低剂量组肝组织病理改变均较模型组减轻,中 性粒细胞浸润减少(箭头所示)。 |
胆汁淤积是一组严重的症候群,表现为黄疸、浅黄色大便、深色小便、肝细胞功能损害等生化指标异常及肝脏组织病理学改变[12]。胆汁的主要成分是胆汁酸,但疏水性胆汁酸过多会导致皮肤瘙痒,肝细胞的凋亡和坏死,肝脏纤维化或者肝硬化甚至肝功能衰竭[13]。
大黄素是中药大黄的主要活性成份,本课题组前期的研究发现,大黄素能够通过抑制炎性介质,抗氧化,改善肝脏循环,减少损伤信号,控制中性粒细胞浸润来达到缓解淤胆型肝炎肝损伤的作用,能够缓解ANIT诱导的急性胆汁淤积大鼠模型的生化指标[8]。本次研究就不同剂量大黄素预处理对肝内胆汁淤积幼龄大鼠的保护效果做进一步研究,为临床应用大黄素治疗婴幼儿、儿童肝内胆汁淤积提供实验依据。
目前国内外公认的肝内胆汁淤积模型为化学药物ANIT单次给药诱导,剂量为每日45~ 100 mg/kg,通过损伤胆管上皮细胞、胆管阻塞和肝细胞毒性导致肝内胆汁淤积,肝脏损伤主要表现为升高的血清胆红素、胆汁酸、肝酶和肝组织病理损害,在大鼠中,ANIT能够模拟人类的肝内胆汁淤积,为成熟的动物模型[14]。本研究中的实验对象为3周龄离乳后大鼠,该周龄的大鼠模型更接近于婴幼儿及儿童时期的病理生理特点。在实验第5天ANIT单剂量灌胃给药,选取造模后24、48、72 h为观察时间节点,在生化指标的观察上,我们监测大鼠胆汁淤积的相关指标(TBIL、DBIL、TBA、ALP、GGT)及肝细胞损伤的相关指标(ALT、AST)血清水平的变化情况。
24、48、72 h时间点模型组大鼠血清生化指标较对照组明显升高。表明造模后3个时间点 ANIT诱导造成模型组大鼠肝内存在胆汁淤积和肝细胞损害,证明幼龄大鼠肝内胆汁淤积动物模型成功建立。大黄素高、中、低剂量组较模型组的血生化指标均有不同程度的降低,表明大黄素不同剂量均可以改善ANIT诱导的幼龄大鼠肝内胆汁淤积和肝细胞损害。大黄素高、低剂量组较中剂量组血生化指标有不同程度升高,表明中剂量组在改善肝内胆汁淤积和保护肝细胞损伤方面具有优势,其原因考虑高剂量大黄素可能会存在一定的肝脏毒性。
模型组造模后48 h较造模后24 h和72 h大鼠血清生化指标有不同程度升高,说明模型组48 h大鼠无论胆汁淤积程度还是肝细胞损伤的程度都较24 h和72 h明显,代表了造模后48 h时间点肝细胞和胆管受损最严重,72 h后肝脏胆汁淤积和肝细胞损伤的情况都有所好转,与文献[15]报道相一致。可能与ANIT在诱导大鼠肝内胆汁淤积过程中与还原性谷胱甘肽在胆汁中可逆性结合,随着时间的推移,结合的ANIT逐渐解离排泄出来相 关[16]。为以后设立药物干预的关键时间点提供了实验依据。
对照组在24、48、72 h时间点肝小叶结构完整,可见肝细胞围绕中央静脉索状排列,肝细胞大小较一致。模型组24 h部分区域肝中央静脉缺如,肝小叶结构欠清晰,肝细胞呈广泛空泡状变性,并见中性粒细胞浸润;48 h肝小叶结构异常,似可见假小叶形成,肝细胞肿胀,胞浆疏松,肝细胞核大小不一,核内染色质聚集,核仁粗大浓染,可见多个点状、灶状坏死区,肝脏kupffer细胞增生,较24 h肝细胞病变加重;造模72 h 时见到上述病变减轻,肝小叶结构尚存,但仍可见坏死灶和中性粒细胞浸润。大黄素中剂量组大鼠24 h、72 h肝脏形态与对照组大鼠肝脏形态相近似;大黄素高剂量、低剂量组大鼠肝脏形态及肝组织病理改变在造模干预后各时间点均较模型组减轻,中性粒细胞浸润减少。本研究在造模后48 h肝脏病理损害最为严重,72 h病理改变明显减轻,与文献报道相一致[17]。大黄素高、中、低三个剂量组之间干预后比较大黄素中剂量组病理改善效果最好。与前面所描述的胆汁淤积相关生化指标和肝细胞损伤指标在48 h时损伤程度最重,大黄素中剂量干预组改善胆汁淤积和受损肝细胞指标效果最好相一致。
本研究从血清生化及病理观察大黄素预处理对ANIT诱导的肝内胆汁淤积的保护作用。结果发现:ANIT单剂量灌胃给药50 mg/kg成功建立幼龄大鼠肝内胆汁淤积动物模型;大黄素可以有效保护ANIT诱导幼龄大鼠的肝内胆汁淤积,中剂量组效果最好。未来本课题组将进一步研究大黄素改善ANIT诱导的肝内胆汁淤积的分子机制,除了本课题组前期做的炎症反应机制外,大黄素针对胆汁淤积的关键性受体FXR[9]及下游的的相关分子将是本课题组未来研究的重点。
| [1] | Fischler B, Lamireau T. Cholestasis in the newborn and infant[J]. Clin Res Hepatol Gastroenterol, 2014, 38(3):263-267. |
| [2] | 朱启镕, 王建设. 婴儿胆汁淤积症的鉴别诊断思路[J]. 临床肝胆病杂志, 2011, 27(7):679-681, 693. |
| [3] | Diniz G, Tosun Yildirim H, Calkavur S, et al. Can neonatal hepatitis be more fatal than biliary atresia?[J]. Fetal Pediatr Pathol, 2015, 34(3):162-168. |
| [4] | Mousa HS, Lleo A, Invernizzi P, et al. Advances in pharmacotherapy for primary biliary cirrhosis[J]. Expert Opin Pharmacother, 2015, 16(5):633-643. |
| [5] | 郑志想. 25% 硫酸镁联合生大黄治疗急性胆汁淤积性肝炎的临床研究[J]. 中华实验和临床感染病杂志, 2013, 7(1):113-114. |
| [6] | 鄢素琪, 邓玉萍, 汤建桥, 等. 利胆合剂治疗婴儿巨细胞病毒感染胆汁淤积性肝病120例临床观察[J]. 中国中西医结合杂志, 2012, 32(12):1632-1637. |
| [7] | Zhao YL, Wang JB, Zhou GD, et al. Investigations of free anthraquinones from rhubarb against alphanaphthylisothiocyanate-induced cholestatic liver injury in rats[J]. Basic Clin Pharmacol Toxicol, 2009, 104(6):463-469. |
| [8] | Ding Y, Zhao L, Mei H, et al. Exploration of emodin to treat alpha-naphthylisothiocyanate-induced cholestatic hepatitis via anti-inflammatory pathway[J]. Eur J Pharmacol, 2008, 590(1-3):377-386. |
| [9] | 丁艳, 徐芳, 熊小丽, 等. 法尼醇X受体在急性淤胆型肝炎大鼠模型中的表达及大黄素的干预作用[J]. 中国当代儿科杂志, 2014, 16(4):424-429. |
| [10] | 雷湘, 陈刚, 陈科力, 等. 大黄素对小鼠的急性毒性研究[J]. 中国药理与临床, 2008, 24(1):29. |
| [11] | 周方, 许红梅. 大黄素对肝内胆汁淤积大鼠P-gp表达的影响[J]. 中国中药杂志, 2010, 35(7):908-911. |
| [12] | 黄志华, 董琛. 婴儿胆汁淤积性肝病鉴别诊断思路[J]. 中国实用儿科杂志, 2013, 28(4):250-254. |
| [13] | Jonker JW, Liddle C, Downes M. FXR and PXR:potential therapeutic targets in cholestasis[J]. J Steroid Biochem Mol Biol, 2012, 130(3-5):147-158. |
| [14] | Ding L, Zhang B, Zhan C, et al. Danning tablets attenuates α-naphthylisothiocyanate-induced cholestasis by modulating the expression of transporters and metabolic enzymes[J]. BMC Complement Altern Med, 2014, 14:249. |
| [15] | 姚嘉明, 于芳芳, 王小奇, 等. 清热化湿疏肝祛瘀法对急性肝内胆汁淤积大鼠的防治作用[J]. 中华中医药学刊, 2012, 30(10):2251-2253. |
| [16] | Jean PA, Roth RA. Naphthylisothiocyanate disposition in bile and its relationship to liver glutathione and toxicity[J]. Biochem Pharmacol, 1995, 50(9):1469-1474. |
| [17] | 欧巧群, 钱新华, 黄笑群. α-萘异硫氰酸酯诱导幼鼠亚急性肝内胆汁淤积的动态变化[J]. 广州医药, 2014, 45(5):7-10. |
 2016, Vol. 18
2016, Vol. 18