慢性腹泻为一组不同病因引起的以大便次数增多或者性状改变为表现的临床综合征,病程持续2个月以上[1],多伴有蛋白质-能量营养不良、营养物质缺乏、免疫功能紊乱、反复感染,并出现恶性循环,至今仍为重要公共卫生问题。近年营养支持在儿科疾病中的应用日渐被重视,改善了很多儿科疾病的临床结局,但营养支持应用于慢性腹泻的临床研究仍不多。本研究回顾总结了我院近2年来对慢性腹泻患儿采用肠内/肠外营养治疗的情况。
1 资料与方法 1.1 研究对象收集2012年7月至2014年7月在我院住院治疗的慢性腹泻患儿共48例,年龄2.0~190.8个月,中位年龄10.2个月。诊断符合全国高等学校教材《儿科学》第2版慢性腹泻诊断标准[1]。
1.2 研究方法收集48例患儿入院后的临床资料,对25例2013年1月1日以后入院的患儿采用STRONGkids评分系统进行了营养评估[2]:运用世界卫生组织(WHO)Anthro及AnthroPlus软件(版本3.2.2)计算年龄别体重Z评分(weight-for-age z-score,WAZ)、年龄别身高Z评分(height-for-age z-score,HAZ)、身高别体重Z评分(weight-for-height z-score,WHZ)、年龄别体质指数Z评分(BMI-for-age z-score,BAZ)。因儿童体格发育随着年龄而增加,单一的年龄别体重或身高别体重已不能分辨身高及体质指数的关系,故年长儿应用BAZ或HAZ来评价营养状况更为合适[3],WHZ、WAZ则应用于6岁或10岁以内儿童[4]。WHO推荐的营养不良分型分度标准[5]:WAZ<-3为重度体重低下,-3<WAZ<-2为中度体重低下;HAZ<-3为重度生长迟缓,-3<HAZ<-2为中度生长迟缓;WHZ<-3为重度消瘦,-3<WHZ<-2为中度消瘦。
治疗:根据腹泻病因进行治疗,合并细菌感染者予相应抗感染治疗,并合理营养治疗、积极预防脱水、维持电解质平衡和使用微生态制剂及肠道粘膜保护剂。
营养治疗:合并营养不良的27例患儿予以营养治疗。如无肠内营养(enteral nutrition,EN)禁忌、耐受口服喂养的患儿继续经口喂养,根据病因选择相应肠内营养制剂(如氨基酸配方奶粉,深度水解配方奶粉,无乳糖配方奶粉,短肽配方奶粉,中链甘油三酯较高配方奶粉及能量密度较高配方奶粉)强化肠内营养。如果经口喂养不耐受,根据病因选择管饲肠内营养或者肠外营养,若经管饲肠内营养能满足营养要素及能量需求,则逐渐过渡至经口喂养;若不能满足,则给予部分肠外营养(partial parenteral nutrition,PPN),病情好转后逐渐增加肠内营养过渡至经口喂养,如始终不能耐受经口喂养,则带管出院。如患儿存在肠内营养禁忌,则予全肠外营养(total parenteralnutrition,TPN),缓解病因、改善症状后,逐渐施行肠内营养。
分组:根据年龄将48例患儿分为<1岁组(27例)和≥1岁组(21例)。接受营养支持治疗的27例患儿分为EN组(10例,年龄4.4~147.6个月)、PPN+EN组(16例,年龄2.0~190.8个月),TPN组(1例,年龄8.7个月)。
1.3 统计学分析应用SPSS 19.0软件进行处理。计量资料采用均数±标准差或中位数(范围)表示。正态分布资料采用t检验,非正态分布资料采用Wilcoxon秩和检验和Mann-Whitney U检验。计数资料采用χ2检验。P<0.05为差异有统计学意义。
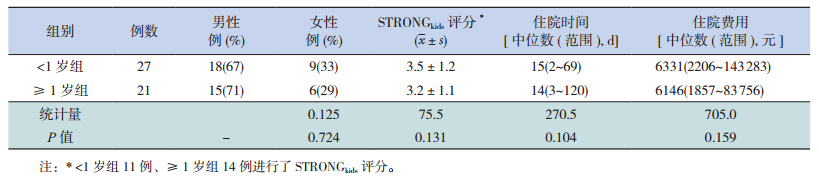
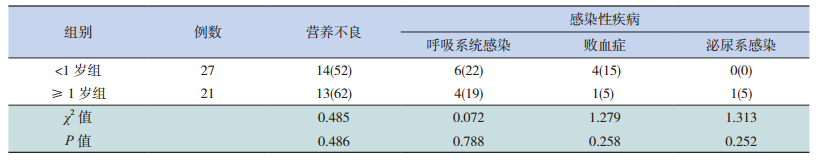
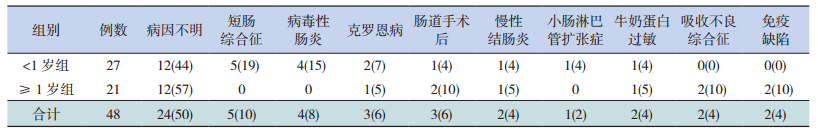
2 结果 2.1 一般资料48例患儿中<1岁组27例(56.2%),中位年龄6.8(2.0~11.2)个月,男女比例2:1;≥1岁组21例,中位年龄29(15~191)个月,男女比例5:2。<1岁和≥1岁两组在性别构成比以及住院时间(15 d vs 14 d)、住院费用(6 331元 vs 6 145元)、合并症发生率(两组营养不良发生率分别为52% vs 62%,呼吸系统感染比例为22% vs 19%,败血症比例为15% vs 5%,泌尿系感染为0% vs 5%)差异无统计学意义(P>0.05);<1岁组11人参与STRONGkids评分,≥1岁组14人参与STRONGkids评分,两组评分差异无统计学意义(P>0.05)。见表 1~2。短肠综合征、病毒性肠炎、肠道手术、吸收不良综合征等为48例患儿的较常见病因,50%(24例)的病例仍病因不明。见表 3。
| 表 1 48例慢性腹泻患儿基本资料 |
| 表 2 48例慢性腹泻患儿合并症分析[例(%)] |
| 表 3 48例慢性腹泻患儿病因分析[例(%)] |
2.2 入院时评估
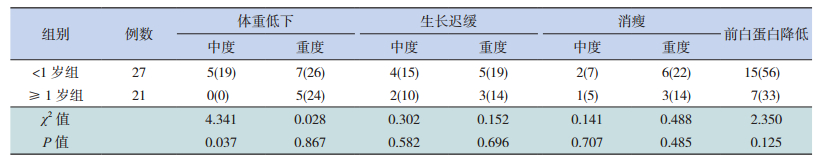
<1岁组入院时体重低下的12例(中度5例、重度7例),生长迟缓9例(中度4例、重度5例),消瘦8例(中度2例、重度6例),前白蛋白降低(<0.15 g/L)15例;≥1岁组,体重低下5例(均为重度),生长迟缓5例(中度2例、重度3例),消瘦4例(中度1例、重度3例),前白蛋白降低7例;两组间仅中度体重低下患儿所占比例的差异有统计学意义(P<0.05)。见表 4。两组间WAZ(-1.7±2.5 vs -1.8±1.5)、WHZ(-1.2±1.9 vs -1.8±1.7)、HAZ(-1.1±2.2 vs -1.2±1.8)、BAZ(-1.5±2.1 vs -1.7±1.4),差异无统计学意义(P>0.05)。所有病例中仅1例小肠淋巴管扩张症患儿出现低蛋白血症。所有患儿的血红蛋白均>90 g/L,<1岁组有6例轻度贫血,≥1岁组有4例轻度贫血。
| 表 4 慢性腹泻患儿入院时营养评定结果[例(%)] |
2.3 肠内/肠外营养治疗
48例患儿中27例合并营养不良者予以营养治疗,分为EN组、TPN组及PPN+EN组。EN组有10例患儿:5例病因不明者口服无乳糖配方或者短肽配方奶粉,1例克罗恩病患儿予高热卡(1 kcal/mL)整蛋白肠内营养制剂口服,1例先天性巨结肠术后患儿口服高热卡短肽配方肠内营养制剂,另3例病因不明患儿给予鼻饲短肽配方奶粉:其中2例出院后继续鼻饲、1例在住院第20天改为经口进食。10例患儿经过2~15 d(中位数3 d)症状均好转,仅1例在肠内营养过程中出现不良反应:表现为不愿经口进食、腹泻加剧。
PPN+EN组16例,病因为短肠综合征(5例)的患儿予氨基酸配方或短肽配方奶,其中3例为鼻饲持续泵注;病因为克罗恩病(2例)的患儿予氨基酸配方奶,其中1例为鼻饲;病因为吸收不良综合征(2例)的患儿给予氨基酸配方奶;其余患儿根据肠道耐受情况选择短肽配方或整蛋白配方奶。肠内营养不足部分予部分肠外营养补充,12例使用外周静脉置入的中心静脉导管(PICC)或中心静脉置管、4例选用外周静脉。PPN+EN组相关不良反应中:5例导管相关感染、1例肝功能异常;8例患儿出现腹胀/腹泻。PPN+EN组12例症状好转,好转中位时间为15 d(3~60 d),改经口进食的中位时间为46 d(11~64 d);4例患儿未能改善症状而自动出院。
予以TPN治疗的1例为小肠淋巴管扩张症患儿,确诊后先予禁食,入院第5天开始TPN(每日61.8 kcal/kg)治疗,第15天开始予以深度水解、中链甘油三酯含量高的奶方并结合肠外营养,第25天改为完全经口喂养,住院第7天腹泻好转,未观察到不良反应及并发症。
随访至今,27例接受营养治疗的患者中,病因为短肠综合征的5例患儿均已改至普通饮食,其中4例营养状况恢复正常、1例仍存在轻中度营养不良。1例小肠淋巴管扩张患儿继续肠内营养治疗,症状及营养状况好转。病因为克罗恩病的患儿,2例改为普通饮食和定期肠内营养,另1例失访。2例吸收不良综合征患儿出院后失访。1例免疫缺陷病患儿随访过程中仍有腹泻症状反复,营养状况为轻~中度营养不良。1例肠道手术后患儿已改为普通饮食,营养状况恢复正常范围。2例病因不明患儿症状未好转,出院后失访。其余患儿在症状及营养状况改善后逐渐失访。研究中无死亡病例。
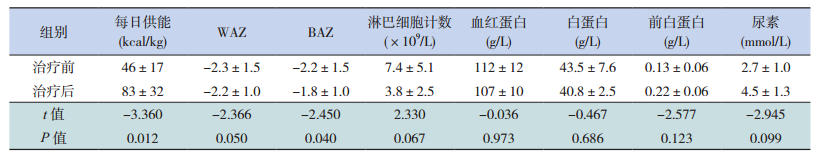
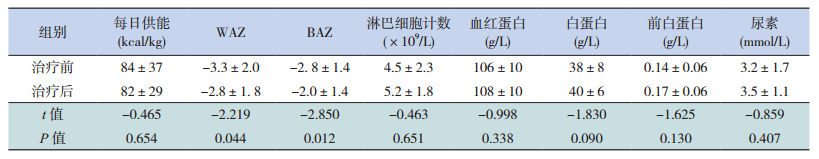
2.4 营养支持治疗效果评定治疗后EN组能量供给增加、BAZ明显增高(P<0.05);而WAZ、外周血淋巴细胞计数、血红蛋白、白蛋白、前白蛋白和尿素较治疗前差异无统计学意义(P>0.05)。PPN+EN组患儿治疗后WAZ、BAZ增加(P<0.05);而能量供给、外周血淋巴细胞计数、血红蛋白、白蛋白、前白蛋白和尿素较治疗前差异无统计学意义(P>0.05)。见表 5~6。
| 表 5 EN组疗效评定(n=10, x±s) |
| 表 6 PPN+EN组疗效评定(n=16, x±s) |
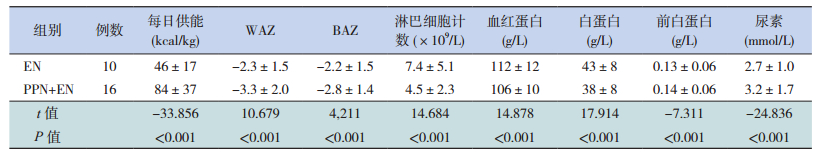
EN组与PPN+EN组患儿的营养监测指标在治疗前已存在异质性(表 7),因此未进一步比较两组患儿的治疗效果。TPN组仅1例,也未与其他组进行疗效比较。
| 表 7 EN组与PPN+EN组治疗前营养监测指标比较(x±s) |
3 讨论
小儿腹泻病目前依然是全球关注的公共卫生问题,虽然治疗手段改进,但是每年仍有80万儿童死于腹泻病[6]。慢性腹泻病因复杂,感染、过敏、免疫缺陷、药物、先天畸形、营养不良等为常见病因,而且它还可继发不同程度营养不良、免疫功能紊乱,常常互为因果、形成恶性循环[1]。
本研究中<1岁组慢性腹泻的病因以短肠综合征及病毒感染较多见,短肠综合征多与该年龄段早期肠道相关手术有关,本研究5例短肠综合征患儿均因不同消化道疾病在新生儿期接受过肠道手术;而病毒感染与婴儿免疫功能尚未健全相关;≥1岁组慢性腹泻较为多见的病因有肠道手术、免疫缺陷、肠吸收不良综合征等。Borschel等[7]研究提示,<1岁组慢性腹泻常见病因依次为食物过敏、嗜酸粒细胞性胃肠炎、病毒感染、短肠综合征、配方奶不耐受,儿童组则依次为吸收不良、短肠综合征、嗜酸粒细胞性胃肠炎、食物过敏等。国内对于慢性腹泻病因尚缺乏严谨的前瞻性队列研究。王玉环等报道[8],感染性腹泻、炎症性肠病、非特异性结肠炎为较多见的慢性腹泻病因,但该研究并未对患儿进行年龄分层统计,未能体现不同年龄儿童慢性腹泻的病因特点。与国外研究不同,本研究中食物过敏并非常见的慢性腹泻成因,可能与患者的环境暴露不同有关。有文献报道[9],发展中国家最常见的慢性腹泻病因为肠道感染;而在发达国家,感染因素导致慢性腹泻的比例在下降,自身免疫性肠病或以炎症为基础的疾病导致的慢性腹泻比例在升高。慢性腹泻病因不明的仍占较高比例,本研究显示分别占<1岁组的44%和≥1岁组的57%,需进一步探索腹泻的疾病成因,建立慢性腹泻的诊断及鉴别诊断体系。慢性腹泻的初步诊断及评估的建立包括以下3步[9]:病史采集(包括病程、大便次数及性状、其他相关症状以及饮食情况);体格检查;实验室检查(炎症相关指标、电解质、血常规、肝功能、血脂分析、粪便病原学等)。而作为儿童消化专科医师,必要时行消化内镜及粘膜活检,可更直观地观察消化道及粘膜的病变。本研究48例慢性腹泻患儿33%合并感染性疾病,56%合并不同程度的营养不良。因此,慢性腹泻病因复杂,常常和感染、营养不良互为因果,导致住院时间长、住院费用高,本研究的中位住院时间均长达半月左右、中位住院费用均在数千元,慢性腹泻成为亟待解决的临床问题。
营养支持在慢性腹泻治疗中的作用日渐被关注。肠内营养符合消化生理过程,可提供必要的肠内刺激、保护肠道屏障功能、改善负氮平衡[10],而且安全性好、并发症少、费用低[11-14]。本研究中没有肠内营养禁忌或肠内喂养不耐受的,均首选肠内营养,EN组仅1例出现不愿经口进食、腹泻加剧的不良反应;PPN+EN组5例出现导管相关感染、1例出现肝功能异常等不良反应。EN组治疗后的每日能量供给和BAZ明显增高,PPN+EN组的WAZ、BAZ明显增加,营养评估较前改善;其他营养监测指标,如外周血淋巴细胞计数、血红蛋白、白蛋白、前白蛋白等因为半衰期较长,治疗前后变化不大,这与张波等人[15]的研究类似。而对于接受营养治疗患者的远期效果和副作用,尚需更大样本的长期随访及病例对照研究。
综上,对于慢性腹泻患儿,需尽早明确病因,重视病程中营养评估及营养干预。肠内营养及肠外营养均可安全、有效地改善患儿营养状态。
| [1] | 孙梅. 婴幼儿腹泻[M]//薛辛东, 杜立中, 毛萌. 儿科学. 第2版. 北京: 人民卫生出版社, 2010: 250-253. |
| [2] | Hulst JM, Zwart H, Hop WC, et al. Dutch national survey to test the STRONGkids nutritional risk screening tool in hospitalized children[J]. Clinical Nutrition,2010, 29 (1) :106–111 . |
| [3] | de Onis M, Garza C, Onyango AW, et al. WHO growth standards for infants and young children[J]. Arch Pediatr,2009, 16 (1) :47–53 . |
| [4] | de Onis M, Onyango AW, Borghi E, et al. Development of a WHO growth reference for school-aged children and adolescents[J]. Bull World Health Organ,2007, 85 (9) :660–667 . |
| [5] | de Onis M, Blössner M. WHO global database on child growth and malnutrition. World Health Organization[DB/OL].(1997)[Mar.1st, 2015]. http://www.who.int/nutgrowthdb/database/en. |
| [6] | Liu L, Johnson HL, Cousens S, et al. Global, regional, and national causes of child mortality: an updated systematic analysis for 2010 with time trends since 2000[J]. Lancet,2012, 379 (9832) :2151–2161 . |
| [7] | Borschel MW, Antonson DL, Murray ND, et al. Two single group, prospective, baseline-controlled feeding studies in infants and children with chronic diarrhea fed a hypoallergenic free amino acid-based formula[J]. BMC Pediatr,2014, 14 :136. |
| [8] | 王玉环, 黄瑛. 儿童慢性腹泻61例临床分析[J]. 中华妇幼临床医学杂志(电子版),2009,5 (4) :356–361. |
| [9] | Lee KS, Kang DS, Yu J, et al. How to do in persistent diarrhea of children?: concepts and treatments of chronic diarrhea[J]. Pediatr Gastroenterol Hepatol Nutr,2012, 15 (4) :229–236 . |
| [10] | 黄永坤, 杨武. 小儿慢性腹泻病的营养治疗[J]. 实用儿科临床杂志,2006,21 (19) :1288–1290. |
| [11] | Cangelosi MJ, Auerbach HR, Cohen JT. A clinical and economic evaluation of enteral nutrition[J]. Curr Med Res Opin,2011, 27 (2) :413–422 . |
| [12] | McClave SA, Martindale RG, Rice TW, et al. Feeding the critically ill patient[J]. Crit Care Med,2014, 42 (12) :2600–2610 . |
| [13] | Gosselin KB, Duggan C. Enteral nutrition in the management of pediatric intestinal failure[J]. J Pediatr,2014, 165 (6) :1085–1090 . |
| [14] | Brantley SL, Russell MK, Mogensen KM, et al. American Society for Parenteral and Enteral Nutrition and Academy of Nutrition and Dietetics: Revised 2014 Standards of Practice and Standards of Professional Performance for Registered Dietitian Nutritionists (Competent, Proficient, and Expert) in Nutrition Support[J]. Nutr Clin Pract,2014, 29 (6) :792–828 . |
| [15] | 张波, 张雪. 小儿慢性腹泻的营养状况及肠内营养治疗探讨[J]. 现代医药卫生,2011,27 (11) :1628–1629. |
 2016, Vol. 18
2016, Vol. 18