国外报道 1岁以内婴儿牛奶蛋白过敏(cow'smilk protein allergy)发生率为 2.0%~7.5% [1],目前国内尚无确切统计数据。婴儿牛奶蛋白过敏主要表现为皮肤、消化道及呼吸道症状,但因症状缺乏特异性易误诊,凭临床经验诊断的牛奶蛋白过敏高于实际牛奶蛋白过敏的确诊率,导致患儿接受了不必要的饮食回避,而氨基酸配方或深度水解配方的欠佳的口感使患儿每日的摄入总量减少,一定程度上影响了患儿的生长发育,也增加了患儿的家庭经济负担。20世纪中期 Graham等 [2]及 Mytilineou等 [3]报道了食物激发试验并应用于临床研究,其有效性及安全性得到了大量实践证明。我国开展食物激发试验相对滞后,一方面临床医生对其风险过度担忧,另一方面,短缺的医疗资源难以允许患儿住院行口服激发试验。国内较少关于牛奶蛋白激发试验相关的临床研究报道。本研究对 2015年 1~12月在我院儿科住院的 16例临床疑似牛奶蛋白过敏的患儿进行了牛奶蛋白口服激发试验,报道如下。
1 资料与方法 1.1 研究对象2015年 1~12月在我院住院临床疑似牛奶蛋白过敏的婴儿 16例,其中男 11例,女 5例,年龄 2~11个月。表现为湿疹 12例(75%),血便 6例(38%),腹泻 5例(31%),呕吐 2例(12%),营养不良 2例(12%),反复咳喘 2例(12%),拒食 1例(6%),排便次数减少 1例(6%)。
入选标准:根据病史、体查及实验室检查等怀疑牛奶蛋白过敏,年龄 1~12个月,回避饮食(母乳喂养的继续母乳喂养,母亲回避牛奶、鸡蛋、海鲜及原已明确过敏的食物;配方奶喂养的选用游离氨基酸配方或深度水解配方)4周,症状大部分改善或消失,同时停用抗过敏药物、全身用激素、哮喘药至少 1周。
排除标准:患各种急性呼吸道、消化道等感染性疾病、先天性疾病及免疫缺陷性疾病。以下情况不进行口服激发试验:皮肤点刺试验强阳性、牛奶蛋白特异性 IgE(sIgE)>95%阳性预测值、急慢性疾病、严重皮疹、中重度营养不良、先天性疾病及遗传代谢性疾病。
1.2 激发试验前的准备患儿入院后建立静脉通路,放置留置针,完善激发前血常规检查及牛奶蛋白 sIgE检测。询问病史并对患儿进行详细全面的体格检查,充分告之患儿家属激发过程中可能出现的情况及风险,签署知情同意书。准备肾上腺素(1:1 000)1支、心电血氧监护及心肺复苏装置。重度过敏患儿选择深度水解配方,轻-中度过敏患儿选择无乳糖配方或普通配方进行激发。
1.3 激发试验的步骤参照 2012年欧洲儿科胃肠病与肝病学会操作指南 [4],婴儿最后一次进食后 2 h开始,取 1滴婴儿配方乳滴于患儿的口唇,观察皮肤等反应。如在 15 min后无任何反应,开始进行配方乳的喂养,每 20 min增加一次配方乳的喂养量,从 1 mL开始,依次为 3 mL、10 mL、30 mL、100 mL(或一餐最大进食量)(共 5次)。观察生命体征、皮肤、呼吸道、消化道等症状,给予最大喂养量后继续观察 2 h。试验中一旦出现相关临床症状,立即停止试验,根据不同的症状对症处理。2 h后检测血常规、C反应蛋白。对没有发生过敏反应的患儿可出院继续随访观察,随后 2周每日至少进食试验配方 250 mL,不添加其他新食物,家长记录饮食日记,并向医生汇报任何迟发反应。对发生过敏反应的患儿,立即停止配方乳喂养,改氨基酸配方或深度水解配方继续喂养。
1.4 激发试验结果的判定根据 2010年美国国立过敏及感染性疾病研究所食物过敏指南 [5],确诊食物过敏的金标准是食物激发试验。患儿在牛奶蛋白激发 2周观察期内出现原症状再现,包括皮疹、呕吐、腹泻、血便、哭闹不安、拒奶等,即判定为口服激发试验阳性,确诊牛奶蛋白过敏;2周内未出现上述症状者,即判定为口服激发试验阴性,排除牛奶蛋白过敏,继续给予试验配方喂养。
1.5 统计学分析采用 STATA 14.0软件对数据进行分析,计数资料用例数和百分率(%)表示,两组间比较采用 Fisher确切概率法。计量资料用均数 ±标准差(x±s)表示,两组间比较采用独立样本 t检验;激发前后细胞计数比较采用重复测量资料方差分析。P<0.05表示差异有统计学意义。
2 结果 2.1 临床表现16例患儿中口服激发试验阳性 11例(69%),其中发生速发型过敏反应 6例,出现时间为进食100 mL配方奶后 1 h,6例均表现为皮疹,30 min后自行消退,1例同时出现腹泻,粪便隐血试验(+),次日症状消失,均未给予特殊用药;迟发型过敏反应 5例,其中 2例激发第 1天出现血便,1例激发第 14天出现血便,1例激发第 1天出现腹泻,1例激发第 8天颜面及全身出现荨麻疹,停用试验配方后症状全部消失。11例激发试验阳性病例中,2例选用深度水解配方激发,其中 1例激发阳性,1例激发阴性,后者 2周后再次用部分水解配方激发,试验呈阳性。
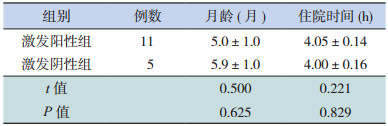
2.2 激发阳性组与阴性组月龄及住院时间的比较16例患儿的平均月龄为 5.3±2.8月,平均住院时间为 4.0±0.4 h,其中激发阳性组与阴性组月龄及住院时间比较差异均无统计学意义(P>0.05),见表 1。
| 表 1 两组患儿月龄及住院时间的比较(x±s) |
2.3 血清牛奶 sIgE检测结果与口服激发试验结果的关系
16例患儿中,sIgE阳性 9例,sIgE阴性 6例,1例拒绝抽血检查。激发阳性组中 sIgE阳性 7例,激发阴性组中 sIgE阳性 2例,Fisher确切概率法检验显示,两组 sIgE阳性率比较差异无统计学意义(P=0.329)。
2.4 激发试验前后外周血血常规结果的比较重复测量资料方差分析显示,激发试验前或激发试验后阳性组与阴性组的外周血白细胞、中性粒细胞及嗜酸性粒细胞(EOS)计数差异均无统计学意义(均 P=0.6527、0.6678、0.6926)。两组激发前后的外周血白细胞、中性粒细胞及 EOS计数差异均无统计学意义(分别 P=0.0746、0.6872、0.6469)。
3 讨论由于牛奶蛋白过敏的发病机制尚不明确,其介导的机制各异,外周血 sIgE检测结果的临床意义有助于确定 IgE介导的食物过敏原,并不能诊断食物过敏 [6],对非 IgE介导的食物过敏无预测作用。本研究中激发试验阳性组与阴性组血清牛奶蛋白sIgE阳性率无明显差异,说明不能单凭血清 sIgE的结果来判断是否存在牛奶蛋白过敏。
非 IgE介导牛奶蛋白过敏进一步分型可分为牛奶蛋白诱导的小肠结肠炎综合征、牛奶蛋白诱导的直肠结肠炎及牛奶蛋白诱导的肠病,诸多学者报道小肠结肠炎综合征可出现外周血白细胞增高,可能与炎症前因子和趋化因子有关 [7]。本研究显示,激发阳性组和阴性组激发后外周血白细胞、中性粒细胞计数与激发前比较无明显差异,可能与本研究未对牛奶蛋白过敏进一步分型、研究中无小肠结肠炎综合征表现患儿以及激发后的血常规检验在激发后 2 h进行有关。激发阳性组和阴性组激发后外周血 EOS计数与激发前比较无明显差异,临床中约 20%患儿 EOS正常或就诊时外周血EOS尚未增高,胃肠组织可能已有嗜酸细胞浸润出现临床症状 [6],因此,不能单以血清 EOS的变化来诊断牛奶蛋白过敏。目前双盲安慰剂激发试验是诊断牛奶蛋白过敏的金标准,但临床中该试验耗时耗力 [4],婴儿受主观情绪影响小,故认为开放性口服激发试验可用于婴儿牛奶蛋白过敏的诊断 [5]。
本研究 16例临床疑似牛奶蛋白过敏的患儿,经口服激发试验确诊牛奶蛋白过敏 11例(69%),与唐鲁静等 [8]报道的口服激发试验确诊率相当,远低于临床诊断率,说明口服激发试验对牛奶蛋白过敏诊断有重要意义。婴儿由于认知度低,受主观因素的影响小,结果可信度高,只有当研究对象年龄增大或对口服激发试验结果高度怀疑时,方考虑行双盲安慰剂激发试验。口服激发试验试验配方的选择并非唯一,疑似合并乳糖不耐受的可选用无乳糖配方激发,对可能出现严重过敏反应者可选用深度水解配方激发。本研究中有 1例患儿腹泻伴严重湿疹,血清 EOS高达 28.4%,予氨基酸配方喂养 1个月后首先予深度水解配方激发,激发试验阴性。2周后予部分水解配方激发,患儿原症状再现,口服激发试验阳性,确诊牛奶蛋白过敏。因此,临床上对疑似严重牛奶蛋白过敏患儿可采用深度水解配方奶粉激发,避免不必要的严重过敏反应。本组病例中有 1例口服激发试验第 14天出现血便,明显长于唐鲁静等 [10]报道的 1周时间,与非 IgE介导的迟发反应缓慢有关系,因此,建议激发试验的观察随访期应严格执行至激发后 2周。
口服激发试验是诊断牛奶蛋白过敏的简单、有效、安全的方法,但应注意以下几点:(1)充分告之患儿家属口服激发试验的重要性,若激发试验阴性,可以排除牛奶蛋白过敏,不必承受较重的经济负担,也不必让孩子长时间回避牛乳及添加了牛乳的食品;若激发试验阳性,明确患儿诊断牛奶蛋白过敏,有助于家人更好地配合医生对患儿进行 3~6个月甚至更长时间的饮食回避。(2)对需进行口服激发试验的患儿进行严格筛选,对曾经出现牛奶蛋白诱发的过敏性休克、有口服激发试验阳性的家族史、皮肤点刺试验强阳性、sIgE>95%阳性预测值、急慢性疾病、严重皮疹、中重度营养不良、先天性疾病及遗传代谢性疾病者不行口服激发试验。(3)注意激发时配方奶粉的选择,对于疑似严重牛奶蛋白过敏患儿,可选择深度水解配方激发,结果阴性者在激发结束后再次返院予部分水解配方甚至整蛋白配方激发;合并乳糖不耐受,可选用无乳糖配方奶粉激发。(4)患儿需在留院观察或住院条件下进行激发试验,本组病例的平均住院时间为 4.0±0.4 h,既不会因住院时间过长而占用紧缺的医疗资源,也不会增加院内感染机会。(5)口服激发试验的观察随访期应严格执行至激发后 2周。
临床口服激发试验的应用,使原尚未明确诊断牛奶蛋白过敏的患儿得到进一步的确诊,既减轻了非牛奶蛋白过敏患儿由于误诊带来的家庭经济负担,又提高了确诊牛奶蛋白过敏婴儿家庭的依从性,平均住院时间短,操作简便、安全性好,值得在临床中推广应用。
| [1] | Sampson HA. Food allergy-accurately identifying clinical reactivity[J]. Allergy,2005, 60 (Suppl 79) :19–24 . |
| [2] | Graham DT, Wolf S, Wolff HG, et al. Changes in tissue sensitivity associated with varying life situations and emotions; their relevance to allergy[J]. J Allergy,1950, 21 (6) :478–486 . |
| [3] | Mytilineou C, Black IB. Regeneration of sympathetic neurons: effect of decentralization[J]. Brain Res,1976, 109 (2) :382–386 . |
| [4] | Koletzko S, Niggemann B, Arato A, et al. Diagnostic approach and management of cow's-milk protein allergy in infants and children: ESPGHAN GI Committee practical guidelines[J]. J Pediatr Gastroenterol Nutr,2012, 55 (2) :221–229 . |
| [5] | NIAID-Sponsored Expert Panel, Boyce JA, Assa'ad A, et al. Guidelines for the diagnosis and management of food allergy in the United States: report of the NIAID-sponsored expert panel[J]. J Allergy Clin Immunol,2010, 126 (6 Suppl) :S1–S58 . |
| [6] | Kim JY, Choi YO, Ji GE. Effect of oral probiotics (Bifidobacterium lactis AD011 and Lactobacillus acidophilus AD031) administration on ovalbumin-induced food allergy mouse model[J]. J Microbiol Biotechnol,2008, 18 (8) :1393–1400 . |
| [7] | Caminiti L, Salzano G, Crisafulli G, et al. Food protein induced enterocolitis syndrome caused by rice beverage[J]. Ital J Pediatr,2013, 39 :31. |
| [8] | 唐鲁静, 赵泓, 陈洁. 牛奶蛋白激发试验在消化道牛奶蛋白过敏症中的临床意义[J]. 中华儿科杂志,2015,53 (4) :285–289. |
 2016, Vol. 18
2016, Vol. 18