2. 四川大学华西第二医院循证药学中心, 四川 成都 610041 ;
3. 出生缺陷与相关妇儿疾病教育部重点实验室, 四川 成都 610041
癫癎是由多种原因引起的脑部慢性疾病,主要发病机制为脑内神经元群反复发作性过渡放电,引起突发性、暂时性脑功能失常[1]。儿童是癫癎的高发人群,其发病率约为成人的10~15倍,约60%的癫癎起病于儿童期[2],我国18岁以下癫癎患儿占75%~80%[3]。癫癎治疗的首选方案为抗癫癎药物(Antiepileptic drugs,AEDs)的单药使用,无效者方考虑多药联合治疗[4-5]。相较于丙戊酸钠、卡马西平等传统AEDs,拉莫三嗪,托吡酯,奥卡西平等新型AEDs具有抗癎谱广、不良反应少、耐受性和安全性好等优点[6],为临床治疗儿童癫癎提供了更多的选择。
拉莫三嗪主要作用机制为抑制兴奋性电压依赖性钠通道,稳定神经细胞膜和减少兴奋性氨基酸-谷氨酸释放[6-7],适用于简单或复杂部分性发作、原发性或继发性全身强直-阵挛发作的单药治疗[8],具有口服生物利用度高,半衰期较长,肝肾功能影响小等特点[9],国内外多项研究均提示其单药治疗儿童癫癎具有较好疗效,不良反应发生率低,对患儿生活质量影响较小[10],但各研究间设计和实施存在差异,样本量较小,其是否优于传统AEDs尚无统一结论。本研究运用系统评价方法对拉莫三嗪单药治疗儿童癫癎的有效性和安全性进行评价,为其进一步的儿科临床应用和将来的临床研究提供依据。
1 资料与方法 1.1 检索策略计算机检索PubMed、Cochrane图书馆、维普数据库(VIP)、中国期刊全文数据库(CNKI)、中国生物医学文献数据库(CBM)、万方数据库,检索时间均从建库至2015年6月。英文检索词包括“epilepsy、epilepsia、seizure、Epileptic、Lamotrigine、Lamictal、Child、Infant、Paediatr”等,中文检索词“包括癫癎、发作、拉莫三嗪、利必通、儿童、小儿、青少年、婴儿、幼儿”等。追踪检索相关参考文献,手检相关杂志、摘要和会议记录,查阅各种会议记录、会议论文集、学位论文等。
1.2 文献纳入和排除标准纳入标准:拉莫三嗪单药治疗儿童癫癎的随机对照试验(randomized controlled trail,RCT),语言限定为中文和英文。研究对象为0~20岁癫癎患儿,性别、人种不限。癫癎及类型的诊断参照国际抗癫癎联盟(ILAE)制定的标准。分为试验组(拉莫三嗪单药治疗)和对照组(安慰剂或其他AEDs单药或添加治疗)。
排除标准:①未设立对照组的文献;②缺乏判效指标和数据的文献;③重复发表的文献;④研究数据不全,联系作者也无法获得有效数据者。
1.3 观察指标癫癎发作完全控制率(治疗期间不再发作的比例)、治疗期间退出率、不良反应。
1.4 文献筛选、质量评价与数据提取两名研究者按照纳入排除标准独立筛选文献、提取资料并交叉核对。纳入研究的方法学质量由两名研究者独立采用Cochrane系统评价员手册5.1.0[11]推荐的偏倚风险评估标准,对纳入文献的随机序列生成、分配隐藏、受试者和研究者施盲、结果施盲、数据完整性、选择性报告结果和其它偏倚等7个方面进行评价。若研究满足以上6~7条质量评价标准,则存在偏倚的可能性很小(A级),若满足2~5条以上标准为部分满足,存在偏倚的可能为中等(B级),若仅满足1条标准或完全不满足,则存在偏倚的可能很大(C级)。分歧经讨论或由第三位研究者协助解决。
1.5 统计学分析采用RevMan 5.2软件进行Meta分析。使用卡方检验及I2进行各研究间的异质性检验。若P≥0.10,则异质性无统计学意义,采用固定效应模型。若P<0.1或I2≥50%,存在统计学异质性,采用随机效应模型。计量资料采用加权均数差值(WMD)作为疗效分析统计量,计数资料采用相对危险度(relative risk,RR)作为疗效分析统计量,均以95%置信区间(CI)表示,P<0.05为差异有统计学意义。不良反应的严重程度按照美国卫生部和癌症协会的不良反应分级标准(CTCAE)[12]分为5级。采用漏斗图和 STATA12.0软件进行Egger's 检验评估纳入研究是否存在潜在的发表偏倚。
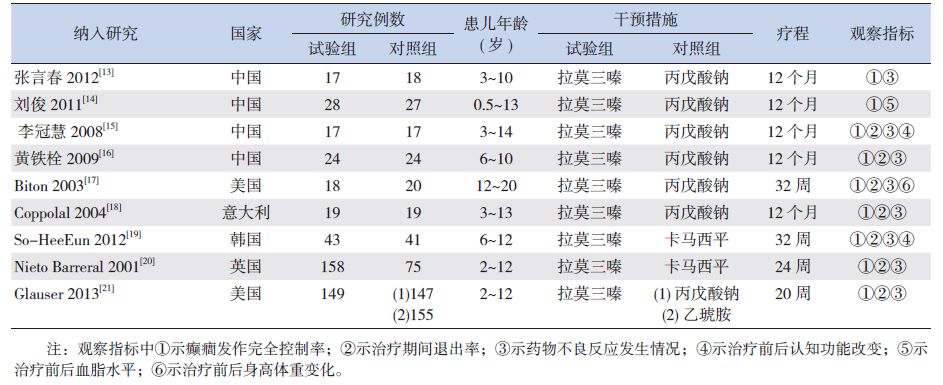
2 结果 2.1 基本情况初检获得文献1 541篇,按照纳入与排除标准筛选后最终纳入9篇[13-20-21]文献,均为RCT研究,共纳入患儿1 016例(试验组473例,对照组543例),年龄为6个月~20岁。9项研究中,6项对照组干预措施为丙戊酸钠[13-18],2项为卡马西平[19-20],
| 表 1 纳入研究的基本情况 |
2.2 质量评价
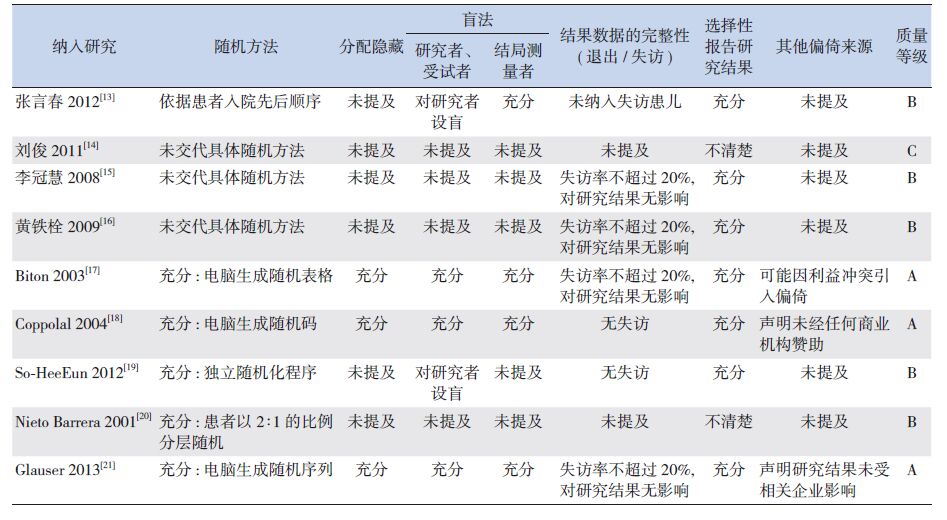
9项研究均为随机分组,4项研究[17-21]报告了采用的随机方法;3项研究[17-18, 21]描述了分配隐藏方法;3项研究为[17-18, 21]为双盲试验,2项[13, 19]为对研究者施盲;6项研究[15-19, 21]报道了失访和退出情况;所有研究均无法获得预先制定的研究计划,但7项研究[13, 15-21]报告了3个及以上的主要判效指标,选择性报告结果的可能性较小。3项研究[17-18, 21]对企业资助信息进行了说明。见表 2。
| 表 2 纳入研究的方法学质量评价 |
2.3 疗效分析
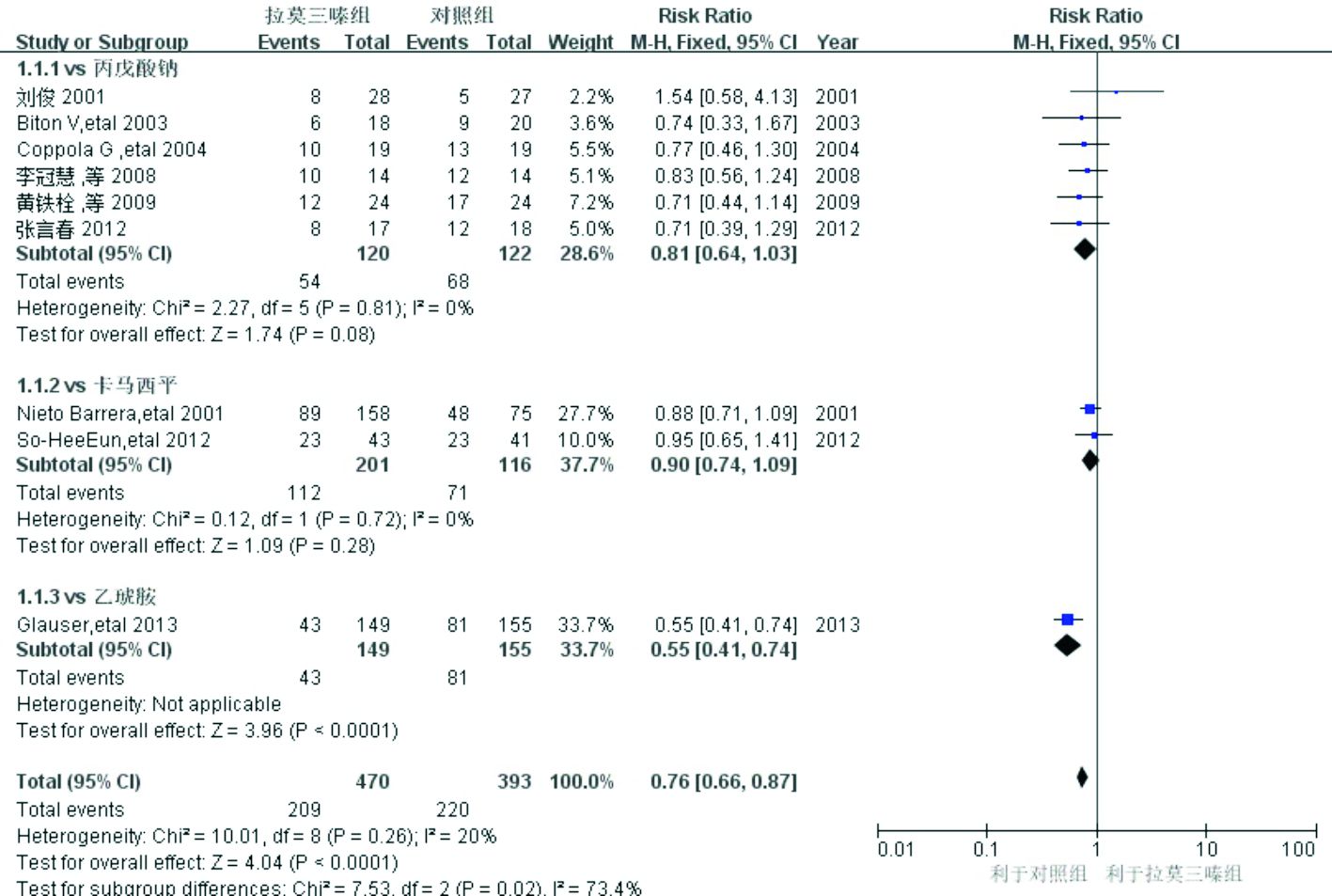
所有研究均报告了癫癎发作完全控制的情况。因对照组干预措施不尽相同,存在临床异质性而无法合并,因此按照对照组干预措施不同进行分析:①拉莫三嗪vs丙戊酸钠:7项研究[13-18, 21]对比了拉莫三嗪和丙戊酸钠单药的癫癎发作完全控制率,其中Glauser等[21]的研究为同时以丙戊酸钠和乙琥胺作为对照,除去该研究进行敏感性分析,异质性检验结果显示无统计学异质性(P=0.81,I2=0%),采用固定效应模型。Meta分析结果显示两组差异无统计学意义(RR=0.81,95%CI:0.64~1.03,P=0.08),提示尚不能认为拉莫三嗪癫癎发作完全控制率低于丙戊酸钠;②拉莫三嗪vs卡马西平:2项研究[19-20]对比了拉莫三嗪和卡马西平的效果,异质性检验结果显示无统计学异质性(P=0.72,I2=0%),采用固定效应模型。结果显示两组差异无统计学意义(RR=0.90,95%CI:0.74~1.09,P=028),提示尚不能认为拉莫三嗪癫癎发作完全控制率低于卡马西平;③拉莫三嗪vs乙琥胺:Glauser等[21]的研究报告了对比乙琥胺的癫癎发作完全控制率,分别为29%和58%,两组差异有统计学意义(χ2检验,P<0.05),提示拉莫三嗪癫癎发作完全控制率低于乙琥胺组。见图 1。
|
图 1 拉莫三嗪组和对照组癫癎发作完全控制率比较的Meta分析 |
2.4 治疗期间退出率
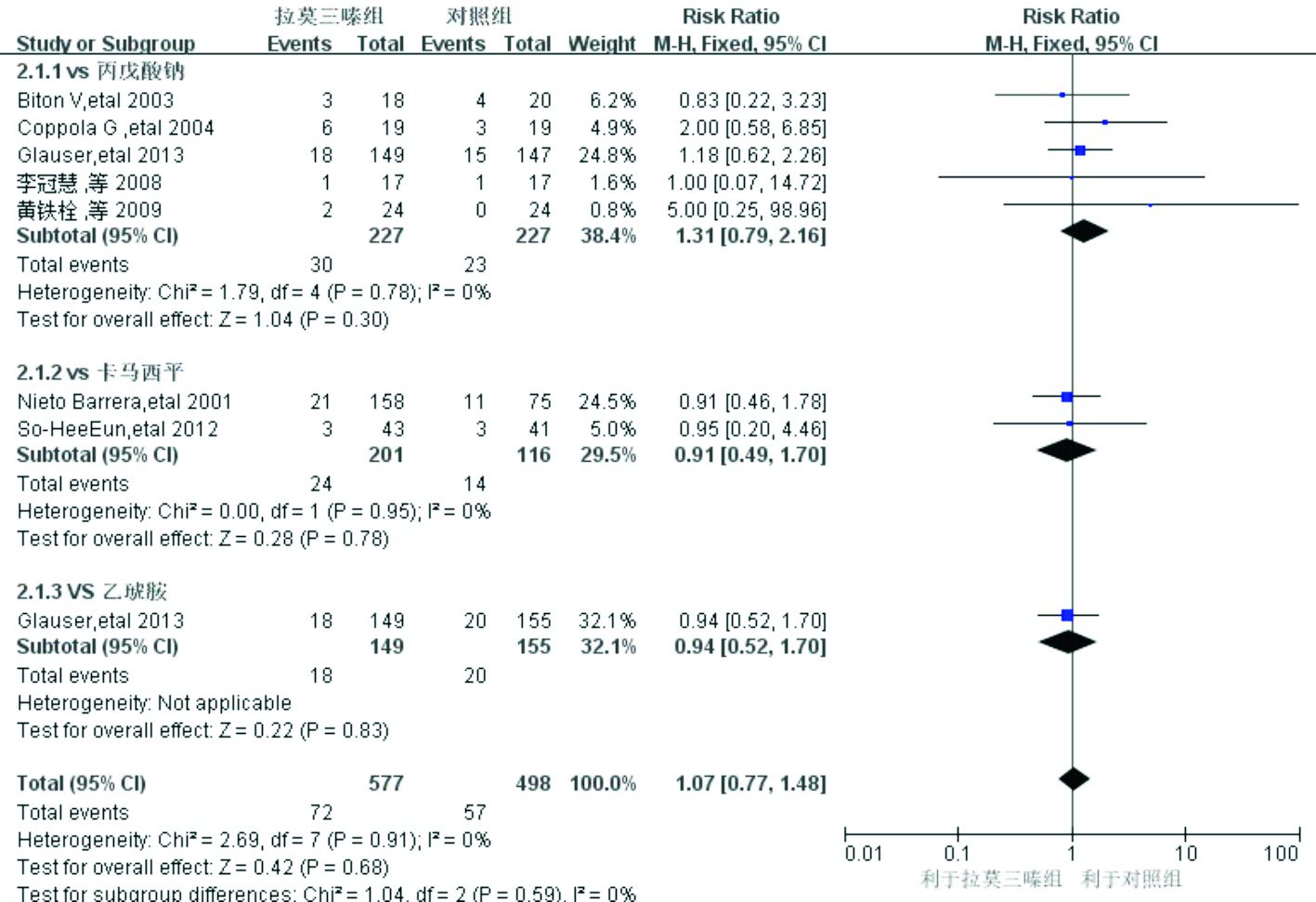
治疗期间退出率是综合反映癫癎治疗有效性和安全性的指标,也是ILEA推荐使用的主要判效指标[22]。共7项研究[15-21]报告了治疗期间的退出情况,按照干预措施不同进行分析:①拉莫三嗪vs丙戊酸钠:5项研究[15-18, 21]对比了拉莫三嗪组和丙戊酸钠的癫癎治疗期间退出率,分别为13.21%和10.13%。异质性检验结果显示无统计学异质性(P=0.78,I2=0%),采用固定效应模型合并效应量。Meta分析结果显示,两组差异无统计学意义(RR=1.31,95%CI:0.79~2.16,P=0.30),提示
尚不能认为拉莫三嗪治疗期间退出率高于丙戊酸钠;②拉莫三嗪vs卡马西平:2项研究[19-20]对比了拉莫三嗪和卡马西平,退出率分别为11.94%和12.07%。异质性检验结果显示无统计学异质性(P=0.95,I2=0%),采用固定效应模型。结果显示,两组差异无统计学意义(RR=0.91,95%CI:0.49~1.70,P=0.78),尚不能认为拉莫三嗪治疗期间退出率低于卡马西平;③拉莫三嗪vs乙琥胺:Glauser等[21]的研究报告了拉莫三嗪对比乙琥胺的结果,退出率分别为12.08%和12.90%。两组差异无统计学意义(P=0.83,I2=0%),尚不能认为拉莫三嗪治疗期间退出率低于乙琥胺。
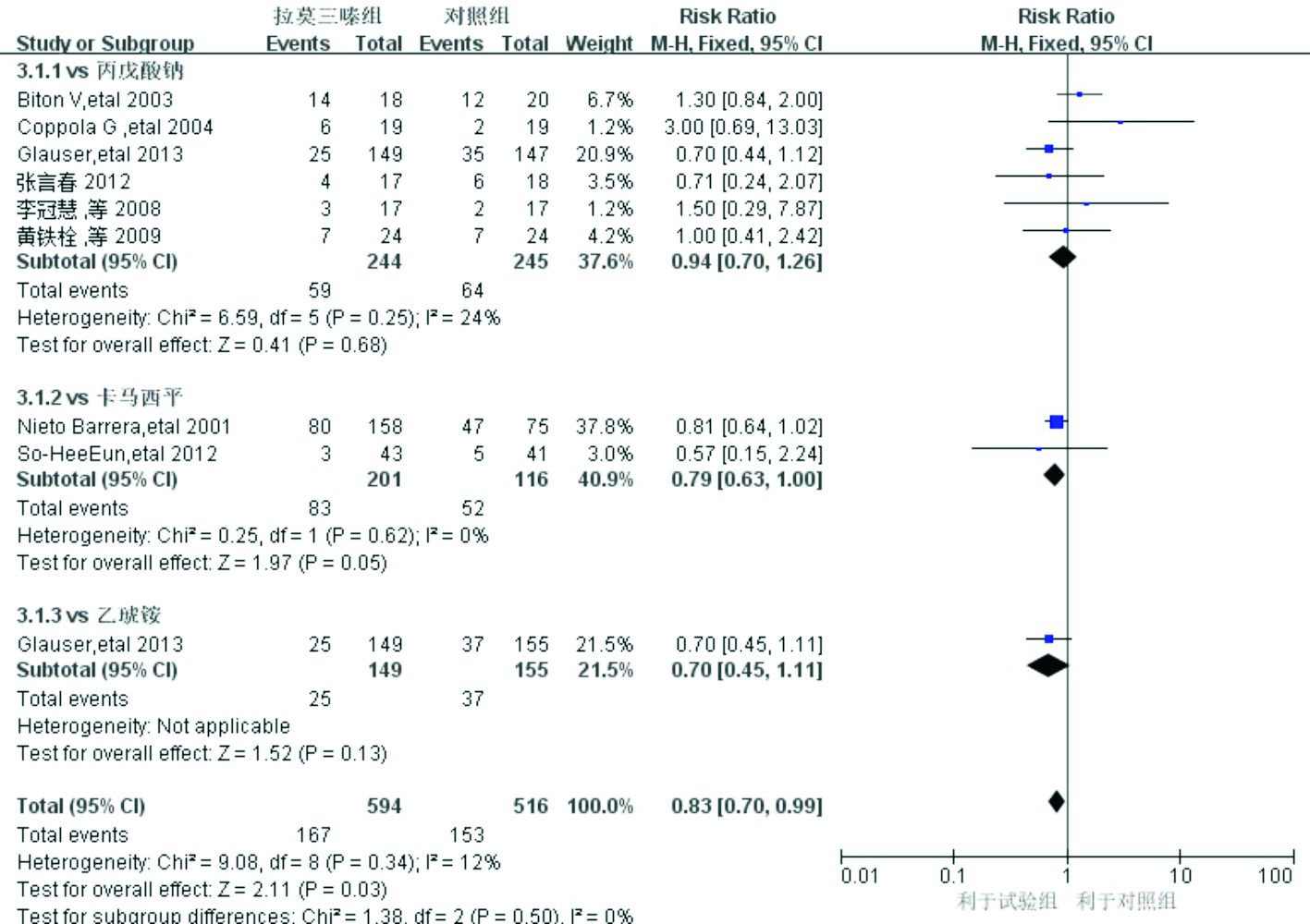
2.5 不良反应发生率8项研究[13-21]报告了不良反应的发生率。按照干预措施不同进行分析:①拉莫三嗪vs丙戊酸钠:6项研究[13, 15-18, 21]对比了拉莫三嗪和丙戊酸钠的不良反应发生率,分别为24.18%和26.12%。异质性检验结果显示无统计学差异(P=0.25,I2=24%),使用固定效应模型。结果显示两组差异无统计学意义(RR=0.94,95%CI:0.70~1.26,P=0.68),提示不能认为拉莫三嗪不良反应发生率低于丙戊酸钠;②拉莫三嗪vs卡马西平:2项研究[19-20]对比了拉莫三嗪和卡马西平的不良反应发生率,分别为41.29%和44.82%。异质性检验显示无统计学差异(P=0.62,I2=0%),使用固定效应模型。结果显示,两组差异有统计学意义(RR=0.81,95%CI:0.64~1.03,P=0.05),提示拉莫三嗪不良反应发生率低于卡马西平;③拉莫三嗪vs乙琥胺:1项研究[21]报告了拉莫三嗪对比乙琥胺的不良反应发生率,分别为16.78%和23.87%,两组差异无统计学意义(P=0.13),尚不能认为拉莫三嗪癫癎不良反应发生率低于乙琥胺。见图 2。
|
图 2 拉莫三嗪组和对照组不良反应发生率比较的Meta分析 |
2.6 不良反应
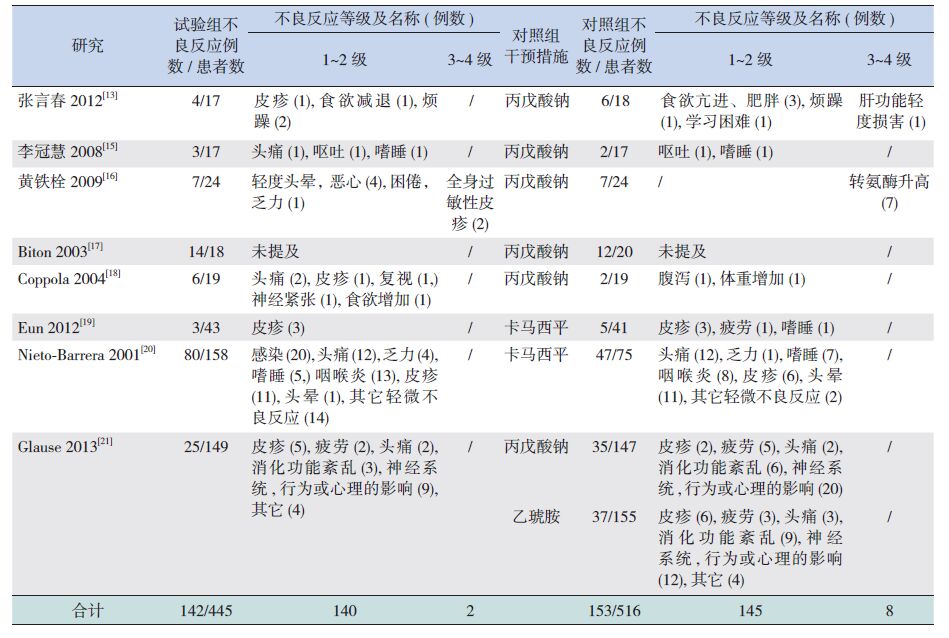
纳入研究报道的不良反应主要为1~2级轻、中度不良反应,包括皮疹、头晕、头痛、嗜睡、乏力等;3~4级严重不良反应中,拉莫三嗪组出现全身性过敏性皮疹2例,且导致患儿退出观察;对照组出现肝功能轻度损害1例,转氨酶升高7例,原始研究分析很可能与药物有关。两组3~4级不良反应发生率分别为0.45%和1.5%,试验组低于对照组,但差异无统计学意义(P=0.06)。未见5级不良反应。所有研究均未报道死亡病例发生。见表 3。
| 表 3 试验组和对照组不良反应 |
2.7 发表偏倚
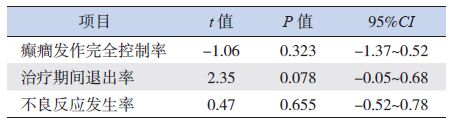
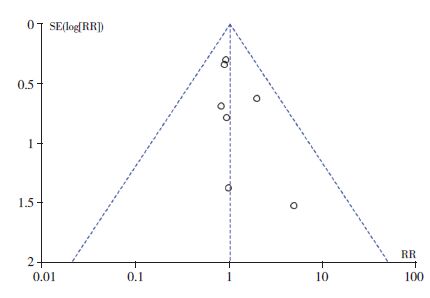
各研究在漏斗图两侧分布对称较好。而癫癎发作完全控制率、治疗期间退出率和不良反应发生率meta分析的Egger's 检验P值均>0.05,提示无明显发表偏倚。图 3~4、见表 4。
|
图 3 基于癫癎发作完全控制率的漏斗图 |
|
图 4 基于治疗期间退出率的漏斗图 |
| 表 4 Egger's 检验结果 |
3 讨论
本研究以癫癎发作完全控制率、退出率、不良反应发生率等作为结局指标,系统评价拉莫三嗪单药治疗儿童癫癎的有效性和安全性,结果显示:在有效性方面,拉莫三嗪单药治疗儿童癫癎同丙戊酸钠及卡马西平相比,在癫癎发作完全控制率、退出率方面差异无统计学意义;同乙琥胺相比,拉莫三嗪单药治疗癫癎发作完全控制率相对较低,退出率差异无统计学意义。在安全性方面,拉莫三嗪与丙戊酸钠和乙琥胺相比总体不良反应发生率相似,低于卡马西平,差异有统计学意义。相关不良反应多轻微且为一过性,罕见严重不良反应。
本研究存在的局限性:(1)纳入的9项研究仅4项详细描述了随机方法,仅3项研究对实施者和研究对象采用盲法,2项研究结果测量实施盲法,存在选择偏倚、实施偏倚及测量偏倚的可能,对结果的解释应慎重;(2)因语言限制只纳入中英文文献,存在选择偏倚的可能;(3)纳入研究的治疗和随访时间相对较短,最长的研究时间为12个月,无法评估长期治疗的疗效,有待更高质量的研究验证。
综上,可初步评价拉莫三嗪对比传统AEDs如丙戊酸钠、卡马西平等在单药治疗儿童癫癎时,癫癎发作完全控制率、退出率无明显差异,不良反应发生率相对较低,严重不良反应罕见。因此,对于传统AEDs治疗无效、不良反应明显患儿,在考虑经济性的前提下,拉莫三嗪可作为较理想的替代药物。由于纳入的临床试验存在方法学质量不高,样本量相对较小,疗程相对较短等局限性,对上述结果的解释应持谨慎态度。总体而言,拉莫三嗪单药治疗儿童癫癎有潜在的应用前景,有待高质量、大样本及较长随访时间的随机对照试验予以证实。
| [1] | 吴江. 神经病学[M]// 北京: 人民卫生出版社. 2005: 264-281. |
| [2] | World Health Organization. Epilepsy. Fact sheet N°999, World Health Organization[EB/OL]. (October, 2012). http://www.who.int/mediacentre/factsheets/fs999/en/index.html. |
| [3] | World Health Organization. Epilepsy Management at Primary Health Level in rural China[EB/OL]. (March, 2009). http://www.who.int/mental_health/neurology/epilepsy_china_report_english.pdf. |
| [4] | 李雪华. 癫癎的治疗方法研究进展[J]. 临床合理用药,2012,5 (6) :155. |
| [5] | 李世绰, 吴立文. 中华医学会. 临床诊疗指南——癫癎病分册. 北京: 人民卫生出版社, 2007 : 48 -50. |
| [6] | Sitges M, Guameros A, Nekrassov V, et al. Effects of carbamazeping, phenytion, valproic acid, oxcarbazepine, lamotrigine, topiramate and vinpoceting on the presynaptic Ca2+ channel-mediated release of [3H] glutamate: Comparison with the Na+ channel-mediated release[J]. Neuropharmacology, 2007, 53(7): 854-862. |
| [7] | Stefani A, Spadoni F, SiniscalchiA, et a1. Lamotrigine inhibits Ca2++ currents in cortical neurons: functional implications[J]. Eur J Pharmacol,2006, 307 (1) :113–116 . |
| [8] | 拉莫三嗪药品说明书. 2011 年版. GlaxoSmithKline Pharmaceuticals S.A. |
| [9] | Wheless JW, Clarke DF, ArzimanoglouA, et al. Treatment of pediatric epilepsy: European expert opinion, 2007[J]. Epileptic Disord,2007, 9 (4) :353–412 . |
| [10] | 宋春杰, 陈惠玲, 王小勇. 拉莫三嗓添加或单药治疗部分发作性癫癎的有效性和耐受性研究[J]. 中国神经免疫学和神经病学杂志,2009,16 (5) :344–347. |
| [11] | Higggins JPT, Green S. Cochrane Handbook for Systematic Reviews of Interventions. Version 5.1.0 [updated March 2011]. Available at: http://www.cochrane-handbook.org/:The CochraneCollaboration,2011. |
| [12] | National Institute of Health. National Cancer Institute. Common Terminology Criteria for Adverse Events, Version 4.3. Available from: http://evs.nci.nih.gov/ftp1/CTCAE/about.html. |
| [13] | 张言春. 拉莫三嗪治疗儿童失神癫癎的疗效研究[J]. 中国社区医师( 医学专业),2012,14 (27) :101. |
| [14] | 刘俊. 拉莫三嗪及丙戊酸钠对癫癎患儿血脂的影响[J]. 实用临床医药杂志,2011,15 (19) :133–135. |
| [15] | 李冠慧, 庞桂香, 王荣, 等. 拉莫三嗪和丙戊酸钠治疗典型失神发作疗效比较[J]. 中国实用儿科杂志,2008,23 (7) :549–550. |
| [16] | 黄铁栓, 朱金兰, 李冰, 等. 丙戊酸和拉莫三嗪治疗儿童失神癫癎的临床研究[J]. 中国当代儿科杂志,2009,11 (8) :653–655. |
| [17] | Biton V, Levisohn P, Hoyler S, et al. Lamotrigine versus valproate monotherapy-associated weight change in adolescents with epilepsy: results from a post hoc analysis of a randomized, double-blind clinical trial[J]. Journals of Child Neurology,2003, 18 (2) :133–139 . |
| [18] | Coppola G, AuricchioG, Federico R, et al. Lamotrigine versus valproic acid as first-line monotherapy in newly diagnosed typical absence seizures: an open-label, randomized, parallelgroup study[J]. Epilepsia,2004, 45 (9) :1049–1053 . |
| [19] | Eun SH, Eun BL, Lee JS. Effects of lamotrigine on cognition and behavior compared to carbamazepine as monotherapy for children with partial epilepsy[J]. Brain & Development,2012, 34 (10) :818–823 . |
| [20] | Nieto-Barrera M, Brozmanova M, Capovilla G. A comparison of monotherapy with lamotrigine or carbamazepine in patients with newly diagnosed partial epilepsy[J]. Epilepsy Research,2001, 46 (2) :145–155 . |
| [21] | Glause TA, Cnaan A, Shinnar S. Ethosuximide, valproic acid, and lamotrigine in childhood absence epilepsy: Initial monotherapy outcomes at 12 months[J]. Epilepsia,2013, 54 (1) :141–155 . |
| [22] | Commission on antiepileptic drugs. Considerations on designing clinical trials toevaluate the place of new antiepileptic drugs in the treatment of newly diagnosed and chronic patients with epilepsy[J]. Epilepsia,1998, 39 (7) :799–803 . |
 2016, Vol. 18
2016, Vol. 18