2. 华中科技大学同济医学院附属武汉儿童医院 临床研究中心, 湖北 武汉 430030;
3. 华中科技大学同济医学院附属武汉儿童医院 康复科, 湖北 武汉 430030
MED13L基因(OMIM 608771)位于染色体12q24.21区域,编码一种组成DNA结合转录因子及RNA聚合酶Ⅱ大型复合物的亚单位。有报道该基因突变与完全性大动脉转位(D-transposition of the great arteries, d-TGA)及精神发育迟缓相关[1-2]。2013年Asadollahi等[3]首先报道了MED13L基因拷贝数异常导致的MED13L单倍剂量不足综合征。2015年Adegbola等[4]将MED13L基因突变及拷贝数变异导致的疾病统称为MED13L综合征,其临床表型包括智力障碍、语言运动发育迟缓、特殊面容、肌张力低下等,伴或不伴先心病。该综合征较为罕见,国内未见报道,本文结合1例MED13L综合征患者进行文献复习,探讨该疾病的临床表型及基因特点。
1 资料与方法 1.1 研究对象患儿,男,4岁2个月,因发育落后就诊。患者3岁时被发现语言、运动发育落后,仅能发单音,步态不稳,眼神交流差,且逐渐出现刻板行为。3岁7个月开始有癫癎发作,每月发作2~3次。否认肝炎、结核及其他传染病史。患儿足月、剖宫产出生,出生史无特殊。患儿父母体健,非近亲结婚,母亲分娩时28岁、孕期无特殊,无自然流产史;家族无类似病史。体格检查:神志清楚,精神尚可,特殊面容(图 1A):斜头畸形、眼睑下垂,鼻梁扁平,两侧嘴角下沉,耳位较低。左手小手指两节。右侧睾丸下降。辅助检查:Gesell发育量表显示各项指标落后;心脏彩超提示室间隔缺损;全脊柱正侧位片提示脊柱侧弯;脑电图可见癫癎波;头部磁共振未见异常。
|
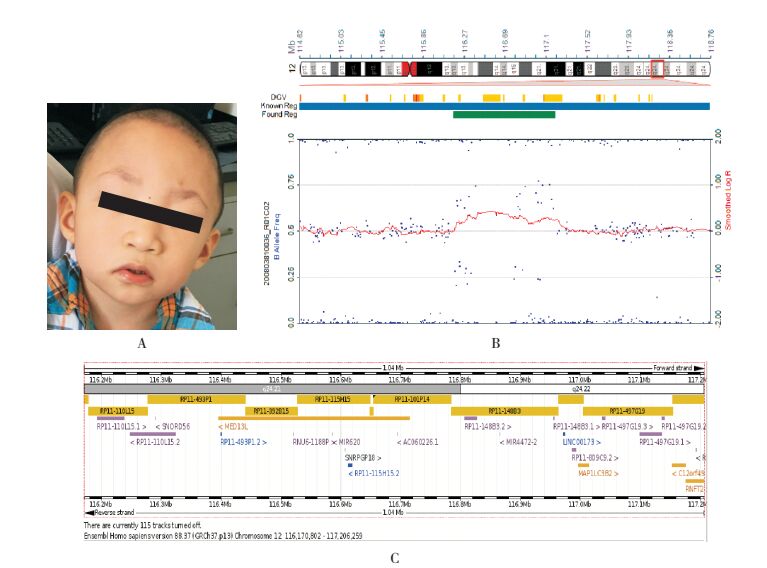
图 1 患者的面部特征及基因组芯片结果 A:患者的面部特点;B:患者全基因组水平微缺失/微重复检测结果红色基线向上偏移,提示该区域存在重复;蓝色信号多一条带,提示该区域存在3个拷贝(箭头所指);C:染色体异常区域累及的基因。 |
经患者家属知情同意,取患儿静脉血2 mL(EDTA抗凝),提取DNA,调整DNA浓度至50 ng/μL。采用Illumina cyto-12 SNP芯片进行染色体微缺失/微重复检测,采用KaryoStudio软件进行分析。
1.3 荧光定量PCR方法进行拷贝数异常验证根据芯片分析结果,选择患者MED13L基因拷贝数异常的区域对患儿及其父母进行荧光定量PCR分析。引物序列为F:CTG ATT TCC TCC TAG CAG AAC AAG;R:GAC TCA TGA TGA GTG CTA CCACG。选择单拷贝基因36B4为内参基因,引物序列为F:CAG CAA GTG GGA AGG TGT AAT CC;R:CCC ATT CTA TCA TCA ACG GGT ACAA。利用SYBR荧光染料,在ABI7500荧光定量PCR仪上以36B4基因为参考进行MED13L基因的相对定量检测,检测结果利用仪器自带软件进行相对定量分析。
2 结果 2.1 全基因组SNP芯片检测结果患儿全基因组SNP芯片检测显示:46, XY, dup(12q24.21).seq[GRCh37/hg19](116170802-117206259)*3,即12号染色体q24.21区域存在重复,片段的大小为1.03 Mb,见图 1B;查询Ensembl数据库http://grch37.ensembl.org/Homo_sapiens/Location/Overview?r=12%3A116170802-117206259,累及的基因包括MED13L、MIR620、RNFT2、NCRNA00173和MAP1LC3B2等,见图 1C。
患者MED13L基因拷贝数异常区域的荧光定量PCR验证显示:患者MED13L基因拷贝数是正常对照(2个拷贝)的1.5倍,患者父母的该区域拷贝数未见异常。
2.2 MED13L综合征的临床表型检索中国期刊全文数据库及NCBI数据库[4-5](截至2017年3月15日)发现,MED13L综合征目前国内未见报道;国外报道的MED13L综合征多为MED13L基因突变或者缺失导致,由MED13L基因部分或者完全重复所致的有5例患者:3例MED13L部分重复,2例完全重复;MED13L基因重复的患者大多存在头面部畸形、语言及运动发育落后,但本例患者的先天性脊柱侧弯在其他已报道的病例中尚未发现。见表 1。
| 表 1 MED13L基因重复所致MED13L综合征的临床表现 |
|
|
MED13L基因位于12q24.21区域,全长317 kb,含有31个外显子。该基因属于中介复合物家族成员,在胚胎发育过程中发挥重要功能。敲除MED13L基因的神经祖细胞增生能力增强,大约有1 117种基因表达发生改变[6-7]。2015年后将MED13L基因突变及拷贝数变异所致的疾病统称为MED13L综合征,其临床表型包括智力障碍、语言运动发育迟缓、面容特殊、肌张力低下等,伴或不伴先心病[4]。本研究患者存在特殊面容、室间隔缺损、语言运动发育落后及自闭症行为等临床表现,与文献报道一致。
目前国外已报道MED13L综合征大约20例,大多数为点突变或缺失突变所致,仅有5例为MED13L基因重复所导致。研究发现MED13L基因点突变的患者多数仅有心脏畸形[5]。Najmabadi等[8]发现MED13L基因杂合点突变仅导致心脏异常,而纯合点突变则导致非综合征型常染色体隐性遗传的智力障碍。Cafiero等[9]报道8例MED13L基因缺失患者,他们都存在特殊面容及运动落后,其中5例存在心脏畸形,3例存在肌张力低下。说明不同基因型的患者临床表型差异很大。本研究病例经全基因组SNP芯片检测发现,染色体12q24.21区域重复一个拷贝,该区域编码的基因包括MED13L、MAP1LC3B2、C12orf49和RNFT2,其中仅MED13L为OMIM基因;荧光定量PCR确认患者MED13L基因拷贝数高于正常对照和他的父母。最终确诊为MED13L综合征。对本病例和文献报道的5例MED13L基因重复导致的MED13L综合征总结发现,该基因型的患者也存在多系统异常,如智力落后、语言迟缓、运动发育落后、先天性心脏病、特殊面容等;但文献中重复区域包括全部MED13L基因的2例患者临床表型较轻,尤其在智力方面[4-5]。本例患者表现为轻中度智力障碍。
另外,本例患者还存在先天性脊柱侧弯和自闭症表现。有研究利用全外显子测序的方法发现MED13L可能是自闭症的候选基因,但MED13L拷贝数异常是否会导致自闭症还需要进一步的研究。MED13L基因重复与脊柱侧弯是否有关也尚未见报道。
综上所述,本研究通过全基因组芯片技术确诊1例MED13L综合征,对于凡有特殊面容、语言智力发育落后、肌张力低下的患者,及时进行基因芯片检测有助于早期确诊。
| [1] |
Schiano C, Casamassimi A, Vietri MT, et al. The roles of mediator complex in cardiovascular diseases[J]. Biochim Biophys Acta, 2014, 1839(6): 444-451. DOI:10.1016/j.bbagrm.2014.04.012 (  0) 0) |
| [2] |
Muncke N, Jung C, Rüdiger H, et al. Missense mutations and gene interruption in PROSIT240, a novel TRAP240-like gene, in patients with congenital heart defect (transposition of the great arteries)[J]. Circulation, 2003, 108(23): 2843-2850. DOI:10.1161/01.CIR.0000103684.77636.CD (  0) 0) |
| [3] |
Asadollahi R, Oneda B, Sheth F, et al. Dosage changes of MED13L further delineate its role in congenital heart defects and intellectual disability[J]. Eur J Hum Genet, 2013, 21(10): 1100-1104. DOI:10.1038/ejhg.2013.17 (  0) 0) |
| [4] |
Adegbola A, Musante L, Callewaert B, et al. Redefining the MED13L syndrome[J]. Eur J Hum Genet, 2015, 23(10): 1308-1317. DOI:10.1038/ejhg.2015.26 (  0) 0) |
| [5] |
van Haelst MM, Monroe GR, Duran K, et al. Further confirmation of the MED13L haploinsufficiency syndrome[J]. Eur J Hum Genet, 2015, 23(1): 135-138. DOI:10.1038/ejhg.2014.69 (  0) 0) |
| [6] |
Risheg H, Graham JM Jr, Clark RD, et al. A recurrent mutation in MED12 leading to R961W causes Opitz-Kaveggia syndrome[J]. Nat Genet, 2007, 39(4): 451-453. DOI:10.1038/ng1992 (  0) 0) |
| [7] |
Utami KH, Winata CL, Hillmer AM, et al. Impaired development of neural-crest cell-derived organs and intellectual disability caused by MED13L haploinsufficiency[J]. Hum Mutat, 2014, 35(11): 1311-1320. (  0) 0) |
| [8] |
Najmabadi H, Hu H, Garshasbi M, et al. Deep sequencing reveals 50 novel genes for recessive cognitive disorders[J]. Nature, 2011, 478(7367): 57-63. DOI:10.1038/nature10423 (  0) 0) |
| [9] |
Cafiero C, Marangi G, Orteschi D, et al. Novel de novo heterozygous loss-of-function variants in MED13L and further delineation of the MED13L haploinsufficiency syndrome[J]. Eur J Hum Genet, 2015, 23(11): 1499-1504. DOI:10.1038/ejhg.2015.19 (  0) 0) |
| [10] |
Codina-Solà M, Rodríguez-Santiago B, Homs A, et al. Integrated analysis of whole-exome sequencing and transcriptome profiling in males with autism spectrum disorders[J]. Mol Autism, 2015, 6: 21. DOI:10.1186/s13229-015-0017-0 (  0) 0) |
 2017, Vol. 19
2017, Vol. 19


