Li-Fraumeni综合征(Li-Fraumeni syndrome, LFS)于1969年首次报道,是一种典型的遗传易感肿瘤综合征,呈常染色体显性遗传,又被称为SBLA(sarcoma, breast, leukemia, and adrenal gland cancer)综合征,与其最为相关的疾病为肉瘤、乳腺癌、肾上腺皮质癌,也可为白血病、淋巴瘤、肾母细胞瘤等[1]。LFS发病与基因遗传学改变密切相关,关于LFS的致病基因,尽管有CHEK2、BRCA1基因与Li-Fraumeni综合征发病关系的报道,但目前认为TP53基因是比较明确的LFS致病基因,大约70%的患者存在TP53基因[2-4]。
LFS在国内研究较少。以Li-Fraumeni综合征为关键词检索万方数据库,共检索出中文期刊文献10篇,其中仅1篇报道3例乳腺癌患者检出TP53基因改变[5],其余9篇为综述国外的研究进展;中国知网检索出相关中文期刊文献12篇,除去重复文献及国外文献翻译或文摘,仅1篇相关综述。而PubMed关于LFS的报道中仅1篇为LFS在中国大陆人群的家系报道[6],该家系6名成员被诊断不同肿瘤,包括乳腺癌、成神经管细胞瘤、肾上腺嗜铬细胞瘤、脉络丛乳头状癌。因此,为了提高对LFS的认识和有效的监测、管理,本文对一个存在遗传因素的横纹肌肉瘤家系进行报道和文献复习,探讨Li-Fraumeni综合征的临床特点。
1 资料与方法 1.1 研究对象先证者,男,2岁6个月,发现左颌下肿物1月余。患儿2岁2个月出现打鼾,2岁5个月发现左颌下无痛性肿物,并进行性增大,患儿逐渐出现发音障碍、日间张口呼吸及夜间憋醒。面颊部CT提示左侧咽旁间隙占位性病变。全麻下行“左口底、咽旁肿块切取活检术+气管切开术”,病理提示胚胎型横纹肌肉瘤。术后未予特殊治疗,左下颌肿物较前增大,1个月后复查头颈部CT提示左颌下横纹肌肉瘤伴囊变坏死,口底、舌根、腺样体及左侧颌下腺、咽鼓管圆枕受侵可能性大。诊断:左颌下胚胎型横纹肌肉瘤(T2bNxM0,TNM3期),病理分期Ⅲ期,临床中危。VAC(长春新碱+放线菌素D+环磷酰胺)化疗2疗程后行病灶部位Ⅰ-125放射性粒子植入术,术后交替予VAC、VI(长春新碱+伊利替康)方案化疗,目前仍在治疗中。
患儿父母非近亲结婚,患儿哥哥3岁时经病理确诊为多形型横纹肌肉瘤,治疗无效死亡;姐姐及弟弟体健。患儿外祖母于43岁时确诊乳腺癌,乳腺癌术后同年被诊断出结肠癌症。
1.2 TP53基因突变检测征得患儿家长知情同意,采集患儿及其父母、姐弟的外周血标本,用Sanger基因测序方法行TP53基因突变检测。
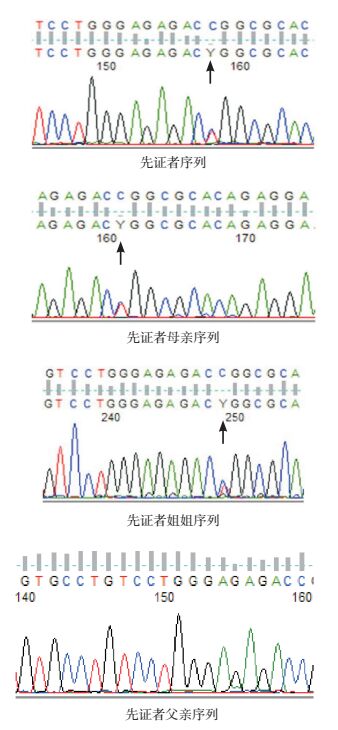
2 结果患儿及其母亲、姐姐均存在TP53基因EXON 8的错义突变:c.844C > T(p.Arg282Trp)(杂合),患儿父亲及弟弟未检出该变异,见图 1。
|
图 1 先证者及其父母、姐姐的TP53基因测序结果 患儿及其母亲、姐姐的TP53基因均检出c.844C>T(p.Arg282Trp)杂合突变(突变位点如箭头所示),患儿父亲未检出该变异。 |
LFS是一种遗传易感性肿瘤综合征,肿瘤发病年龄早,个体肿瘤发生率高[7]。最早于1988年由Li和Fraumeni发表的LFS诊断标准[8]需要同时符合以下2个条件:(1)先证者45岁前确诊肉瘤;(2)一名一级或二级亲属在45岁前确诊任何类型的癌症或者任何年龄确诊肉瘤。2009年更新的Chompret诊断标准[9]进一步扩大了疾病范围,其诊断符合以下标准中的任意一条即可:(1)先证者在46岁以前诊断为LFS疾病谱系(包括软组织肉瘤、骨肉瘤、绝经前乳腺癌、脑肿瘤、肾上腺皮脂瘤、白血病或者肺细支气管肺泡癌)中的任何疾病,并且至少有1名一级或二级亲属在56岁前确诊LFS谱系疾病(如果先证者患乳腺癌则家系患病中不包括乳腺癌);(2)先证者患多种肿瘤(多种乳腺肿瘤除外)且其中2种属于LFS谱系肿瘤,最早发现的肿瘤于46岁以前发病;(3)先证者如果为肾上腺皮质癌或者脉络丛肿瘤,则无论家系是否患病。2015年Bougeard等[10]发表的一篇法国人群大样本研究纳入1 730例LFS患者,首次肿瘤发生的平均年龄为24.9岁,41%的患者在18岁以前即确诊肿瘤;在儿童患者中,LFS疾病谱系中最常见的依次为骨肉瘤、肾上腺皮质癌、中枢神经系统肿瘤及软组织肿瘤,发病率分别为30%、27%、26%及23%;而成人发病率最高的为乳腺癌(79%)及软组织肿瘤(27%)。本文先证者于2岁被诊断为横纹肌肉瘤,其哥哥在3岁被诊断为横纹肌肉瘤,其外祖母于43岁被诊断为乳腺癌,符合LFS诊断标准,也符合儿童LFS患者疾病谱系的特点。
TP53基因是比较明确的LFS致病基因,位于17p13.1,作为一种抑癌基因,它可以转录产生P53蛋白,该蛋白可以延迟细胞周期进程,为细胞修复提供机会。TP53变异的情况下,细胞内损伤的DNA得不到修复,进而引起细胞癌变,也是这类患者对于抗肿瘤药物反应不良及预后不佳的原因;而且存在TP53基因突变的LFS患者患二次肿瘤的几率明显高于该基因正常的患者[10-11]。目前已经发现20余种TP53基因的变异,以缺失突变最为常见。6个热点突变可见于20%的TP53突变患者,包括p.R175H、p.G245S、p.R248Q、p.R248W、p.R273H及p.R282W[12-13]。本文所报道家系中的TP53基因改变就属于6个常见热点突变之一。
LFS患者有较大的几率患二次甚至多次肿瘤。1998年Hisada等[14]发现,200例LFS患者中15%罹患二次肿瘤,4%罹患三次肿瘤,2%的患者罹患四次肿瘤;而2007年日本报告1例患者共出现9次不同部位的原发性肿瘤[15]。因此,应对LFS家系的患者进行系统监测管理:定期体格检查、血液学检查及影像学检查,以早期发现二次肿瘤[16]。2016年加拿大学者研究发现,予以定期监测TP53突变的LFS患者5年生存率从59.6%提高到88.8%[17-18]。2017年3月Alderfer等[19]发表一项针对LFS患者家庭成员的调查,12名12~25岁的被调查者均认为需要向LFS患者的家庭成员提供基因及肿瘤相关检查,然而最终是否接受检查则取决于个人意愿;同时该研究发现,在最终实际接受检查的人群中,上述检查并未对其后续生活带来负面影响。NCCN(美国国立癌症网络)甚至发表了基因相关的乳腺癌及卵巢癌的风险评估相关指南,并且在2017年进行了更新[20-21]。一旦确诊患有LFS,即对患者家庭成员进行筛查,乳腺癌、结肠直肠癌、胃癌、肺癌、前列腺癌及黑色素瘤等肿瘤可能在无症状时即被发现;而对LFS患者家庭成员中TP53突变基因携带者自幼进行早期疾病监测,可早期诊断的疾病更加广泛,包括乳腺癌、软组织肉瘤、脑部肿瘤、骨肉瘤、肾上腺皮质癌、膀胱癌、结肠直肠癌、胃癌、肾母细胞瘤、肝癌、肺癌、黑色素瘤及胰腺癌[22]。因此,本文先证者及其母亲、姐姐都应定期系统监测。LFS家系中儿童(0~18岁)的肿瘤筛查方案(Toronto方案)见表 1 [16]。需要着重强调的是,儿童肿瘤的危险因素目前仍难以全面评估,强烈推荐对存在TP53基因改变或者已有明确肿瘤(符合LFS诊断)的儿童进行终生随访及肿瘤检测。
| 表 1 Li-Fraumeni综合征家系的肿瘤早期监测方案 |
|
|
总之,越来越多的学者认为LFS在儿童肿瘤的发病中占有重要地位[16]。对于儿童肿瘤患者,尤其是某些具有遗传易感性的肿瘤,在明确诊断的同时有必要进行遗传学评估,尤其是进行TP53基因检测。如果存在TP53基因突变,治疗上则应当更为积极,并采取适当措施优化患儿及家庭成员管理。
| [1] |
Li FP, Fraumeni JF Jr. Soft-tissue sarcomas, breast cancer, and other neoplasms[J]. Ann Intern Med, 1969, 71(4): 747-752. DOI:10.7326/0003-4819-71-4-747 (  0) 0) |
| [2] |
Ruijs MW, Verhoef S, Rookus MA, et al. TP53 germline mutation testing in 180 families suspected of Li-Fraumeni syndrome:mutation detection rate and relative frequency of cancers in different familial phenotypes[J]. J Med Genet, 2010, 47(6): 421-428. DOI:10.1136/jmg.2009.073429 (  0) 0) |
| [3] |
Evans DG, Birch JM, Narod SA. Is CHEK2 a cause of the Li-Fraumeni syndrome?[J]. J Med Genet, 2008, 45(1): 63-64. (  0) 0) |
| [4] |
Pennington KP, Walsh T, Lee M, et al. BRCA1, TP53, and CHEK2 germline mutations in uterine serous carcinoma[J]. Cancer, 2013, 119(2): 332-338. DOI:10.1002/cncr.27720 (  0) 0) |
| [5] |
杨晓晨, 胡震, 吴炅, 等. 中国乳腺癌高风险人群中TP53基因胚系突变的研究[J]. 中华医学遗传学杂志, 2015, 32(6): 761-765. (  0) 0) |
| [6] |
Hu H, Liu J, Liao X, et al. Genetic and functional analysis of a Li Fraumeni syndrome family in China[J]. Sci Rep, 2016, 6: 20221. DOI:10.1038/srep20221 (  0) 0) |
| [7] |
Garber JE, Goldstein AM, Kantor AF, et al. Follow-up study of twenty-four families with Li-Fraumeni syndrome[J]. Cancer Res, 1991, 51(22): 6094-6097. (  0) 0) |
| [8] |
Li FP, Fraumeni JF, Mulvihill JJ, et al. A cancer family syndrome in twenty-four kindreds[J]. Cancer Res, 1988, 48(18): 5358-5362. (  0) 0) |
| [9] |
Tinat J, Bougeard G, Baert-Desurmont S, et al. 2009 version of the Chompret criteria for Li-Fraumeni syndrome[J]. J Clin Oncol, 2009, 27(26): e108-109. DOI:10.1200/JCO.2009.22.7967 (  0) 0) |
| [10] |
Bougeard G, Renaux-Petel M, Flaman JM, et al. Revisiting Li-Fraumeni syndrome from TP53 mutation carriers[J]. J Clin Oncol, 2015, 33(21): 2345-2352. DOI:10.1200/JCO.2014.59.5728 (  0) 0) |
| [11] |
Hof J, Krentz S, van Schewick C, et al. Mutations and deletions of the TP53 gene predict nonresponse to treatment and poor outcome in first relapse of childhood acute lymphoblastic leukemia[J]. J Clin Oncol, 2011, 29(23): 3185-3193. DOI:10.1200/JCO.2011.34.8144 (  0) 0) |
| [12] |
Olivier M, Goldgar DE, Sodha N, et al. Li-Fraumeni and related syndromes:correlation between tumor type, family structure, and TP53 genotype[J]. Cancer Res, 2003, 63(20): 6643-6650. (  0) 0) |
| [13] |
Wasserman JD, Novokmet A, Eichler-Jonsson C, et al. Prevalence and functional consequence of TP53 mutations in pediatric adrenocortical carcinoma:a children's oncology group study[J]. J Clin Oncol, 2015, 33(6): 602-609. DOI:10.1200/JCO.2013.52.6863 (  0) 0) |
| [14] |
Hisada M, Garber JE, Fung CY, et al. Multiple primary cancers in families with Li-Fraumeni syndrome[J]. J Natl Cancer Inst, 1998, 90(8): 606-611. DOI:10.1093/jnci/90.8.606 (  0) 0) |
| [15] |
Izawa N, Matsumoto S, Manabe J, et al. A Japanese patient with Li-Fraumeni syndrome who had nine primary malignancies associated with a germline mutation of the p53 tumor-suppressor gene[J]. Int J Clin Oncol, 2008, 13(1): 78-82. DOI:10.1007/s10147-007-0692-8 (  0) 0) |
| [16] |
Kratz CP, Achatz MI, Brugières L, et al. Cancer Screening Recommendations for individuals with Li-Fraumeni syndrome[J]. Clin Cancer Res, 2017, 23(11): e38-e45. DOI:10.1158/1078-0432.CCR-17-0408 (  0) 0) |
| [17] |
Villani A, Shore A, Wasserman JD, et al. Biochemical and imaging surveillance in germline TP53 mutation carriers with Li-Fraumeni syndrome:11 year follow-up of a prospective observational study[J]. Lancet Oncol, 2016, 17(9): 1295-1305. DOI:10.1016/S1470-2045(16)30249-2 (  0) 0) |
| [18] |
Villani A, Tabori U, Schiffman J, et al. Biochemical and imaging surveillance in germline TP53 mutation carriers with Li-Fraumeni syndrome:a prospective observational study[J]. Lancet Oncol, 2011, 12(6): 559-567. DOI:10.1016/S1470-2045(11)70119-X (  0) 0) |
| [19] |
Alderfer MA, Lindell RB, Viadro CI, et al. Should Genetic Testing be Offered for Children? The perspectives of adolescents and emerging adults in families with Li-Fraumeni Syndrome[J]. J Genet Couns, 2017, 26(5): 1106-1115. DOI:10.1007/s10897-017-0091-x (  0) 0) |
| [20] |
Ballinger ML, Mitchell G, Thomas DM. Surveillance recommendations for patients with germline TP53 mutations[J]. Curr Opin Oncol, 2015, 27(4): 332-337. DOI:10.1097/CCO.0000000000000200 (  0) 0) |
| [21] |
Daly MB, Pilarski R, Berry M, et al. NCCN Guidelines Insights:Genetic/Familial High-Risk Assessment:Breast and Ovarian, Version 2.2017[J]. J Natl Compr Canc Netw, 2017, 15(1): 9-20. DOI:10.6004/jnccn.2017.0003 (  0) 0) |
| [22] |
McBride KA, Ballinger ML, Killick E, et al. Li-Fraumeni syndrome:cancer risk assessment and clinical management[J]. Nat Rev Clin Oncol, 2014, 11(5): 260-271. DOI:10.1038/nrclinonc.2014.41 (  0) 0) |
 2017, Vol. 19
2017, Vol. 19


