特应性皮炎(atopic dermatitis, AD)是一种慢性复发性炎症性皮肤病,在西方发达国家的发病率为10%~20%[1],我国最新的流行病学调查显示1~7岁儿童的AD发病率高达12.94%[2]。儿童AD,特别是婴幼儿AD,除了疾病本身所造成的皮肤损伤外,其皮肤病变所引起的瘙痒会严重影响患儿的生活质量。已知婴幼儿的生长发育主要在睡眠中发生,AD的瘙痒会直接导致患儿睡眠不足,影响睡眠质量,从而间接地影响生长发育;在较大儿童,皮肤问题会增加其自卑感,从而会影响其人际交往等[3],因此了解AD对儿童日常生活的影响在AD的管理上十分重要。
婴儿皮炎生活质量指数(Infants' Dermatitis Quality of Life Index, IDQOL)、儿童皮炎生活质量指数(Children's Dermatology Life Quality Index, CDLQI)和皮炎家庭生活影响指数(Dermatitis Family Impact, DFI)问卷是目前被广泛认可的评估AD患儿及家庭生活质量的工具[4]。利用该工具,国外针对儿童AD已进行了很多临床观察,均揭示儿童AD不仅影响患儿本身的生活质量,也影响其家庭生活质量[5-7]。鉴于不同国家或区域、不同人种生活方式的不同,可能相同疾病对生活质量的影响会存在着差异。本研究对上海地区1~12岁AD患儿治疗前后的生活质量进行了前瞻性临床研究,现报道如下。
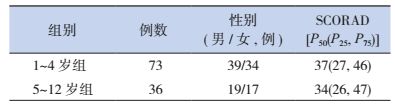
1 资料与方法 1.1 研究对象以2013年1月至2015年2月在我院皮肤科门诊就诊的AD患儿为研究对象。根据纳入与排除标准共纳入AD患儿109例,其中男58例,女51例;年龄1~11岁,中位年龄3岁。AD患儿生活质量的评估参照IDQOL问卷和CDLQI问卷,两份问卷分别适应于1~4岁和5~12岁患儿,因此,本研究将109例AD患儿分成两组,即1~4岁组和5~12岁组。两个年龄组的性别分布及特应性皮炎严重程度评分(SCORAD)见表 1。
| 表 1 1~4岁组和5~12岁组AD患儿的一般资料 |
同时在我院儿保科收集55例正常健康儿童作为对照组,其中男35例,女20例;年龄1~11岁,中位年龄4岁。AD组和对照组在年龄、性别的比较中差异无统计学意义(P > 0.05)。
1.2 入选标准及排除标准研究对象的入选标准:(1)年龄1~12岁;(2)按照Williams诊断标准确诊为AD[8];(3)患儿及家长自愿参加临床试验并签署知情同意书;(4)为我院初诊患儿,且未经过系统的治疗。
入组的排除标准:(1)并发慢性疾病的患儿,如哮喘、食物不耐受或过敏性鼻炎;(2)存在心理问题可能影响随访的患儿;(3)存在其他皮肤病,可能影响AD严重性评估的患儿;(4)看护人对问卷理解能力差的患儿。
1.3 AD严重程度评判标准AD的严重程度评判参照SCORAD评分体系[9],评判标准依据皮疹的范围和皮疹的程度。皮疹程度包括6项指标:红斑、水肿/丘疹、抓痕、渗出/结痂、苔癣化和干燥。AD程度评估总分为103分,其中轻度: < 25分,中度:25~50分,重度: > 50分。
1.4 AD患儿生活质量的评估AD患儿生活质量的评估参照IDQOL问卷和CDLQI问卷。每份问卷均包括10个问题,主要涉及患儿近1周内的症状和困难。IDQOL问卷包括瘙痒、情绪、睡眠时间、睡眠障碍、进食、沐浴、穿衣、家庭活动、玩耍或游泳、治疗问题;CDLQI问卷包括瘙痒或搔抓、情绪、人际交往、睡眠、兴趣爱好、体育活动、上课、治疗、穿衣、欺负/取笑/回避问题。每道答题分为4个等级,分别为无影响(0分)、轻度影响(1分)、中度影响(2分)、重度影响(3分)。每份问卷的最高分值为30分。IDQOL问卷和CDLQI问卷分别适应于1~4岁和5~12岁患儿,前者由患儿看护人完成,后者在患儿看护人的帮助下完成。
1.5 AD患儿家庭生活质量的评估AD患儿家庭生活质量的评估采用DFI问卷。该问卷同样包括10个问题,主要涉及患儿近1周内对看护人生活质量的影响,包括情绪、疲劳度、家务量、睡眠、购物和家庭成员关系等。每道答题分为4个等级,分别为无影响(0分)、轻度影响(1分)、中度影响(2分)、重度影响(3分)。每份问卷的最高分值为30分。该问卷适应于本研究的所有患儿,由患儿看护人完成。
所有AD患儿均被要求进行两次问卷调查,分别在初诊时和治疗后3个月。每次调查包括两份问卷(IDQOL/CDLQI和DFI),同一人的两次调查要求同一看护人回答。
1.6 治疗方案轻度AD患儿外用弱效激素(0.05%地奈德软膏,重庆华邦制药有限公司),中、重度AD患儿外用中效激素(0.1%曲安奈德益康唑乳膏,西安杨森制药有限公司),均为每天两次,治疗时间持续1~2周,待皮肤基本消退后仅使用外用润肤剂治疗,皮损复发按照疾病的严重程度重复使用外用激素。并结合问卷结果,由有经验的皮肤科医生向患儿看护人进行AD有关知识的普及教育与家庭护理的指导。
1.7 统计学分析使用SPSS 22.0统计软件包进行数据处理与分析。使用Kolmogorov-Smirnov检验对各计量资料进行正态性检验。正态分布的计量资料以均数±标准差(x±s)表示,两组间比较采用独立样本t检验;非正态分布的资料采用中位数和四分位数间距[P50(P25,P75)]描述,两组间比较采用秩和检验(Mann-Whitney U test)。正态分布的资料治疗前后比较采用配对样本t检验,非正态分布的资料采用Wilcoxon秩和检验。计数资料以例数或百分率(%)表示,两组间的比较采用χ2检验。儿童生活质量与SCORAD评分之间的相关性使用Pearson相关分析及直线回归分析。P < 0.05示差异有统计学意义。
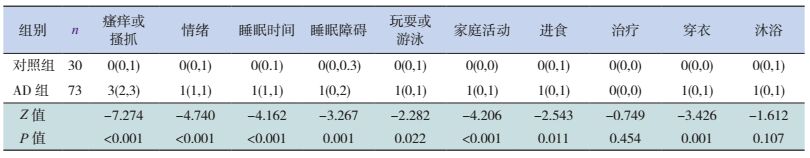
2 结果 2.1 AD患儿IDQOL评分治疗前,对1~4岁AD患儿影响较大的3个问题分别为“瘙痒或搔抓”“情绪”和“睡眠”。与对照组比较,AD患儿除了“治疗”和“沐浴”两个方面没有受到明显影响外,其他方面均受到了明显影响(P < 0.05),见表 2。
| 表 2 1~4岁组AD患儿与对照组IDQOL评分比较 [P50(P25,P75)] |
2.2 AD患儿CDLQI评分
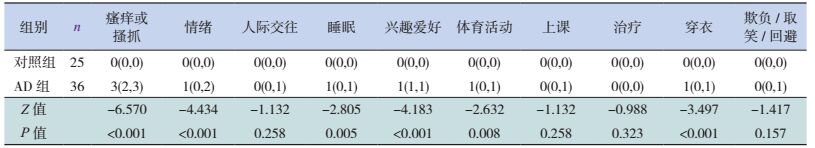
治疗前,对5~12岁AD患儿影响较大的3个问题同样为“瘙痒或搔抓”“情绪”和“睡眠”。与对照组比较,AD患儿除了“人际交往”“上课”“治疗”和“欺负/取笑/回避问题”4个方面没有受到明显影响外,其他方面均受到了明显影响(P < 0.05),见表 3。
| 表 3 5~12岁组AD患儿与对照组CDLQI评分的比较 [P50(P25,P75)] |
2.3 AD患儿DFI评分
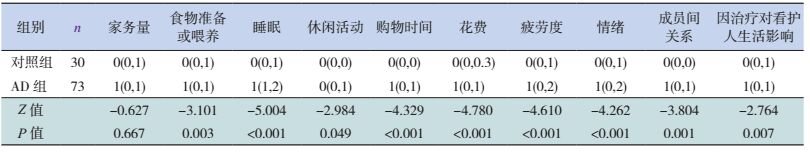
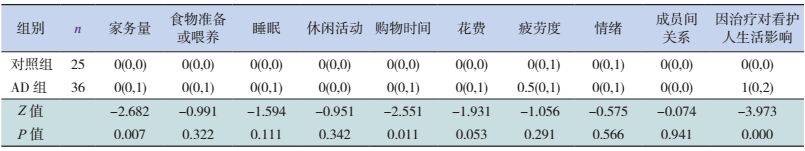
治疗前,对于1~12岁所有AD患儿的看护人,影响较大的3个问题分别是“睡眠”“疲劳度”和“情绪”。将AD患儿分成两个年龄组(即1~4岁组和5~12岁组)分析发现:与对照组比较,1~4岁组看护人除了“家务量”问题没有受到明显影响外,其他问题均受到了明显影响(P < 0.05),见表 4。而在5~12岁组中,“家务量”“购物时间”“因治疗对看护人生活影响”3个方面受到了明显影响(P < 0.05),其他方面未受到明显影响,见表 5。
| 表 4 1~4岁组AD患儿与对照组DFI评分的比较 [P50(P25,P75)] |
| 表 5 5~12岁组AD患儿与对照组DFI评分的比较 [P50(P25,P75)] |
2.4 SCORAD评分与IDQOL/CDLQI和DFI评分的相关性分析
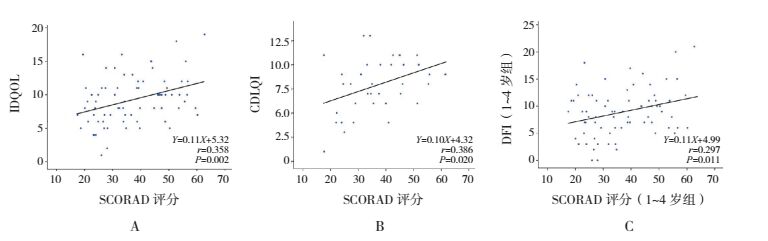
采用线性回归方法,对SCORAD评分与治疗前IDQOL/CDLQI评分进行相关性分析,结果发现:SCORAD评分与IDQOL/CDLQI总分均存在着明显正相关关系(分别r=0.358,P=0.002;r=0.386,P=0.020),见图 1A~B。
|
图 1 SCORAD评分与IDQOL、CDLQI和DFI评分的相关性 A:SCORAD评分与IDQOL总分的相关性;B:SCORAD评分与CDLQI总分的相关性;C:SCORAD评分与1~4岁组DFI总分的相关性。 |
同样对SCORAD评分与治疗前DFI评分进行相关性分析,结果发现:在1~4岁组中,SCORAD评分与DFI评分存在明显正相关关系(r=0.297,P=0.011;图 1C);在5~12岁组中,SCORAD评分与DFI评分不存在明显相关关系(r=0.107,P=0.534);而SCORAD评分与DFI评分各项问题的评分相关关系中,仅发现1~4岁组的SCORAD评分与“睡眠”和“疲劳度”评分存在明显正相关关系(分别r=0.367,P=0.001;r=0.318,P=0.006)。
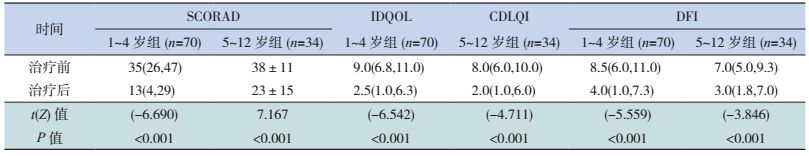
2.5 局部外用激素治疗对IDQOL/CDLQI和DFI评分的改善作用入组的109例AD患儿中,104例(95.4%)在局部间歇外用激素治疗3个月后接受了随访,其中完成IDQOL问卷的有70例(1~4岁组),完成CDLQI问卷的有34例(5~12岁组)。对完成问卷的70例1~4岁AD患儿和34例5~12岁AD患儿治疗前后进行统计,结果显示,治疗3个月后两组患儿SCORAD评分均显著降低(P < 0.001)。治疗3个月后IDQOL、ICDLQI及DFI评分均显著降低(均P < 0.001)。见表 6。
| 表 6 外用激素治疗后SCORAD/IDQOL/CDLQI和DFI的改善 [x±s或P50(P25,P75)] |
3 讨论
中国特应性皮炎诊疗指南(2014版)提出,AD治疗的目的是缓解或消除临床症状,消除诱因和/或加重因素,减少和预防复发,提高患者的生活质量[10]。目前对于生活质量的评估日益受到临床重视,已成为评估疾病严重程度的一部分。
本研究显示,AD患儿的生活质量受到了明显影响,直接来自于患儿或患儿家长的主观意识表明,影响IDQOL和CDLQI较大的3个问题均是“瘙痒”或“搔抓”、“情绪”和“睡眠”。此进一步验证了既往大多数的研究,即瘙痒、睡眠和情绪问题是影响患儿生活质量的主要问题,如韩国研究显示,影响IDQOL最明显的问题也是“瘙痒”“情绪影响”及“入睡时间”[11]。另外一项研究也表明瘙痒严重影响AD患者生活质量,而且高达79%的患儿睡眠受到干扰,瘙痒和长期睡眠不足影响患儿的情绪[7]。另外,也有研究显示,在中、重度AD患儿中,影响IDQOL最大的3个问题分别是“瘙痒”“情绪影响”及“治疗”,影响CDLQI最大的3个问题分别是“空闲时间”“瘙痒”及“人际关系”[12]。
已知IDQOL和CDLQI问卷所涉及的问题都是主观意识问题,正常儿童在生长发育过程中也会遇到类似问题,只是与患儿主观意识的程度不同。鉴于此,本研究利用无AD的健康体检儿童作为对照,结果显示:与健康对照组相比,IDQOL问卷的10个问题中,AD组“治疗”和“沐浴”并没有受到影响,“瘙痒”“情绪”和“睡眠”仍然是主要的问题,且“家庭活动”和“穿衣”问题也明显突出;CDLQI问卷的10个问题,与健康对照组相比,AD组“瘙痒”“情绪”和“睡眠”仍然是主要的问题,“兴趣爱好”“穿衣”“体育活动”方面也受到了明显影响。这些结果提示,不管任何年龄的患儿,主观上的瘙痒、情绪和睡眠的影响都是相对重要的问题;此外,在1~4岁组的AD患儿中,对家庭活动、穿衣等方面的影响较为突出;在5~12岁的患儿中,对兴趣爱好、穿衣等方面的影响较为突出。
从直接来自于患儿家长的主观意识还表明,影响DFI较大的3个问题是“睡眠”“疲劳度”和“情绪”。实际上,既往研究也显示AD对患儿DFI的影响差异很大。有研究表明高达87.1%的患儿家长睡眠受到影响[7],从而增加了疲惫感,影响家长情绪;但是也有研究表明,在DFI问题中,除了对睡眠的影响比较大外,经济压力和食物准备也受到了明显影响[13];Chernyshov等[14]研究发现,AD患者家长情绪及家庭经济开支影响比较大,照顾AD患者也占用很多时间,因而严重影响家长自由支配的时间。由此可见,AD对家庭生活质量的影响是多方面的,不同的生活方式、主观的承受能力可能决定DFI的变化不同。本研究将AD患儿与健康体检儿进行比较,结果显示1~4岁组除了“家务量”问题没有受到明显影响外,其他问题均受到了明显影响。而在5~12岁组中,“家务量” “购物时间” “因治疗对看护人生活影响”3个方面受到了明显影响,其他均未受到明显影响。有研究表明照顾学龄期AD患者家长精神压力及疲劳度比照顾学龄前患儿明显减轻[15],本研究结果与之一致,考虑与AD严重程度随着年龄的增长逐渐减轻及家长对AD疾病的认知增强有关。
本研究结果显示,总体上SCORAD评分与IDQOL、CDLQI和DFI评分存在正相关关系,但就其中的具体问题,除了1~4岁组的SCORAD评分与睡眠和疲劳度评分存在正相关关系外,其余问题均无相关关系。既往研究也表明SCORAD评分与睡眠有明显正相关关系[16-17],本研究结果与之一致。
目前根据疾病的严重程度,选用不同的外用糖皮质激素仍是AD的一线治疗[18]。已知外用糖皮质激素可以明显改善AD严重程度,在临床中广泛应用[19],并且Kubota等[20]也证实外用糖皮质激素和他克莫司软膏序贯治疗AD,随着疾病严重程度的改善生活质量也明显改善,表现为EASI评分明显下降,IDQOL(CDLQI)评分也明显改善。本研究结果也显示,随着AD疾病严重程度的明显改善,总体生活质量也随之明显改善。因此IDQOL、CDLQI和DFI评分作为激素治疗AD的疗效评估有一定的临床意义。
总之,AD对患儿及其家庭生活质量的影响较大,在临床工作中不仅要治疗疾病本身,还要重视患儿和家庭的生活质量评估。采用外用糖皮质激素治疗可有效控制疾病,并改善患儿和家庭的生活质量。
| [1] | Weidinger S, Novak N. Atopic dermatitis[J]. Lancet, 2016, 387 (10023): 1109–1122. DOI:10.1016/S0140-6736(15)00149-X |
| [2] | Guo Y, Ping L, Tang J, et al. Prevalence of atopic dermatitis in Chinese children aged 1-7 ys[J]. Sci Rep, 2016, 6 : 29751. DOI:10.1038/srep29751 |
| [3] | Chernyshov PV. Stigmatization and self-perception in children with atopic dermatitis[J]. Clin Cosmet Investig Dermatol, 2016, 9 : 159–166. DOI:10.2147/CCID |
| [4] | Hill MK, Kheirandish Pishkenari A, Braunberger TL, et al. Recent trends in disease severity and quality of life instruments for patients with atopic dermatitis:A systematic review[J]. J Am Acad Dermatol, 2016, 75 (5): 906–917. DOI:10.1016/j.jaad.2016.07.002 |
| [5] | Jang HJ, Hwang S, Ahn Y, et al. Family quality of life among families of children with atopic dermatitis[J]. Asia Pac Allergy, 2016, 6 (4): 213–219. DOI:10.5415/apallergy.2016.6.4.213 |
| [6] | Pustišek N, Vurnek Živković M, Šitum M, et al. Quality of life in families with children with atopic dermatitis[J]. Pediatr Dermatol, 2015, 33 (1): 28–32. |
| [7] | Sánchezpérez J, Daudéntello E, Mora AM, et al. Impact of atopic dermatitis on health-related quality of life in Spanish children and adults:the PSEDA study[J]. Actas Dermosifiliogr, 2013, 104 (1): 44–52. DOI:10.1016/j.ad.2012.03.008 |
| [8] | Williams HC, Burney PG, Pembroke AC, et al. The U.K. Working Party's Diagnostic Criteria for Atopic Dermatitis. Ⅲ. Independent hospital validation[J]. Br J Dermatol, 1994, 131 (3): 406–416. DOI:10.1111/bjd.1994.131.issue-3 |
| [9] | Oranje AP, Glazenburg EJ, Wolkerstorfer A, et al. Practical issues on interpretation of scoring atopic dermatitis:the SCORAD index, objective SCORAD and the three-item severity score[J]. Br J Dermatol, 2007, 157 (4): 645–648. DOI:10.1111/bjd.2007.157.issue-4 |
| [10] | 中华医学会皮肤性病学分会免疫学组. 中国特应性皮炎诊疗指南(2014版)[J]. 全科医学临床与教育, 2014, 47 (6): 603–606. |
| [11] | Kim DH, Li K, Seo SJ, et al. Quality of life and disease severity are correlated in patients with atopic dermatitis[J]. J Korean Med Sci, 2012, 27 (11): 1327–1332. DOI:10.3346/jkms.2012.27.11.1327 |
| [12] | Ražnatović Djurović M, Janković J, Tomić Spirić V, et al. Health-related quality of life in children with moderate to severe atopic dermatitis[J]. Acta Dermatovenerol Croat, 2015, 23 (3): 178–184. |
| [13] | Al Shobaili HA. The impact of childhood atopic dermatitis on the patients' family[J]. Pediatr Dermatol, 2010, 27 (6): 618–623. DOI:10.1111/pde.2010.27.issue-6 |
| [14] | Chernyshov PV, Kaliuzhna LD, Reznikova AA, et al. Comparison of the impairment of family quality of life assessed by disease-specific and dermatology-specific instruments in children with atopic dermatitis[J]. J Eur Acad Dermatol Venereol, 2015, 29 (6): 1221–1224. DOI:10.1111/jdv.12600 |
| [15] | Chernyshov PV, Ho RC, Monti F, et al. An international multi-center study on self-assessed and family quality of life in children with atopic dermatitis[J]. Acta Dermatovenerol Croat, 2015, 23 (4): 247–253. |
| [16] | Yano C, Saeki H, Ishiji T, et al. Impact of disease severity on sleep quality in Japanese patients with atopic dermatitis[J]. J Dermatol Sci, 2013, 72 (2): 195–197. DOI:10.1016/j.jdermsci.2013.06.010 |
| [17] | Kong TS, Han TY, Lee JH, et al. Correlation between severity of atopic dermatitis and sleep quality in children and adults[J]. Ann Dermatol, 2016, 28 (3): 321–326. DOI:10.5021/ad.2016.28.3.321 |
| [18] | Eichenfield LF, Tom WL, Berger TG, et al. Guidelines of care for the management of atopic dermatitis:Section 2. Management and treatment of atopic dermatitis with topical therapies[J]. J Am Acad Dermatol, 2014, 71 (1): 116–132. DOI:10.1016/j.jaad.2014.03.023 |
| [19] | Wollenberg A, Oranje A, Deleuran M, et al. ETFAD/EADV Eczema task force 2015 position paper on diagnosis and treatment of atopic dermatitis in adult and paediatric patients[J]. J Eur Acad Dermatol Venereol, 2016, 30 (5): 729–747. DOI:10.1111/jdv.2016.30.issue-5 |
| [20] | Kubota Y, Yoneda K, Nakai K, et al. Effect of sequential applications of topical tacrolimus and topical corticosteroids in the treatment of pediatric atopic dermatitis:an open-label pilot study[J]. J Am Acad Dermatol, 2009, 60 (2): 212–217. DOI:10.1016/j.jaad.2008.09.034 |
 2017, Vol. 19
2017, Vol. 19