患儿,女,1岁9个月,因发现甘油三酯升高、面容特殊1年余就诊。1月龄时因呕吐就诊发现甘油三酯升高(18.5 mmol/L),超声显示肝大、肝脏弥漫性病变,诊断为“高脂血症、脂肪肝”,以后多次复查甘油三酯波动在3.7~18 mmol/L;4月龄开始出现特殊体征:全身皮肤黝黑、皮下脂肪缺失、毛发增多、面部呈空双颊、颈部黑棘皮及四肢肌肉肥大。7月龄时因高热查血常规发现中性粒细胞缺乏,以后多次复查均提示粒细胞缺乏。患儿1月龄起停母乳,改深度水解蛋白及中链脂肪酸来源的牛奶喂养,4~6月龄时添加辅食后禁食动物油脂(仅提供少量植物油脂),甘油三酯降至3.5~5.0 mmol/L。中性粒细胞缺乏未予特殊治疗。患儿既往无特殊病史,无过敏史,已进行卡介苗、乙肝疫苗接种。患儿系第4胎第1产,足月顺产出生,出生时无产伤窒息史,出生体重3.2 kg,其母第1胎为药物流产,第2、3胎均为妊娠2个月时宫内发育停止。父母非近亲婚配,其母有甲醛接触史,第4胎备孕期间服用免疫抑制剂6月余(具体用药不详),否认家族遗传病史。
入院时查体:T 37.0℃、P 100次/min、R 28次/min、体重12.6 kg。神清,全身皮肤黝黑、皮下脂肪缺失、弹性稍差,毛发多,颈部黑棘皮,浅表淋巴结无肿大,空双颊,扁桃体I度肿大,无脓性分泌物。肝脏约肋下3 cm,脾脏未触及。心肺无异常。四肢肌肉肥大。神经系统检查无异常。
辅助检查:血常规中性粒细胞0.28×109/L,余项均正常。甘油三酯正常,复测仍正常;胆固醇、高密度脂蛋白、低密度脂蛋白、肝肾功能、电解质、心肌酶、降钙素原、血沉、免疫全套、铜蓝蛋白、大小便常规均无异常。CRP 22.1 mg/L(参考值:0~3 mg/L)。糖化血红蛋白HbA1c、HbA1基本正常;胰岛素55.1 μIU/mL(参考值2.6~24.9 μIU/mL);C肽6.82 ng/mL(参考值:1.1~4.4 ng/mL);血糖正常,尿糖阴性。中性粒细胞爆发试验:中性粒细胞活化率79.9%(参考值:> 90%)。肺炎支原体DNA、EB病毒DNA均阴性。T淋巴细胞亚群正常。中性粒细胞肾上腺素激发试验阴性。腹部彩超:肝上界第6肋间、肋下20 mm,肝表面光滑,实质回声分布均匀;脾厚25 mm、肋下(-),实质回声分布均匀;双肾形态规则,轮廓清晰,大小正常;肝门部及腹腔内可见多个低回声结节,边界清晰,分布欠均匀,较大者约25×15 mm,位于肝门部。颈部彩超:双侧颈部多个低回声结节,考虑肿大淋巴结。骨髓细胞学:增生明显活跃、部分粒细胞可见中毒颗粒;巨核细胞多见,血小板成堆分布;铁染色示铁利用障碍。
2 诊断思维1岁9个月,女性患儿,新生儿期即发现高甘油三酯血症,伴逐渐出现的特殊体征:全身皮肤黝黑、皮下脂肪消失,颈部黑棘皮,毛发增多、浓密,面部呈空双颊,四肢肌肉肥大,以及肝大、中性粒细胞缺乏。高甘油三酯血症是指甘油三酯含量超过1.7 mmol/L,分为原发性和继发性两种。原发性系由于遗传缺陷或与环境因素如饮食习惯、生活方式等相互作用引起,多见于儿童、青少年。继发性往往可以找到明确的系统疾病或者代谢综合征、肥胖/超重、药物等原因,以成人多见。本例患儿新生儿期起病,无继发因素,原发性可能性大,需注意遗传因素导致的脂肪代谢性疾病。脂肪代谢性疾病分为先天性全身脂肪营养不良(congenital generalized lipodystrophy, CGL)、获得性全身脂肪营养不良(acquired generalized lipodystrophy, AGL)以及家族性部分脂肪营养不良(familial partial lipodystrophy, FPLD)、获得性部分脂肪营养不良(acquired partial lipodystrophy, APL)。部分性脂肪营养不良(FPLD、APL)为区域性的脂肪萎缩,非萎缩部位的脂肪细胞异常增生或肥大。而本例患儿全身皮下脂肪基本消失。全身性脂肪营养不良(CGL、AGL)主要表现为:生后不久出现的广泛皮下脂肪缺乏、肌肉组织逐渐肥大,并逐渐出现多毛、黑棘皮、肝大及代谢紊乱,其中获得性全身脂肪营养不良与感染及自身免疫相关。本例患儿新生儿期发现高甘油三酯血症,逐渐全身皮下脂肪消失、四肢肌肉肥大,符合全身性脂肪营养不良特点,患儿无明确感染因素,且免疫球蛋白正常,淋巴细胞亚群正常,无反复感染、皮肤病变、关节肿痛等自身免疫疾病相关的临床表现,无获得性全身脂肪营养不良依据;先天性全身脂肪营养不良为常染色体隐性遗传,已经发现的致病基因有AGPAT2、BSCL2、CAV1、PTRF,进一步行基因检测有助诊断。
本研究患儿高甘油三酯血症合并中性粒细胞减少,病程长达14个月,经临床随访、中性粒细胞肾上腺素刺激试验、相关病原微生物、营养素、骨髓及免疫等检查不支持假性和获得性中性粒细胞减少,需行先天性中性粒细胞减少症相关基因检测寻找病因。
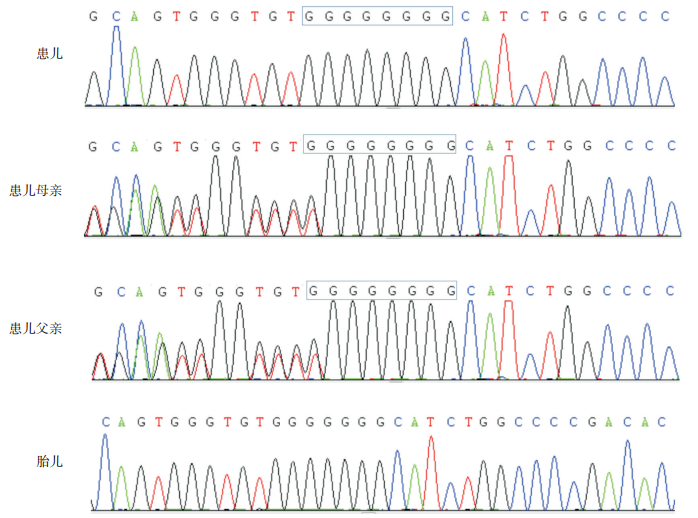
3 进一步检查征得患儿家属同意后,取患儿及其父母外周静脉血(EDTA抗凝),提取DNA,进行单基因病全外显子组测序分析及全基因组基因拷贝数变异(copy number variations CNV)检测。结果显示,患儿存在BSCL2基因(位于11号染色体)移码突变:c.974(外显子7)_c.975(外显子7)insG,p.G325Gfs*13(NM_001122955);患儿父母均为该位点的杂合子。见图 1。CNV检测无异常。未发现与中性粒细胞减少相关的基因变异。
|
图 1 患儿及其家系的BSCL2基因测序结果 患儿BSCL2基因存在c.974(外显子7)_c.975(外显子7)insG纯合突变,患儿父母均为该位点的杂合子。胎儿为c.974_c.975野生型(图中框内为突变位点)。 |
由于该基因突变引起的先天性全身脂肪营养不良为常染色体隐性遗传,故对其母亲再次受孕后的胎儿行产前诊断,胎龄20周时行羊膜腔穿刺,取羊水进行细胞培养,提取DNA,行BSCL2基因编码区974_975位点测序,结果显示胎儿为c.974(外显子7)_c.975(外显子7)野生型(图 1),属正常表型。
4 诊断及依据诊断:先天性全身脂肪营养不良(CGL)。依据:(1)新生儿期即发现甘油三酯升高,逐渐出现特殊体征:毛发多,全身皮下脂肪缺失,空双颊,颈部黑棘皮,四肢肌肉肥大;(2)无继发性全身脂肪营养不良依据;(3)禁食动物油脂后甘油三酯恢复正常;(4)BSCL2基因存在已报道的CGL致病突变:c.974(外显子7)_c.975(外显子7)insG,p.G325Gfs*13(NM_001122955),其父母均为杂合子突变。
5 临床经过确诊后患儿予以中链脂肪酸、深度水解蛋白奶粉喂养,辅食中禁食动物油脂,植物油脂控制在1~2 mL/d。定期随访至2018年6月(2岁半),患儿血脂保持正常,中性粒细胞仍缺乏(< 0.5×109/L),体征无明显变化。
6 讨论先天性全身脂肪营养不良(CGL)为罕见的常染色体隐性遗传的系统性疾病,发病率约为1/1 000万,男女比例1 : 1,是由Berardinelli和Seip首先报道,故也称Berardinelli-Seip综合征(BSS)[1-4]。目前已发现与CGL相关的4种基因:分别是位于染色体9q34的AGPAT2和位于11q13的BSCL2、CAV1、PTRF,分别导致4种类型的CGL(CGL1、CGL2、CGL3、CGL4)[5]。95%的CGL病例由AGPAT2或BSCL2基因突变所致。BSCL2基因突变呈现多样化,目前报道的突变类型有错义突变、插入突变、缺失突变、衔接突变以及复杂重排等5种,以错义或者无义突变最为常见[6]。本研究病例发现的BSCL2基因移码突变为劳文芹等[7]已报道的突变,故可确诊为CGL。
BSCL2基因突变所致的CGL病情最严重,具有代谢活性的脂肪组织和机械脂肪组织全部缺失,智力障碍及早期死亡的发生率高[8]。BSCL2基因编码的seipin蛋白参与脂肪细胞分化、脂滴形成,并维持脂滴形态、限制脂滴在非脂肪细胞合成及沉积,BSCL2基因突变可破坏seipin蛋白的N-糖基化位点,导致蛋白质的错误折叠及神经元变性,进而引起一系列脂肪代谢障碍表现[9]。CGL临床表现为生后不久即出现的高甘油三酯血症,部分患者同时存在高胆固醇血症,全身皮下脂肪消失、黑棘皮,脂肪异位沉积于肝脏导致的肝肿大、脂肪肝,脂肪沉积于骨骼肌导致的四肢肌肉肥大,以及胰岛素抵抗、高胰岛素血症、糖尿病、心肌肥厚等[10];部分患者儿童期可出现食欲亢进,生长加速,甲状腺功能正常的高代谢状态,以及性早熟、骨龄提前、智力低下等,女童可有多毛、阴蒂肥大表现;青春期女性患者可有月经不规律等多囊卵巢的表现[11-12]。本研究患儿生后1个月即发现甘油三酯升高,并逐渐出现全身皮下脂肪消失、黑棘皮、多毛以及四肢肌肉肥大、肝大等表现,临床特点与文献相符。本研究患儿有胰岛素及C肽增高,但血糖、尿糖均正常,无胰岛素抵抗及高胰岛素血症等临床表现,是否进一步发展有待随访观察。另外、患儿的单基因病全外显子测序和CNV检测结果未发现先天性中性粒细胞减少相关基因变异,查阅国内外文献,既往的CGL患者没有合并中性粒细胞减少的报道,故本例患儿合并的中性粒细胞减少原因不明。
CGL目前尚无特效治疗。饮食控制是最重要的手段:低脂、低热量饮食,增加中链三酰甘油和鱼油的摄入有助于改善肝功能和降低血脂,延缓糖尿病发生。婴幼儿阶段的喂养更是面临挑战,婴儿期建议采用中链脂肪酸来源的牛奶喂养,或深度水解蛋白牛奶,添加辅食后可食用少量植物菜籽类油脂。糖尿病、高脂血症和脂肪肝是CGL治疗的难点。严重高甘油三酯血症的患儿可采用苯氧酸类药物治疗,非高密度脂蛋白胆固醇升高的患儿可加用低剂量他汀类药物。已经发生糖尿病者可应用胰岛素治疗,但对于具有胰岛素抵抗的糖尿病患者的胰岛素治疗有争议,二甲双胍为首选[1, 13]。胰岛素增敏剂罗格列酮可降低甘油三酯、糖化血红蛋白、增加体脂,但在儿童中的应用仍需观察[14]。有研究[15]表明瘦素能够显著降低三酰甘油水平,改善胰岛素抵抗,并抑制食欲,降低空腹血糖和糖化血红蛋白水平。美国国立卫生研究院推荐使用美曲普汀(重组人瘦素类似物)皮下注射(每日0.06~0.24 mg/kg)改善胰岛素敏感性[16]。本研究患儿胆固醇正常,未予以他汀类药物治疗;虽然胰岛素及糖化血红蛋白有增高,但血糖、尿糖均正常,无胰岛素使用指征,仅予以饮食控制。
CGL预后不佳,多数在青年期或中年期死亡,死亡原因多为肝肾功能衰竭、心脏骤停、糖尿病肾病、糖尿病视网膜病变等,肝硬化食道静脉曲张破裂出血也是主要死因[17]。本例患儿确诊后,一直予以饮食控制,目前患儿随访半年余,甘油三酯正常。
7 结语先天性全身脂肪营养不良临床罕见,与AGPAT2、BSCL2、CAV1、PTRF等基因突变有关,是一种常染色体隐性遗传病,表现为新生儿期出现的全身皮下脂肪消失、四肢肌肉肥大和一系列代谢紊乱:如高甘油三酯、高胰岛素血症、高血糖等。本研究患儿表现为新生儿期生后不久即出现的甘油三酯升高、全身皮下脂肪消失,经基因检测确诊为CGL,但中性粒细胞缺乏暂无法证明与该病有关。而且患儿母亲再次妊娠20周时行胎儿羊水脱落细胞基因检测无异常,生产健康男婴。因此,对于新生儿期出现的高甘油三酯血症,需考虑先天性全身脂肪营养不良,基因检测有助于确诊并指导母亲优生优育。
| [1] |
Schott M, Scherbaum WA, Bornstein SR. Acquired and inherited lipodystrophies[J]. N Engl J Med, 2004, 351(1): 103-104. DOI:10.1056/NEJM200407013510121 (  0) 0) |
| [2] |
Kazandjieva J, Guleva D, Marina S, et al. Berardinelli-Seip syndrome-A case report[J]. Serbian J Dermatol Venereol, 2016, 8(2): 101-104. (  0) 0) |
| [3] |
Berardinelli W. An undiagnosed endocrinometabolic syndrome:report of 2 cases[J]. J Clin Endocrinol Metab, 1954, 14(2): 193-204. DOI:10.1210/jcem-14-2-193 (  0) 0) |
| [4] |
Seip M. Lipodystrophy and gigantism with associated endocrine manifestations. A new diencephalic syndrome[J]. Acta Paediatrica, 1959, 48: 555-574. (  0) 0) |
| [5] |
刘国庆, 崔鑫, 谢元. Seipin与先天性全身脂肪营养不良[J]. 重庆医科大学学报, 2013, 38(1): 1-4. DOI:10.3969/j.issn.0253-3626.2013.01.001 (  0) 0) |
| [6] |
张梦奇, 马明圣, 邱正庆. BSCL2基因突变致先天性全身脂肪营养不良症1例报告并文献复习[J]. 临床儿科杂志, 2017, 35(7): 532-536. DOI:10.3969/j.issn.1000-3606.2017.07.015 (  0) 0) |
| [7] |
劳文芹, 孟哲, 欧辉, 等. 儿童Berardinelli-Seip综合征2例报告[J]. 中国实用儿科杂志, 2016, 31(2): 157-158. (  0) 0) |
| [8] |
Haque WA, Shimomura I, Matsuzawa Y, et al. Serum adiponectin and leptin levels in patients with lipodystrophies[J]. J Clin Endocrinol Metab, 2002, 87(5): 2395. DOI:10.1210/jcem.87.5.8624 (  0) 0) |
| [9] |
Windpassinger C, Auer-Grumbach M, Irobi J, et al. Heterozygous missense mutations in BSCL2 are associated with distal hereditary motor neuropathy and Silver syndrome[J]. Nat Genetics, 2004, 36(3): 271-276. DOI:10.1038/ng1313 (  0) 0) |
| [10] |
袁欣, 陈瑞敏, 王剑, 等. 先天性全身性脂肪营养不良BSCL2基因突变1例并文献复习[J]. 中国循证儿科杂志, 2016, 11(5): 377-381. DOI:10.3969/j.issn.1673-5501.2016.05.013 (  0) 0) |
| [11] |
Shawky RM, Gamal R, Seifeldin NS. Berardinelli-Seip syndrome type 2-An Egyptian child[J]. Egyptian J Med Human Genet, 2015, 16: 189-193. DOI:10.1016/j.ejmhg.2014.08.004 (  0) 0) |
| [12] |
Garg A, Misra A. Lipodystrophies:rare disorders causing metabolic syndrome[J]. Endocrinol Metab Clin North Am, 2004, 33(2): 305-331. DOI:10.1016/j.ecl.2004.03.003 (  0) 0) |
| [13] |
RichardE, RobertM, HalB. 尼尔逊儿科学[M]. 第16版. , 科学出版社, 2001: 2018.
(  0) 0) |
| [14] |
赵诸慧, 沈水仙, 支涤静, 等. 儿童全身性脂肪营养不良伴糖尿病1例报告[J]. 临床儿科杂志, 2006, 24(12): 1013-1014. DOI:10.3969/j.issn.1000-3606.2006.12.027 (  0) 0) |
| [15] |
Oral EA, Simha V, Ruiz E, et al. Leptin-replacement therapy for lipodystrophy[J]. N Engl J Med, 2002, 346(8): 570-578. DOI:10.1056/NEJMoa012437 (  0) 0) |
| [16] |
Patni N, Garg A. Congenital generalized lipodystrophies--new insights into metabolic dysfunction[J]. Nat Rev Endocrinol, 2015, 11(9): 522-534. DOI:10.1038/nrendo.2015.123 (  0) 0) |
| [17] |
蒋优君, 梁黎, 董关萍, 等. 先天性全身性脂肪营养不良一例[J]. 中华儿科杂志, 2004, 42(12): 959. DOI:10.3760/j.issn:0578-1310.2004.12.034 (  0) 0) |
 2018, Vol. 20
2018, Vol. 20


