2. 华中科技大学同济医学院附属武汉儿童医院内分泌科, 湖北 武汉 430016
随着经济发展及生活水平的改善,学龄前期儿童肥胖症的发病率逐年升高。我国儿童期单纯性肥胖研究协作组[1]发现,我国0~6岁儿童肥胖检出率高达7.2%,已接近欧美国家水平。学龄期超重、肥胖儿童以及肥胖成人均存在心脏自主神经功能受损,发生心血管疾病的风险增高[2-4]。心率减速力(deceleration capacity of rate, DC)及心率变异性(heart rate variability, HRV)是反映心脏自主神经功能的常用指标。维生素D(VitD)是人体不可缺少的脂溶性必需维生素,有研究[5]发现34%的肥胖儿童伴有VitD缺乏。VitD缺乏与肥胖,心血管疾病,代谢性疾病,内分泌疾病及儿童肿瘤有着密切的联系[6-8]。学龄前期儿童处于脂肪重聚期且生长发育较为迅速,极易发生肥胖伴VitD缺乏。目前暂无VitD不足或缺乏与学龄前期肥胖儿童心脏自主神经功能关系的研究。本研究拟采用DC及HRV评估VitD缺乏和不足的学龄前期肥胖儿童的心脏自主神经功能状态,探讨VitD缺乏和不足对心脏自主神经功能的影响。
1 资料与方法 1.1 研究对象将2014年1月至2017年12月武汉儿童医院就诊并进行了25-羟基维生素D测定的242例学龄前期(3~ < 6岁)单纯性肥胖儿童作为研究对象。单纯性肥胖诊断参照文献[9]即体重指数(body mass index, BMI)超过中国0~18岁儿童肥胖筛查的BMI界值。排除标准:①神经内分泌疾病、遗传性疾病、肾脏肾上腺疾病、代谢性疾病等引起的继发性肥胖;②伴有先天性心脏病、心肌病、川崎病等器质性心脏疾病;③伴有血压、血脂、血糖等异常;④动态心电图异常,如期前收缩、传导阻滞、快速性心律失常等;⑤近期无用药史。
根据VitD水平分为VitD缺乏组、VitD不足组及VitD充足组。VitD充足组83例(男39例、女44例,平均年龄4.9±1.0岁,BMI 21.1±1.5 kg/m2);VitD不足组83例(男39例、女44例,平均年龄4.6±1.1岁,BMI 21.1±1.6 kg/m2);VitD缺乏组76例(男35例、女41例,平均年龄4.1±1.0岁,BMI 21.2±1.6 kg/m2)。三组间年龄(F=2.73,P=0.067)、BMI(F=0.10,P=0.904)以及性别比例(χ2=0.014,P=0.906)的差异无统计学意义。
1.2 BMI测定由专人测量患儿的身高及体重。身高精确到0.01 m,体重精确到0.1 kg。
BMI(kg/m2)=体重/身高2。
1.3 25-羟基维生素D测定采用Roch cobas8000 e602仪器,用色谱法测定患儿血清25-羟基VitD。VitD是否充足参照文献[9-10]判定:10~19 ng/mL为VitD缺乏,20~29 ng/mL为VitD不足,30~100 ng/mL为VitD充足。
1.4 HRV、DC和AC的测定所有患儿均采用美国DMS公司的Version 12.5十二导同步动态心电图仪进行动态心电图检查,检查时间不低于24 h。使用动态心电图分析系统对心电图数据进行分析,自动计算出DC、心率加速力(acceleration capacity of rate, AC)及HRV各指标数值。
HRV是指窦性心率逐次心动周期的时间变异数,包含时域和频域指标。HRV时域指标包括:RR间期总体标准差(standard deviation of normal-to-normal R-R intervals, SDNN)、RR间期平均值的标准差(standard deviation of the average normal-to-normal intervals, SDANN)、相邻RR间期差值的均方根(root mean square of successive differences, RMSSD);HRV频域指标包括低频功率(low-frequency power, LF)和高频功率(high-frequency power, HF)。
DC值检测[11]:使用500 HZ数字化自动处理系统将动态心电图转化为以心动周期RR间期值为纵坐标的序列图。每个心动周期的RR值较前一个心动周期延长者称为减速周期(当实测的RR值比前一个心动周期值延长后缩短超过5%时,该周期则将被自动删除)。以每个减速点为心率段的中心点,依次将其双侧的20个心动周期组成一个心率段,对不同心率段进行有序排列。经位相整序后,计算对应周期的平均值X(i),再将结果代入公式计算DC值。DC=[X(0)+X(1)-X(-1)-X(-2)]×1/4。X(0)为所有中心点RR间期的平均值,X(1)为中心点右侧紧邻的第1个心动周期的平均值,X(-1)为中心点左侧紧邻的第1个心动周期的平均值,X(-2)为中心点左侧第2个所有心动周期的平均值。计算结果为正值用DC表示,负值则用AC表示。
1.5 统计学分析采用SPSS 17.0软件进行数据处理。计量资料以均数±标准差(x±s)表示,多组间比较采用单因素方差分析,组间两两比较采用SNK-q检验。相关性分析采用Pearson相关性检验。P < 0.05表示差异具有统计学意义。
2 结果 2.1 三组间DC,AC,HRV的比较VitD不足、缺乏组的DC、RMSSD、LF低于VitD充足组,以缺乏组最低,差异均具有统计学意义(P < 0.05);VitD不足、缺乏组的AC值高于充足组,以缺乏组最高,差异均具有统计学意义(P < 0.05);VitD缺乏组的SDNN和HF低于充足组(P < 0.05),但不足组与充足组间的差异无统计学意义(P > 0.05)。见表 1。
| 表 1 VitD缺乏组、不足组及充足组间DC、AC、HRV的比较 (x±s) |
|
|
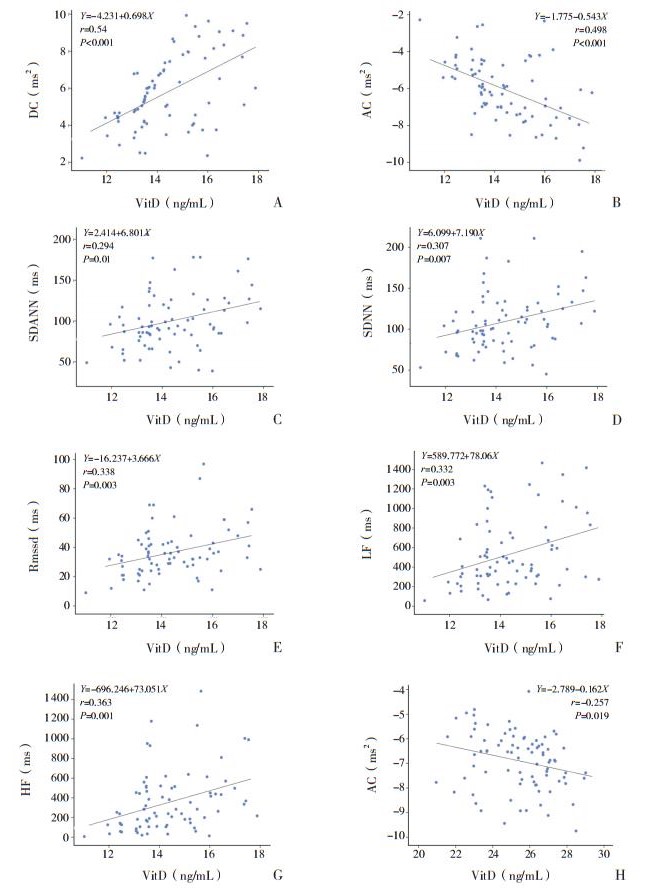
VitD缺乏组的VitD水平与DC呈正相关(r=0.54),与SDNN呈正相关(r=0.307),与SDANN呈正相关(r=0.294),与RMSSD呈正相关(r=0.338),与LF呈正相关(r=0.332),与HF呈正相关(r=0.363),与AC呈负相关(r=-0.498),P < 0.05;不足组的VitD水平与AC呈负相关(r=-0.257,P < 0.05)。见图 1。
|
图 1 VitD缺乏组或不足组的VitD与DC、AC及HRV的相关性 A~G为VitD缺乏组;H为VitD不足组。注:[DC]心率减速力;[AC]心率加速力;[SDNN]RR间期总体标准差;[SDANN]RR间期平均值的标准差;[RMSSD]相邻RR间期差值的均方根;[LF]低频功率;[HF]高频功率。 |
25-羟基维生素D是VitD的活性形式之一,可反映体内VitD的水平[12]。学龄前期儿童因奶制品摄入减少,易出现VitD缺乏。而且学龄前期是儿童肥胖症发生的主要年龄阶段[13]。VitD是脂溶性维生素,肥胖儿童大量的VitD储存在脂肪组织中,使得血液循环中的VitD浓度及生物利用度下降。因此VitD水平与肥胖程度呈负相关[14]。心脏自主神经包括心脏迷走神经和交感神经。清醒安静状态及睡眠状态时迷走神经对心脏的调节占优势;运动状态时,迷走神经张力减弱,交感神经张力相对增强,使心率增快。所以迷走神经是心脏的减速神经,其功能减弱对患儿的危害性大于交感神经兴奋性增高[11]。DC及HRV是反映心脏自主神经功能的常用指标,DC、RMSSD和HF反映心脏迷走神经的张力,当心脏迷走神经张力减弱或活性降低时,DC下降,保护作用下降,发生心血管疾病及猝死的风险增高;SDANN和LF反映心脏交感神经的张力,交感神经张力增强时,AC增强。SDNN则反映心脏交感神经与迷走神经的平衡状态[11]。
易兰芬等[2]发现学龄期肥胖儿童自主神经功能受损,主要表现为迷走神经张力减弱。本研究患儿的DC、RMSSD、LF以VitD缺乏组最低,AC以VitD缺乏组最高,其中VitD不足组的DC、RMSSD、LF低于VitD充足组,AC高于VitD充足组;VitD缺乏组的SDNN和HF低于VitD充足组,提示VitD不足或者缺乏的肥胖儿童迷走神经和交感神经张力均有所减弱,而缺乏组迷走神经张力减弱或活性降低更为明显,对心脏的保护作用也将进一步降低,患儿发生心律失常及心源性疾病甚至猝死的风险也进一步增高。本研究还发现,VitD缺乏组的VitD水平与DC和HRV呈正相关,与AC呈负相关;而VitD不足组的VitD水平仅与AC呈负相关,表明学龄前期肥胖儿童的VitD不足时,仅心脏交感神经张力随VitD水平降低而减弱;VitD缺乏时,则心脏迷走神经的张力随VitD降低而降低,且VitD浓度越低心脏迷走神经功能越弱,发生心血管事件的风险也越高。结合VitD的特性及VitD与肥胖的关系,考虑学龄前期肥胖患儿出现心脏自主神经功能障碍的原因可能是:①VitD是体内瘦素(leptin, LP)合成不可缺少的成分,而LP可以激活交感神经,使血液中去甲肾上腺素增加。因此VitD缺乏导致LP水平降低、交感神经活性减弱[15]。②VitD缺乏使肥胖患者胰岛β细胞的L型钙通道关闭,胰岛素受体底物磷酸化受阻,使胰岛素的合成和分泌减少,VitD缺乏还可加重胰岛素抵抗[16]。VitD对胰岛素的双重影响导致心脏自主神经功能紊乱。③肥胖儿童处于慢性炎症、缺血缺氧状态,VitD缺乏可使炎症反应过度持续,影响心脏自主神经功能。④VitD依赖性钙调节蛋白广泛分布于中枢及周围神经系统[17],它通过与VitD结合而发挥作用,因此VitD缺乏可影响神经递质合成、神经营养因子和蛋白质的表达,直接导致心脏自主神经功能紊乱。
综上所述,VitD不足或缺乏的学龄前期肥胖患儿均存在不同程度的心脏自主神经功能障碍。对于肥胖儿童应注意是否合并VitD缺乏,积极检测其DC和HRV,以及时发现其心血管病风险。
| [1] |
李辉, 季成叶, 宗心南, 等. 中国0-18岁儿童青少年体块指数的生长曲线[J]. 中华儿科杂志, 2009, 47(7): 493-498. DOI:10.3760/cma.j.issn.0578-1310.2009.07.004 (  0) 0) |
| [2] |
易兰芬, 文红霞, 黄小力, 等. 学龄期肥胖儿童心脏自主神经功能分析[J]. 中国当代儿科杂志, 2017, 19(5): 524-528. (  0) 0) |
| [3] |
王小凤, 张巍, 杨建国, 等. 高血压伴肥胖患者心率变异性和超敏C蛋白的分析[J]. 临床荟萃, 2014, 29(4): 442-445. DOI:10.3969/j.issn.1004-583X.2014.04.028 (  0) 0) |
| [4] |
黄小力, 文红霞, 易兰芬, 等. 超重、肥胖儿童与代谢综合症患儿心率减速力的研究[J]. 临床儿科杂志, 2017, 32(10): 725-728. DOI:10.3969/j.issn.1000-3606.2017.10.002 (  0) 0) |
| [5] |
Turer CB, Lin H, Flores G. Prevalence of vitamin D deficiency among overweight and obese US children[J]. Pediatrics, 2013, 131(1): e152-e161. DOI:10.1542/peds.2012-1711 (  0) 0) |
| [6] |
Kuroda M, Sakaue H. Role of vitamin D and calcium in obesity and type 2 diabetes[J]. Clin Calcium, 2016, 26(3): 349-354. (  0) 0) |
| [7] |
Aguirre M, Manzano M, Salas Y, et al. Vitamin D deficiency in patients admitted to the general ward with breast, lung, and colorectal cancer in Buenos Aires, Argentina[J]. Arch Osteoporos, 2016, 11: 4. DOI:10.1007/s11657-015-0256-x (  0) 0) |
| [8] |
Desai CK, Huang J, Lokhandwala A, et al. The role of vitamin supplementation in the prevention of cardiovascular disease events[J]. Clin Cardiol, 2014, 37(9): 576-581. (  0) 0) |
| [9] |
Holick MF. Vitamin D deficiency[J]. N Engl J Med, 2007, 357(3): 266-281. DOI:10.1056/NEJMra070553 (  0) 0) |
| [10] |
Bischoff-Ferrari HA, Giovannucci E, Willett WC, et al. Estimation of optimal serum concentrations of 25-hydroxy vitamin D for multiple health outcomes[J]. Am J Clin Nutr, 2006, 84(1): 18-28. DOI:10.1093/ajcn/84.1.18 (  0) 0) |
| [11] |
郭继鸿. 心率减速力检测[J]. 临床心电学杂志, 2009, 18(1): 59-68. DOI:10.3969/j.issn.1005-0272.2009.01.019 (  0) 0) |
| [12] |
Holick MF. Resurrection of vitamin D deficiency and rickets[J]. J Clin Invest, 2006, 116(8): 2062-2072. DOI:10.1172/JCI29449 (  0) 0) |
| [13] |
曲文君, 孙瑾, 倪波. 大连市7岁以下儿童单纯性肥胖检出率及影响因素分析[J]. 中国儿童保健杂志, 2015, 23(2): 206-209. (  0) 0) |
| [14] |
孙薇. 肥胖儿童维生素D缺乏与糖脂代谢、胰岛素抵抗的关系研究[J]. 海南医学院学报, 2016, 22(13): 1438-1441. (  0) 0) |
| [15] |
Menendez C, Lage M, Peino R, et al. Retinoic acid and vitamin D(3) powerfully inhibit in vitro leptin secretion by human adipose tisse[J]. J Endocrinol, 2001, 170(2): 425-431. DOI:10.1677/joe.0.1700425 (  0) 0) |
| [16] |
Wang L, Wang H, Wen H, et al. Relationship between HOMAIR and serum vitamin D in Chinese children and adolescents[J]. J Pediatr Endocrinol Metab, 2016, 29(7): 777-781. (  0) 0) |
| [17] |
Soni M, Kos K, Lang IA, et al. Vitamin D and cognitive function[J]. Scand J Clin Lab Invest Suppl, 2012, 243: 79-82. (  0) 0) |
 2018, Vol. 20
2018, Vol. 20


