脓毒症(sepsis)是指各种病原体严重感染导致的、伴有器官功能障碍表现的临床综合征,同时伴或不伴乳酸血症[1];新生儿败血症(neonatal sepsis)则专指细菌或真菌严重感染导致的新生儿脓毒症[2],其发病率和病死率均较高,是新生儿时期死亡的第三大原因,尤其是在发展中国家[3-4]。血乳酸(serum lactate)作为反映微循环障碍的敏感指标,近来较多地用于判断疾病的严重程度和预后,并且认为动态监测血乳酸尤其是乳酸清除率,对于评估疾病预后更有价值[5]。然而,目前报道乳酸水平与新生儿败血症预后关系的研究较少,其病例数较少,且仅为定性结论,即乳酸水平可以作为判断新生儿败血症预后的早期指标[6]。本研究拟探讨患儿入院时乳酸水平及24 h内乳酸清除率与新生儿败血症预后的关系,并计算血乳酸判断不良预后的临界值及敏感性、特异性,以指导早期干预治疗。
1 资料与方法 1.1 研究对象选取2017年8月至2018年2月重庆医科大学附属儿童医院新生儿中心收治的301例新生儿败血症患儿为研究对象,其中男187例,女114例;发病中位日龄为0 d(范围0~32 d);早产儿45例,足月儿256例;存活277例,死亡24例。
1.2 诊断标准新生儿败血症的诊断参照中华医学会2003年修订的新生儿败血症诊疗方案中的诊断标准[7]。(1)确定诊断:具有临床表现并符合下列任一条:①血培养或无菌体腔内培养出致病菌;②如果血培养标本培养出条件致病菌,则必须与另次(份)血、无菌体腔内或导管头培养出同种细菌。(2)临床诊断:具有临床表现且具备以下任一条:①非特异性检查≥2条;②血标本病原菌抗原或DNA检测阳性。
存在微循环障碍的判断标准:皮肤大理石花纹、肢端凉、毛细血管充盈时间 > 3 s[8]。
1.3 纳入标准和排除标准纳入标准:(1)符合新生儿败血症的诊断标准[7];(2)入院即完善血乳酸检测(即动脉血气分析)。
排除标准:(1)严重先天性畸形;(2)窒息、肝脏疾病、肾衰竭、恶性肿瘤、药物中毒、糖尿病及先天性代谢疾病等引起动脉血乳酸水平增高的情况。
1.4 分组根据患儿入院时动脉血乳酸水平分为乳酸正常组(52例,< 2 mmol/L)、轻度升高组(218例,2~6 mmol/L)、重度升高组(31例,> 6 mmol/L)[9-10];根据预后分为预后良好组(262例,好转并不遗留后遗症)和预后不良组(39例,包含死亡、脑积水、支气管肺发育不良、视网膜病变等后遗症);根据胎龄分为足月儿组(256例)和早产儿组(胎龄 < 32周20例,胎龄≥32周25例);根据发病时间分为早发败血症组(249例,出生3 d内发病)和晚发败血症组(52例,出生3 d后发病)[11]。
1.5 资料收集收集患儿临床资料,包括患儿性别、发病日龄、胎龄、体重、有无微循环障碍、入院时血乳酸水平、24 h内血乳酸水平、C反应蛋白(CRP)、降钙素原(PCT)、转归、住院天数、抗生素使用时间、呼吸机使用情况等;并计算24 h内乳酸清除率[乳酸清除率=(入院时动脉血乳酸水平-治疗24 h血乳酸水平)/入院时血乳酸水平]×100%[5]。
1.6 统计学分析采用SPSS 22.0软件包进行数据处理,符合正态分布的计量资料采用均数±标准差(x±s)表示,两个独立样本组间比较采用成组t检验,多组间比较使用单因素方差分析,两两比较采用SNK法。非正态分布的计量资料采用中位数及四分位数间距[P50(P25,P75)]表示,两个独立样本的组间比较采用Kolmogorov-Smirnov检验,多组间比较使用Kruskal-Wallis检验。计数资料用例数和百分率(%)表示,组间比较采用χ2检验或Fisher精确概率检验;组间两两比较进行卡方分割检验,调整检验水准为0.017。采用多因素logistic回归分析评估影响新生儿败血症预后的危险因素,绘制ROC曲线并计算曲线下面积,确定临界值。P < 0.05为差异有统计学意义。
2 结果 2.1 不同乳酸水平患儿临床资料的比较在足月儿早发败血症患儿中,不同乳酸水平各组间性别、体重、胎龄、发病日龄方面比较差异无统计学意义(P > 0.05),见表 1,但病死率比较差异有统计学意义(P < 0.05),其中乳酸重度升高组病死率高于乳酸轻度升高组和乳酸正常组(P < 0.017),见表 2。足月儿晚发败血症组乳酸重度升高只有1例,故不宜分组进行统计学分析。早产儿不同乳酸水平各组间性别、体重、胎龄、发病日龄及病死率等的比较差异均无统计学意义(P < 0.05),见表 3、4。
| 表 1 足月儿早发败血症不同乳酸水平组基本资料的比较 |
|
|
| 表 2 足月儿早发败血症不同乳酸水平组患儿临床资料的比较 |
|
|
| 表 3 早产儿败血症不同乳酸水平组基本资料的比较 |
|
|
| 表 4 早产儿败血症不同乳酸水平组患儿临床资料的比较 |
|
|
在足月儿中,不同预后各组间患儿性别、体重、胎龄、发病日龄等基本资料的比较差异无统计学意义(P > 0.05),见表 5,但预后不良组入院时微循环障碍率、血乳酸水平、呼吸机使用率较预后良好组明显升高,差异有统计学意义(P < 0.05),见表 6。在45例早产儿中,由于进行预后良好和预后不良分组后,各组病例数较少,故未对早产儿预后进行分组统计分析。
| 表 5 足月儿不同预后患儿基本资料的比较 |
|
|
| 表 6 足月儿不同预后组患儿临床资料的比较 |
|
|
足月儿中共59例患儿在入院24 h内再次检测动脉血乳酸水平,其中预后良好组和不良组间性别、体重、胎龄、发病日龄的比较差异无统计学意义(P > 0.05);两组24 h乳酸清除率的比较差异也无统计学意义(P > 0.05),见表 7。
| 表 7 足月儿不同预后组患儿乳酸清除率的比较 |
|
|
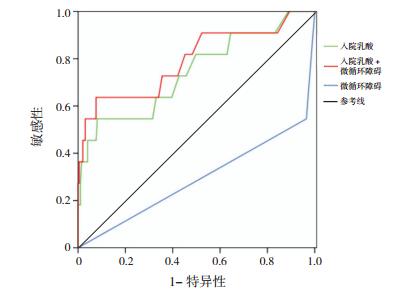
对入院乳酸、有微循环障碍、入院乳酸结合微循环障碍进行ROC曲线分析,显示上述指标在判断新生儿败血症不良预后的曲线下面积分别为为0. 741、0.290、0.792(表 8、图 1)。
| 表 8 各项指标判断新生儿败血症预后不良的ROC曲线分析 |
|
|
|
图 1 各项指标判断预后不良的ROC曲线 |
根据约登指数评估入院乳酸水平的临界值,其最大约登指数0.464对应的入院乳酸水平为6.15 mmol/L,即入院乳酸水平判断新生儿败血症不良预后的临界值为6.15 mmol/L,其对应的敏感性为0.545,特异性为0.919;入院乳酸及微循环障碍二者结合所对应的敏感性为0.636,特异性为0.924。
3 讨论新生儿败血症是新生儿死亡的重要原因[12]。临床上常用CRP、PCT等炎症指标来诊断并评估患儿的病情严重程度[13-14],但其各有优缺点。CRP合成于肝脏,为正向蛋白,在炎症发生4~6 h后可升高,6~12 h后血液中可检捕,36~50 h达高峰,新生儿败血症时CRP达峰值时间较长[15-17]。本研究中足月儿早发败血症患儿不同乳酸水平分组、不同预后组间CRP差异无统计学意义,故无法对预后作出早期有效评估。PCT是甲状腺外器官产生的一种糖蛋白,当严重感染发生时PCT大量释放入血,3 h后即可检捕,6~12 h可达峰值,能作为早期评估指标[15, 18-19],但PCT基础分泌水平随日龄变化,提示败血症的PCT标准不一,有文献报道生后第1天PCT存在一个与感染无关的高峰[20]。本研究中PCT值在不同乳酸水平分组、不同预后组间差异均无统计学意义,故也较难作为早期预后评估的统一指标。
血乳酸是葡萄糖无氧代谢的终产物之一,作为全身灌注与氧代谢的重要指标,其水平升高反映了机体在低灌注情况下无氧代谢的增加。当组织灌注减少、组织缺氧时,糖酵解途径被激活,使丙酮酸通过无氧代谢形成乳酸,释放到血液中导致血乳酸水平升高[21]。预后差的败血症患儿多存在严重的循环障碍[22],而循环障碍导致低灌注和低氧,从而引起乳酸生成增多,同时肝脏灌注减低使乳酸的代谢减慢,使血乳酸水平进一步升高[23]。因此,本研究旨在探讨血乳酸作为反映微循环障碍的指标能否更好地评估患儿预后,以提供更加合理、科学的理论依据。
本研究显示,在足月儿中,乳酸重度升高组的病死率显著高于乳酸轻度升高组和乳酸正常组,与国外成人及儿童脓毒血症相关文献报道一致[24-25],提示入院乳酸水平与患儿预后相关。文献报道,入院时血乳酸水平、动态乳酸变化即乳酸清除率在评估成人及幼儿脓毒症预后中有重要价值[26-27]。有研究显示,在成年人及儿童脓毒症中早期乳酸水平明显升高、早期乳酸清除率 < 10%者,其病死率显著升高[26]。本研究显示,在足月儿中,预后不良组较预后良好组入院时血乳酸水平显著升高,与国内外报道相符[21, 24, 26-28]。而本研究中预后不良组和预后良好组组间乳酸清除率比较差异无统计学意义,考虑与本研究为回顾性研究,进行二次乳酸水平检测的病例数较少有关。
本研究ROC曲线分析显示,入院乳酸为6.15 mmol/L是判断败血症新生儿预后是否良好的最佳临界值,对判断新生儿败血症预后具有较高的特异性,但其敏感性较低。其敏感性较低的原因,第一,可能与本研究样本量较小有关;其次,本研究中不良结局包含脑积水、支气管肺发育不良、视网膜病变等远期后遗症,他们均是缓慢进展而来,而入院乳酸水平仅仅反映了急性期的代谢变化,不能反映长期损害的过程,因此上述不良结局对应的早期乳酸水平可能较低,从而导致敏感性不高。当入院血乳酸水平联合微循环障碍这一临床表现时,其敏感性和特异性均有所增加,因此结合两项指标对判断新生儿不良预后更有价值。
综上所述,本研究显示,入院时血乳酸水平可作为判断新生儿败血症预后的指标,特异性高,但敏感性较低。血乳酸水平联合微循环障碍这一临床表现有助于提高新生儿败血症预后判断的敏感性和特异性。根据血乳酸代谢水平及时纠正组织低灌注、缺氧状态,有利于阻止病情进展,改善患儿预后。血乳酸测定及时、经济、创伤小,其临床意义显著,值得临床推广应用。
| [1] |
Nolt B, Tu F, Wang X, et al. Lactate and immunosuppression in sepsis[J]. Shock, 2018, 49(2): 120-125. DOI:10.1097/SHK.0000000000000958 (  0) 0) |
| [2] |
王政力, 余加林. 新生儿败血症诊断新进展[J]. 中国当代儿科杂志, 2013, 15(3): 236-241. (  0) 0) |
| [3] |
Shane AL, Sánchez PJ, Stoll BJ. Neonatal sepsis[J]. Lancet, 2017, 390(10104): 1770-1780. DOI:10.1016/S0140-6736(17)31002-4 (  0) 0) |
| [4] |
Zea-Vera A, Ochoa TJ. Challenges in the diagnosis and management of neonatal sepsis[J]. J Trop Pediatr, 2015, 61(1): 1-13. (  0) 0) |
| [5] |
Ryoo SM, Lee J, Lee YS, et al. Lactate level versus lactate clearance for predicting mortality in patients with septic shock defined by sepsis-3[J]. Crit Care Med, 2018, 46(6): e489-e495. DOI:10.1097/CCM.0000000000003030 (  0) 0) |
| [6] |
Jia Y, Wang Y, Yu X. Relationship between blood lactic acid, blood procalcitonin, C-reactive protein and neonatal sepsis and corresponding prognostic significance in sick children[J]. Exp Ther Med, 2017, 14(3): 2189-2193. (  0) 0) |
| [7] |
中华医学会儿科学分会新生儿学组, 中华医学会中华儿科杂志编辑委员会. 新生儿败血症诊疗方案[J]. 中华儿科杂志, 2003, 41(12): 897-899. DOI:10.3760/j.issn:0578-1310.2003.12.005 (  0) 0) |
| [8] |
Mohammed I, Nonas SA. Mechanisms, detection, and potential management of microcirculatory disturbances in sepsis[J]. Crit Care Clin, 2010, 26(2): 393-408. DOI:10.1016/j.ccc.2010.01.003 (  0) 0) |
| [9] |
Russell J, Lee T, Singer J, et al. The Septic Shock 3.0 definition and trials:a vasopressin and septic shock trial experience[J]. Crit Care Med, 2017, 45(6): 940-948. DOI:10.1097/CCM.0000000000002323 (  0) 0) |
| [10] |
Rojas-Marcial C, Pedraza-Zárate MÁ, Bautista-Barranco H, et al. Lactate levels with regards to the pulse pressure in patients with shock[J]. Rev Med Inst Mex Seguro Soc, 2016, 54(1): 16-19. (  0) 0) |
| [11] |
中华医学会儿科学分会新生儿学组, 中国医师协会新生儿科医师分会感染专业委员会. 新生儿败血症诊断及治疗专家共识(2019年版)[J]. 中华儿科杂志, 2019, 57(4): 252-257. (  0) 0) |
| [12] |
Cantey JB, Baird SD. Ending the culture of culture-negative sepsis in the neonatal ICU[J]. Pediatrics, 2017, 140(4): pii:e20170044. DOI:10.1542/peds.2017-0044 (  0) 0) |
| [13] |
Schuetz P, Birkhahn R, Sherwin R, et al. Serial procalcitonin predicts mortality in severe sepsis patients:results from the multicenter procalcitonin monitoring sepsis (MOSES) study[J]. Crit Care Med, 2017, 45(5): 781-789. DOI:10.1097/CCM.0000000000002321 (  0) 0) |
| [14] |
冯亚群, 胡祥华, 梁亚勇. 联合检测降钙素原和超敏C反应蛋白对新生儿败血症早期诊断的临床价值[J]. 实用医学杂志, 2010, 26(9): 1582-1584. DOI:10.3969/j.issn.1006-5725.2010.09.041 (  0) 0) |
| [15] |
Yang A, Liu J, Yue L, et al. Neutrophil CD64 combined with PCT, CRP and WBC improves the sensitivity for the early diagnosis of neonatal sepsis[J]. Clin Chem Lab Med, 2016, 54(2): 345-351. (  0) 0) |
| [16] |
Perrone S, Lotti F, Longini M, et al. C reactive protein in healthy term newborns during the first 48 hours of life[J]. Arch Dis Child Fetal Neonatal Ed, 2018, 103(2): F163-F166. DOI:10.1136/archdischild-2016-312506 (  0) 0) |
| [17] |
龚红蕾, 徐美玉, 施晓民, 等. 血清PA、ALB和CRP在小儿脓毒症急性期和恢复期的水平变化[J]. 江苏医药, 2014, 40(19): 2284-2285. (  0) 0) |
| [18] |
Arora S, Singh P, Singh PM, et al. Procalcitonin levels in survivors and nonsurvivors of sepsis:systematic review and meta-analysis[J]. Shock, 2015, 43(3): 212-221. DOI:10.1097/SHK.0000000000000305 (  0) 0) |
| [19] |
Meisner M. Pathobiochemistry and clinical use of procalcitonin[J]. Clin Chim Acta, 2002, 323(1-2): 17-29. DOI:10.1016/S0009-8981(02)00101-8 (  0) 0) |
| [20] |
Fukuzumi N, Osawa K, Sato I, et al. Age-specific percentile-based reference curve of serum procalcitonin concentrations in Japanese preterm infants[J]. Sci Rep, 2016, 6: 23871. DOI:10.1038/srep23871 (  0) 0) |
| [21] |
安莹波. 早期动脉血乳酸水平和乳酸清除率对评估严重脓毒症患者预后的临床价值[J]. 微循环学杂志, 2013, 23(3): 50-51. (  0) 0) |
| [22] |
陈爱斌, 茅双根. 新生儿感染性休克的诊断及治疗[J]. 中华全科医学, 2018, 16(7): 1049-1050. (  0) 0) |
| [23] |
Ha T, Shin T, Jo IJ, et al. Lactate clearance and mortality in septic patients with hepatic dysfunction[J]. Am J Emerg Med, 2016, 34(6): 1011-1015. DOI:10.1016/j.ajem.2016.02.053 (  0) 0) |
| [24] |
Casserly B, Phillips G, Schorr C, et al. Lactate measurements in sepsis-induced tissue hypoperfusion:results from the Surviving Sepsis Campaign database[J]. Crit Care Med, 2015, 43(3): 567-573. DOI:10.1097/CCM.0000000000000742 (  0) 0) |
| [25] |
颜海鹏, 卢秀兰, 仇君, 等. 血乳酸在脓毒症患儿病情及预后评价中的意义[J]. 中国当代儿科杂志, 2016, 18(6): 506-510. (  0) 0) |
| [26] |
廖继旸, 袁金霞, 韩云, 等. 成人乳酸清除率指导脓毒症复苏治疗价值的Meta分析[J]. 解放军医学杂志, 2018, 43(9): 761-768. (  0) 0) |
| [27] |
Scott HF, Brou L, Deakyne SJ, et al. Lactate clearance and normalization and prolonged organ dysfunction in pediatric sepsis[J]. J Pediatr, 2016, 170: 149-155.e1-4. DOI:10.1016/j.jpeds.2015.11.071 (  0) 0) |
| [28] |
Arnold RC, Shapiro NI, Jones AE, et al. Multicenter study of early lactate clearance as a determinant of survival in patients with presumed sepsis[J]. Shock, 2009, 32(1): 35-39. (  0) 0) |
 2019, Vol. 21
2019, Vol. 21


