维生素D(vitamin D, VD)在免疫相关细胞中具有显著的抗炎、抗微生物及维持细胞膜稳定等重要作用[1]。有研究认为VD水平可影响儿童肺炎的严重程度[2];儿童肺炎的发病率与VD的缺乏呈正相关[3];有Meta分析显示,补充VD可预防呼吸道感染的发生,对降低儿童肺炎的风险具有一定意义[4]。因此,VD对儿童肺炎辅助治疗价值的研究值得期待。本研究采用Meta分析的方法,搜索随机对照试验的高质量文献,对有关VD辅助治疗儿童肺炎的临床研究进行系统分析,评价VD辅助治疗儿童肺炎的临床疗效,进一步明确其应用价值,为临床应用提供循证医学证据。
1 资料与方法 1.1 文献纳入和排除标准纳入关于VD辅助治疗儿童肺炎疗效的随机对照研究,且Jadad评分≥4分,即高质量文献。试验组为在常规治疗的基础上加用VD制剂辅助治疗,对照组为单纯常规治疗或常规治疗加用安慰剂治疗,两组间常规治疗方法具有同质性。
排除患儿合并其他疾病的文献或合用其他维生素治疗的文献。
1.2 结局指标结局指标包括疾病恢复时间、住院时间、相关临床症状体征消退时间、疾病复发率、不良反应率及病死率等。
1.3 文献检索策略检索以下中英文数据库(时间自建库至2019年8月):Cochrane Library、PubMed、EMbase、中国知网数据库、万方数据库以及维普数据库。同时手工检索期刊文献。
中文检索词为:肺炎、肺部感染、维生素D、维他命D、儿童、幼儿、小儿、婴儿。英文检索词为:pneumonia、pulmonary inflammat*、lung inflammat*、pulmonary infect*、vitamin D、cholecalciferol、ergocalciferol、child、kid、infant、young people、pediatric、preschool。
1.4 文献筛选及数据提取2名研究人员独立地进行文献检索及资料提取。首先阅读题目和摘要初步筛选文献,然后阅读全文后进行确认,并对结果进行交叉核对,如遇分歧通过讨论或咨询第三方解决。提取的资料内容包括:第一作者、发表时间、研究对象的基本特征(样本量、年龄)、干预措施及结局指标等。
1.5 文献质量评价采用修改后的Jadad评分标准[5]对纳入的文献进行质量评价,1~3分视为低质量,4~6分视为高质量。采用Cochrane协作网偏倚风险评价工具对文献进行质量评价。2名研究者独立对纳入的文献进行质量评价,意见不一致时,通过第三方裁定。
1.6 统计学分析使用Cochrane协作网提供的Review Manager 5.3(RevMan 5.3)统计软件对提取的数据进行数据处理及分析。P < 0.05示有统计学意义。不能进行Meta分析的数据则进行描述性分析。
采用卡方检验进行异质性评价,用I2统计测量异质性的程度。当P > 0.05且I2 < 50%时,表明没有显著的异质性,采用固定效应模型;当P < 0.05或I2 > 50%时,表明异质性显著,则进一步分析异质性来源,在排除明显的临床异质性后,采用随机效应模型进行Meta分析。
2 结果 2.1 文献检索结果及特征经初步检索,共检索到文献312篇,通过阅读文题及摘要后筛选出19篇,后逐一阅读全文,12篇文献Jadad评分 < 4分被排除,最终纳入文献7篇,包括1 527例患儿,其中VD辅助治疗组762例,对照组765例。纳入研究的基本特征见表 1。
| 表 1 纳入文献的基本特征 |
|
|
纳入研究的Jadad评分结果见表 2。2篇文献评分为满分7分,4篇文献为6分,1篇文献为4分。
| 表 2 纳入文献的Jadad评分 |
|
|
Cochrane协作网偏倚风险工具对文献的偏倚风险评价结果见图 1。本Meta分析所纳入的研究均进行了适当的随机分配方法,分配方案隐藏、结果测量者盲法、结果数据的完整性、选择性报告及其他偏倚风险大部分均较低或不清,其中2篇文献[11-12]的研究对象及方案实施者未实施盲法。
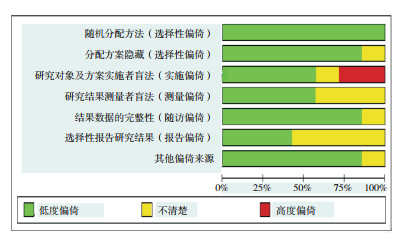
|
图 1 纳入文献偏倚风险评价结果 |
3篇文献[6-8]报道了VD辅助治疗组与对照组的疾病恢复时间,各研究间异质性低(I2=12%,P=0.32),故采用固定效应模型进行Meta分析,结果显示两组疾病恢复时间的比较差异无统计学意义(MD=-1.02,95%CI:-5.74~3.70,P=0.67),见图 2。
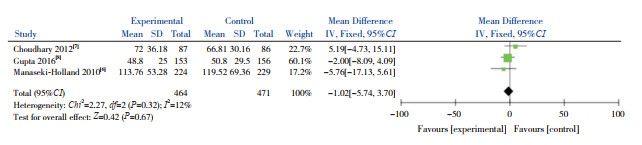
|
图 2 两组疾病恢复时间比较的Meta分析森林图 |
4篇文献[7-8, 11-12]报道了VD辅助治疗组与对照组的住院时间,各研究间异质性低(I2=44%,P=0.15),故采用固定效应模型进行Meta分析,结果显示两组住院时间的比较差异无统计学意义(MD=1.06,95%CI:-4.90~7.02,P=0.73)。根据对照组是否加用安慰剂进行亚组分析,结果显示VD辅助治疗组与对照组住院时间的比较差异仍无统计学意义(有安慰剂组:P=0.56;无安慰剂组:P=0.64)。见图 3。
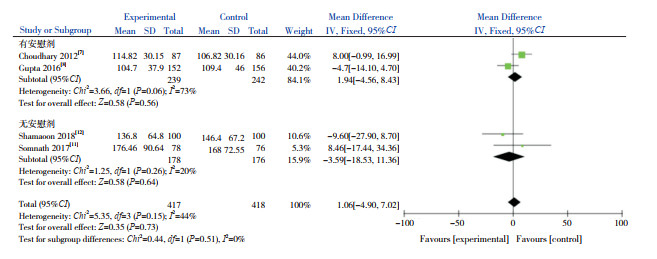
|
图 3 两组住院时间比较的Meta分析森林图 |
4篇文献[7-9, 11]报道了VD辅助治疗组与对照组的退烧时间,各研究间异质性低(I2=0%,P=0.48),故采用固定效应模型进行Meta分析,结果显示两组退烧时间比较差异无统计学意义(MD=1.66,95%CI:-2.44~5.76,P=0.43)。根据对照组是否加用安慰剂进行亚组分析,结果显示VD辅助治疗组与对照组退烧时间的比较差异仍无统计学意义(有安慰剂组:P=0.21;无安慰剂组:P=0.35)。见图 4。
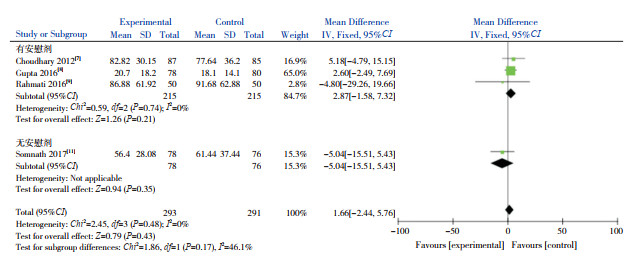
|
图 4 两组退烧时间比较的Meta分析森林图 |
4篇文献[6, 8, 11-12]报道了VD辅助治疗组与对照组的疾病复发率,各研究间异质性显著(I2=70%,P=0.02),故采用随机效应模型进行Meta分析,结果显示两组疾病复发率比较差异无统计学意义(RR=0.72,95%CI:0.46~1.12,P=0.14)。根据对照组是否加用安慰剂进行亚组分析,亚组分析中各研究间异质性有所减小(有安慰剂组:I2=58%,P=0.12;无安慰剂组:I2=56%,P=0.13)。Meta分析结果显示VD辅助治疗组与对照组疾病复发率的比较差异仍无统计学意义(有安慰剂组:P=0.47;无安慰剂组:P=0.11)。见图 5。
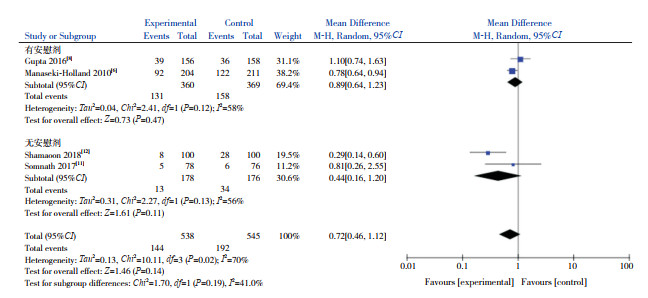
|
图 5 两组复发率比较的Meta分析森林图 |
4篇文献[6-8, 11]报道了VD辅助治疗组与对照组的不良反应率,各研究间异质性低(I2=0%,P=0.42),故采用固定效应模型进行Meta分析,结果显示两组不良反应率比较差异无统计学意义(RR=1.22,95%CI:0.90~1.66,P=0.20)。根据对照组是否加用安慰剂进行亚组分析,结果显示VD辅助治疗组与对照组不良反应率的比较差异仍无统计学意义(有安慰剂组:P=0.35;无安慰剂组:P=0.26)。见图 6。
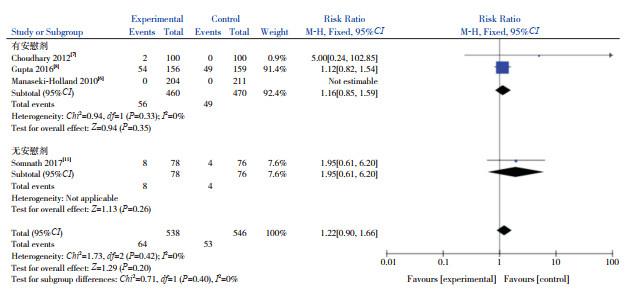
|
图 6 两组不良反应率比较的Meta分析森林图 |
4篇文献[6-8, 11]报道了VD辅助治疗组与对照组的病死率,各研究间异质性低(I2=0%,P=0.67),故采用固定效应模型进行Meta分析,结果显示两组病死率的比较差异无统计学意义(RR=1.02,95%CI:0.23~4.45,P=0.98)。根据对照组是否加用安慰剂进行亚组分析,结果显示VD辅助治疗组与对照组病死率的比较差异仍无统计学意义(有安慰剂组:P=0.98)。见图 7。
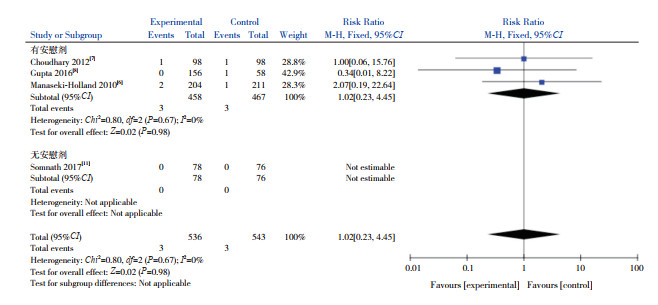
|
图 7 两组病死率比较的Meta分析森林图 |
各个结局指标中,只有疾病复发率异质性显著(I2=70%,P=0.02)。为进一步分析异质性来源,对此结局指标采用逐一剔除文献法进行敏感性分析,发现剔除Shamaoon等[12]的研究后各研究间异质性较低(I2=17%,P=0.30)。分析此文献,其Jadad评分最低,仅为4分,其余文献的Jadad评分均为6分或7分。剔除Shamaoon等[12]的文献后,采用固定效应模型进行Meta分析,结果显示两组疾病复发率的比较差异仍无统计学意义(RR=0.85,95%CI:0.72~1.01,P=0.07),见图 8。
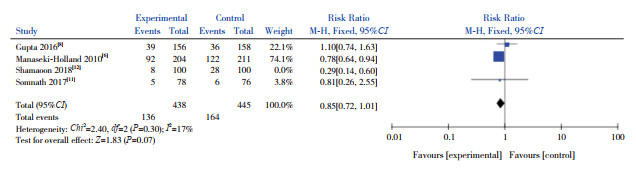
|
图 8 两组复发率敏感性分析森林图 |
本研究在回顾既往研究结果的基础上,运用循证医学方法对VD辅助治疗儿童肺炎的疗效进行了客观评价,纳入的文献均为Jadad评分≥4分的高质量文献。本研究共纳入7项研究,Meta分析结果显示两组患儿疾病恢复时间、住院时间及退烧时间的比较差异均无统计学意义,两组肺炎的复发率、不良反应率及病死率的比较差异也无统计学意义,这与Das等[13]的系统评价分析结果一致。因此,本Meta分析认为VD辅助治疗对儿童肺炎的疗效没有明显作用。
本Meta分析纳入的文献中,有1篇文献[10]的结局数据无法行Meta分析,故仅在此进行描述性分析。这篇文献指出,短期补充VD对儿童肺炎的缓解时间无明显作用。Rahmati等[9]的研究报道,VD辅助治疗儿童肺炎可减少抗生素的使用时间,但此结局指标在本Meta分析所纳入的文献中仅这一篇予以报道,因此未对此指标进行Meta分析。
关于结局指标的异质性,本研究所观察指标中只有疾病复发率的异质性是显著的。对于该指标,根据对照组是否应用安慰剂进行了亚组分析。亚组分析中各研究间异质性有所减小,Meta分析结果显示VD辅助治疗组与对照组的疾病复发率差异仍无统计学意义。进一步的敏感性分析显示,剔除文献质量相对较低的文献[12]后,异质性显著降低,但Meta分析仍显示两组疾病复发率的比较差异无统计学意义。
本Meta分析的局限性:本研究所收集的数据来自不同的国家或地区,具有不同的研究背景和干预条件,此外,各研究中研究对象肺炎的严重程度、VD补充用量和时间及治疗前VD水平等也可能对结局指标产生影响,但由于纳入文献较少,未进一步进行亚组分析。
综上所述,本Meta分析研究显示,VD辅助治疗不会影响儿童肺炎的疾病恢复时间、住院时间及退烧时间,也不会减少儿童肺炎的复发率、不良反应率及病死率。由于纳入的研究数量有限,仍有待进一步开展大样本、高质量的临床随机对照研究,并进行亚组分析,以更全面了解VD辅助治疗儿童肺炎的临床应用价值。
| [1] |
Rolf L, Muris AH, Hupperts R, et al. Vitamin D effects on B cell function in autoimmunity[J]. Ann N Y Acad Sci, 2014, 1317: 84-91. DOI:10.1111/nyas.12440 (  0) 0) |
| [2] |
任静, 孙斌, 缪珀, 等. 血清维生素D水平与幼龄儿童社区获得性肺炎严重程度及危险因素的相关性研究[J]. 中国当代儿科杂志, 2013, 15(7): 519-521. (  0) 0) |
| [3] |
Holland SM, Qader G, Masher MI, et al. Effects of vitamin D supplementation to children diagnosed with neumonia in Kabul:a randomised controlled trial[J]. Trop Med Int Health, 2010, 15: 1148-1155. (  0) 0) |
| [4] |
Charan J, Goyal JP, Saxena D, et al. Vitamin D for prevention of respiratory tract infections:a systematic review and meta-analysis[J]. J Pharmacol Pharmacother, 2012, 3(4): 300-303. DOI:10.4103/0976-500X.103685 (  0) 0) |
| [5] |
Jadad AR, Moore RA, Carroll D, et al. Assessing the quality of reports of randomized clinical trials:is blinding necessary[J]. Control Clin Trials, 1996, 17(1): 1-12. DOI:10.1016/0197-2456(95)00134-4 (  0) 0) |
| [6] |
Manaseki-Holland S, Qader G, Isag Masher M, et al. Effects of vitamin D supplementation to children diagnosed with pneumonia in Kabul:a randomised controlled trial[J]. Trop Med Int Health, 2010, 15(10): 1148-1155. DOI:10.1111/j.1365-3156.2010.02578.x (  0) 0) |
| [7] |
Choudhary N, Gupta P. Vitamin D supplementation for severe pneumonia-a randomized controlled trial[J]. Indian Pediatr, 2012, 49(6): 449-454. DOI:10.1007/s13312-012-0073-x (  0) 0) |
| [8] |
Gupta P, Dewan P, Shah D, et al. Vitamin D supplementation for treatment and prevention of pneumonia in under-five children:a randomized double-blind placebo controlled trial[J]. Indian Pediatr, 2016, 53(11): 967-976. DOI:10.1007/s13312-016-0970-5 (  0) 0) |
| [9] |
Rahmati MB, Rezapour M, Shahvari SZ. The effects of vitamin D supplementation in respiratory index of severity in children (RISC)of hospitalized patients with community-acquired pneumonia:a double-blind randomized clinical trial[J]. Acta HealthMedica, 2016, 1(3): 60-64. DOI:10.19082/ah60 (  0) 0) |
| [10] |
Rajshekhar CS, Vanaki* R, Badakali AV, et al. Efficacy of vitamin D supplementation in the treatment of severe pneumonia in children aged less than five years[J]. Int J Contemp Pediatr, 2016, 3(1): 96-99. (  0) 0) |
| [11] |
Somnath SH, Biswal N, Chandrasekaran V, et al. Therapeutic effect of vitamin D in acute lower respiratory infection:a randomized controlled trial[J]. Clin Nutr ESPEN, 2017, 20: 24-28. DOI:10.1016/j.clnesp.2017.02.003 (  0) 0) |
| [12] |
Shamaoon M, Maryam, Ahsan M, et al. Vitamin D and pneumonia; Role of vitamin D supplementation in children with pneumonia, a randomised control trial[J]. Professional Med J, 2018, 25(4): 532-537. DOI:10.29309/TPMJ/18.4508 (  0) 0) |
| [13] |
Das RR, Singh M, Panigrahi I, et al. Vitamin D supplementation for the treatment of acute childhood pneumonia:a systematic review[J]. ISRN Pediatr, 2013, 2013: 459160. (  0) 0) |
 2020, Vol. 22
2020, Vol. 22


