2. 重庆医科大学附属儿童医院 新生儿科, 重庆 400014;
3. 儿童发育疾病研究教育部重点实验室, 重庆 400014;
4. 国家儿童健康与疾病临床医学研究中心, 重庆 400014;
5. 儿童发育重大疾病国家国际科技合作基地, 重庆 400014;
6. 儿科学重庆市重点实验室, 重庆 400014
侵袭性真菌感染(invasive fungal infection, IFI)是指真菌侵入人体,累及组织和器官,甚至引起播散性感染,导致炎症反应及组织损伤的疾病。近年来,随着新生儿重症监护病房(NICU)中高危患儿的增多、广谱抗生素的广泛使用、各种侵入性操作增加及高级生命支持系统的应用,IFI已成为NICU中早产儿晚发型感染的主要病因[1]。出生体重越轻,IFI发病率越高,病死率越高,在极低出生体重儿(very low birth weight infant, VLBWI)中,IFI发病率在1%~7.5%之间[2-4],病死率高达19.3%[5],合并真菌感染的新生儿病死率远高于其他新生儿。在存活患儿中,约60%的患儿遗留不同程度的神经系统后遗症[6-7]。
新生儿真菌感染临床表现缺乏特异性,早期诊断困难,病死率高。为改善预后,越来越多的研究致力于早期正确识别IFI。另一方面,预防真菌感染也被视为改善预后的非常重要的策略。近年来国内外陆续有学者开展了有关抗真菌药物预防IFI方面的系统评价[8-13],但这些系统评价大多纳入样本量较小,且涉及的抗真菌药物较多,结局指标较少,难以全面说明氟康唑预防IFI的效果和安全性。本文系统检索国内外对VLBWI预防性给予氟康唑的随机对照试验(RCT),评价其疗效与安全性。
1 资料与方法 1.1 文献纳入标准(1) 研究类型:国内外公开发表的RCT研究,限定语种为中文和英文;(2)研究对象:VLBWI(< 1 500 g),有发生真菌感染的高危因素但未被确诊为真菌感染;(3)干预措施:试验组进行口服/静脉给予氟康唑预防用药,对照组不使用氟
康唑。
1.2 文献排除标准(1) 非RCT研究、个案报道、综述、Meta分析;(2)试验组使用非氟康唑的其他抗真菌药物或其他药物的文献;(3)未报道本研究设定的结局指标的文献。
1.3 结局指标(1) 疗效指标:IFI发生率、真菌定植率、住院期间病死率、耐药情况。
(2) 安全性指标:①并发症,包括肝功能损害、脓毒症、新生儿坏死性小肠结肠炎(necrotizing enterocolitis, NEC)、支气管肺发育不良(bronchopulmonary dysplasia, BPD)、动脉导管未闭(patent ductus arteriosus, PDA)、早产儿视网膜病(retinopathy of prematurity, ROP)、脑室内出血(intraventricular hemorrhage, IVH) > Ⅱ°;②远期神经系统发育。
1.4 检索策略计算机检索PubMed、Embase、Cochrane图书馆、万方数据库、中国科技期刊数据库(维普)和中国知网,检索时间为建库至2019年9月30日。对于综述和系统综述,追溯原始文献,以补充获取相关文献。英文检索词为“fluconazole”“antifungal agent”“prematurity”“premature infant”“very low birth weight”“invasive fungal infection”“fungal infection”“systemic mycosis”。中文检索词为“氟康唑”“抗真菌药物”“极低出生体重儿”“早产儿”“侵袭性真菌感染”“真菌感染”。
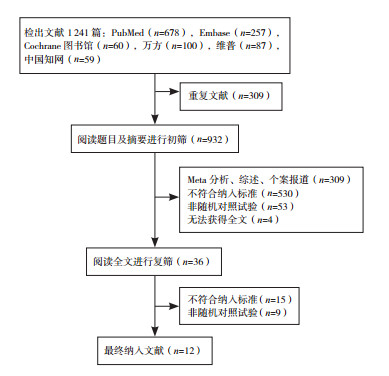
1.5 资料提取及文献质量评价由2名研究者独立进行文献筛选和资料提取并交叉核对,阅读文题和摘要排除明确不符合纳入标准的文献,进一步阅读全文进行排除,对于信息不全的文献,与作者联系后仍无法获得完整资料者,讨论后决定是否纳入。如意见不统一,则请第3名研究者加入讨论,最终达成共识。文献筛选流程及结果见图 1。
|
图 1 文献筛选流程图 |
采用Cochrane系统评价员手册5.1.0版(Review Manager 5.3软件中自带)提供的标准对随机对照研究从以下方面进行质量评价:随机方法、分配方案、盲法、对失访的报告、选择性偏倚及其他偏倚。若所有标准均为低风险,则为低偏倚风险研究(low risk of bias),其质量最高;一类或多类风险未知,则为未知偏倚风险研究(unclear risk of bias),质量为中等;一类或多类高风险,则为高偏倚风险研究(high risk of bias),其质量较低。同时对纳入文献采用Jadad评分法[14]进行文献质量评价。
1.6 统计学分析用Review Manager 5.3软件进行Meta分析,纳入研究结果间的异质性分析采用I2检验,当I2≤50%且P≥0.1时,表明各研究间无明显异质性,采用固定效应模型分析;当I2 > 50%且P < 0.1时,表明各研究间存在显著异质性,则进一步分析异质性来源,在排除明显临床异质性的影响后,采用随机效应模型进行分析。计数资料采用相对危险度(RR)为效应指标,计量资料采用标准化差值(SMD)为效应指标,P < 0.05为差异有统计学意义,各效应量均给出其点估计值和95%置信区间(CI)。采用Cochrane风险偏倚评估工具判断是否存在偏倚。利用Review Manager 5.3软件逐一排除文献进行敏感性分析。
2 结果 2.1 文献检索结果根据图 1所示的筛选流程,初步共检索到1 241篇文献,其中中文文献246篇,英文文献995篇,逐层筛选后最终获得12篇文献[15-26]纳入研究。共计纳入1 679例VLBWI,其中试验组944例,对照组735例。Jadad量表评分结果显示纳入的12项研究均为高质量研究(均≥3分)。纳入文献基本特征见表 1。
| 表 1 纳入文献基本特征 |
|
|
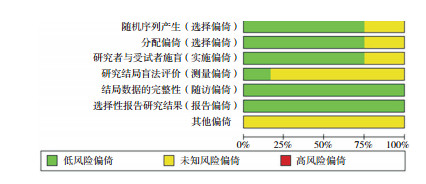
采用Cochrane协作网风险偏倚评估工具对所有文献进行评价。纳入的9篇文献[15-19, 21-23, 25]采用随机方法,报道了随机序列产生的方法,且实现了分配隐藏,故选择性偏倚较小;纳入的9篇文献[15-19, 22-25]对研究者和受试者实施盲法,故实施偏倚较小;仅有2篇文献[22-23]实现了研究结局盲法评价,故测量偏倚较大;12篇文献结局数据完整且不存在选择性报告研究结果,故随访及发表性偏倚均较小;没有文献报道了其他偏倚情况。见图 2。
|
图 2 偏倚风险图 |
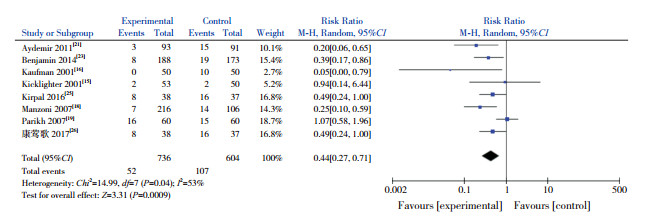
共8篇文献[15-16, 18-19, 21, 23, 25-26]观察研究了预防性使用氟康唑对IFI发生率的影响,试验组和对照组IFI发生率分别为7.1%(52/736)和17.7%(107/604),异质性检验I2=53%、P=0.04,结果存在中度异质性,进一步进行敏感性分析发现,去除Parikh等[19]的研究后异质性明显下降(I2=5%、P=0.39),但经详细评估该RCT质量较高,故继续纳入,采用随机效应模型进行统计学分析,试验组患儿的IFI发生率显著低于对照组(RR=0.44;95%CI:0.27~0.71,P=0.0009)。见图 3。
|
图 3 IFI发生率 |
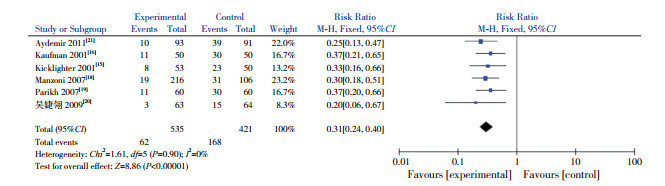
共6篇文献[15-16, 18-21]观察了预防性使用氟康唑对真菌定植率的影响,包括了消化道、气管导管或鼻咽部、皮肤定植。试验组和安慰剂对照组真菌定植率分别为11.6%(62/535)和39.9%(168/421),异质性检验I2=0%、P=0.90,各研究间具有同质性,采用固定效应模型进行统计学分析,试验组患儿的真菌定植率显著低于对照组(RR=0.31;95%CI:0.24~0.40,P < 0.00001)。见图 4。
|
图 4 真菌定植率 |
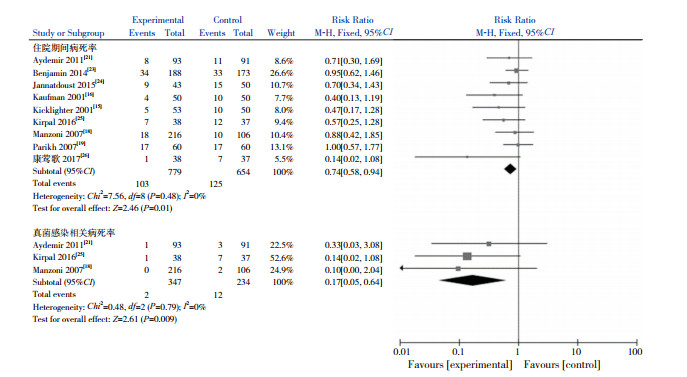
共9篇文献[15-16, 18-19, 21, 23-26]观察研究了住院患儿病死率的情况,试验组和安慰剂对照组住院期间病死率分别为13.2%(103/779)和19.1%(125/654),异质性检验I2=0%、P=0.48,各研究间具有同质性,采用固定效应模型进行统计学分析,试验组患儿住院期间病死率显著低于对照组(RR=0.74;95%CI:0.58~0.94,P=0.01)。见图 5。
|
图 5 住院期间病死率与真菌感染相关病死率 |
共3篇文献[18, 21, 25]研究了与真菌感染相关的病死率情况,试验组和安慰剂对照组真菌感染相关病死率分别为0.6%(2/347)和5.1%(12/234),异质性检验I2=0%、P=0.79,各研究间具有同质性,采用固定效应模型进行统计学分析,试验组患儿真菌感染相关病死率显著低于对照组(RR=0.17;95%CI:0.05~0.64,P=0.009),见图 5。
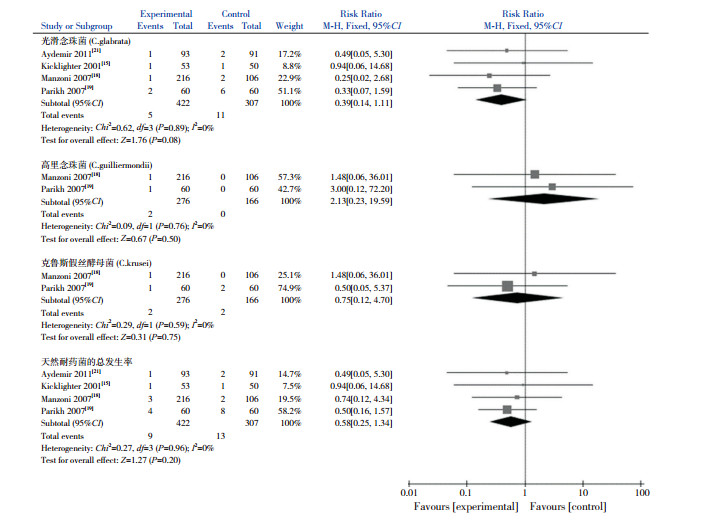
2.7 耐药情况共4篇文献[15, 18-19, 21]研究了预防性使用氟康唑后样本中分离出对氟康唑天然耐药菌的比例,各耐药菌发生率在对照组和试验组比较差异均无统计学意义(P > 0.05),总耐药菌的发生率在两组间比较差异也无统计学意义(RR=0.58;95%CI:0.25~1.34,P=0.20),见图 6。
|
图 6 对氟康唑天然耐药菌比例 |
试验组和对照组在肝功能异常、脓毒症、NEC、BPD、PDA、ROP及IVH > Ⅱ°等并发症的发生率方面进行比较差异均无统计学意义(P > 0.05)。需说明的是,在BPD的发生率上异质性较大(I2=55%、P=0.11),进一步分析异质性来源,去除Benjamin等[23]的研究后异质性明显下降(I2=0%、P=0.94),该研究对象为出生体重 < 750 g的超低出生体重儿,结合临床考虑,超低出生体重儿的BPD发生率与VLBWI的BPD发生率本就存在差异,但由于样本量较少,且漏斗图基本对称,故未行亚组分析。见表 2。
| 表 2 并发症情况 |
|
|
共有2篇文献[22-23]研究了预防性使用氟康唑后VLBWI远期神经系统发育情况,Kaufman等[22]通过采用VABS-Ⅱ评分及CHQ-FP28量表对新生儿期预防性使用氟康唑的VLBWI进行8~10年的随访,试验组和对照组儿童在沟通、生活技能、社交、大运动发育及生活质量的评价等各方面比较差异均无统计学意义(P > 0.05)。Benjamin等[23]从Bayley评分(认知、语言、运动能区发育情况)、视力障碍、听觉障碍及脑瘫情况4个方面评估神经系统发育,差异均无统计学意义(P > 0.05)。
2.10 不同氟康唑剂量对VLBWI结局指标的影响有2篇文献[17-18]研究了不同剂量氟康唑预防性使用的疗效及安全性,减少预防性使用氟康唑的剂量并未提高IFI发生率、真菌定植率、住院期间病死率及并发症的发生率(P > 0.05),见表 3。
| 表 3 不同氟康唑剂量对VLBWI结局指标的影响 |
|
|
近年来,随着新生儿重症监护水平的发展,危重新生儿救治率的升高,NICU中IFI的发生率也与日俱增,由于新生儿IFI临床表现不典型,诊断困难,发生真菌感染后易引起神经系统损害,即使即刻开始治疗也不能降低神经系统损害的发生率[6],故预防真菌感染才是关键。1998年Kicklighter等[15]第1次在VLBWI中预防性使用氟康唑并发现其可降低VLBWI中的真菌定植率,且无肝功能损害等不良反应发生。之后在全世界的NICU中陆续进行了许多RCT研究,但各研究间的结论不完全一致,其疗效与安全性尚无定论。Manzoni等[18]的一项多中心研究表明,在VLBWI中预防性使用氟康唑可有效降低IFI的发生率、真菌定植率,且不明显增加并发症的发生率。在我国,有少数RCT研究对于氟康唑预防VLBWI真菌感染进行了探索[20, 26],其结果均认同氟康唑预防VLBWI侵袭性真菌感染的有效性。
但目前预防性使用氟康唑的安全性尚存在争议。Brion等[27]在对有免疫抑制的成人中使用氟康唑预防真菌感染进行Meta分析发现已有耐药真菌的增加,Sarvikivi等[28]在自己所在的NICU预防性使用氟康唑10年后进行研究分析发现了对氟康唑不甚敏感的菌株,Yoder等[29]的动物实验表明,在预防性使用氟康唑约4年后,在实验动物中出现了真菌血症的暴发。本文纳入的文献中,对氟康唑天然耐药的光滑念珠菌、高里念珠菌、克鲁斯假丝酵母菌的检出比例并无明显升高。但涉及的研究中心较少,容易受到各中心常见感染菌株比例的影响,因此想得到更客观、明确的结论,需扩大样本量,并结合自身NICU中心实际情况分析。
本研究显示,预防性使用氟康唑可有效降低IFI的发生率、真菌定植率,这与张金萍等[9]及Cleminson等[8]的研究结果相符。本文结果显示预防性使用氟康唑可降低患儿住院期间病死率及真菌感染相关病死率,这与Cleminson等[8]的研究结果不同,相比较之下本文纳入文献更多,涉及研究中心及地区更多,各单中心研究发现总体病死率差异并无统计学意义,但总体数据差异有统计学意义,漏斗图检验无明显发表偏倚,统计结论可信。安全性指标显示预防性使用氟康唑不增加肝功能异常的发生率,以及NEC、PDA、ROP等并发症的发生率,说明预防性使用氟康唑相对安全且有效。
预防性用药目的在于以最小剂量的药物,在发生最小的毒副作用的情况下,取得最优的预防效果。Leonart等[10]研究发现3 mg/kg、4 mg/kg与6 mg/kg在预防IFI的效果上无明显区别,剂量越大,药物相关不良反应、耐药性可能越大,这与Manzoni等[18]研究的结果相同。此外,Kaufman等[17]研究发现延长给药间隔与连续给药预防效果无明显区别,故可尽量采取小剂量、间断给药方式进行预防。
本文的局限性:(1)纳入对象来自多个研究中心,各中心真菌感染率及用药方式不同,可能对结果产生影响;(2)纳入4篇文献研究对象为超低出生体重儿[16-17, 22-23],占纳入研究对象总数的34%,这可能对并发症的发生及耐药性的研究产生影响。由于现有研究数目有限,无法对上述因素进行更细化的分组评估。
综上所述,氟康唑预防VLBWI侵袭性真菌感染有效且相对安全,小剂量、间断给药可能取得类似预防效果,有可能降低耐药性的发生。临床上有待进行多中心大样本的随机对照研究进一步探索。
| [1] |
Kaufman DA. Challenging issues in neonatal candidiasis[J]. Curr Med Res Opin, 2010, 26(7): 1769-1778. DOI:10.1185/03007995.2010.487799 (  0) 0) |
| [2] |
Clerihew L, Lamagni TL, Brocklehurst P, et al. Invasive fungal infection in very low birthweight infants:national prospective surveillance study[J]. Arch Dis Child Fetal Neonatal Ed, 2006, 91(3): F188-F192. (  0) 0) |
| [3] |
Boghossian NS, Page GP, Bell EF, et al. Late-onset sepsis in very low birth weight infants from singleton and multiple-gestation births[J]. J Pediatr, 2013, 162(6): 1120-1124. DOI:10.1016/j.jpeds.2012.11.089 (  0) 0) |
| [4] |
Feja KN, Wu F, Roberts K, et al. Risk factors for candidemia in critically ill infants:a matched case-control study[J]. J Pediatr, 2005, 147(2): 156-161. DOI:10.1016/j.jpeds.2005.02.021 (  0) 0) |
| [5] |
Xia H, Wu H, Xia S, et al. Invasive Candidiasis in preterm neonates in China:a retrospective study from 11 NICUS during 2009-2011[J]. Pediatr Infect Dis J, 2014, 33(1): 106-109. DOI:10.1097/INF.0000000000000009 (  0) 0) |
| [6] |
Benjamin DK Jr, Stoll BJ, Fanaroff AA, et al. Neonatal candidiasis among extremely low birth weight infants:risk factors, mortality rates, and neurodevelopmental outcomes at 18 to 22 months[J]. Pediatrics, 2006, 117(1): 84-92. DOI:10.1542/peds.2004-2292 (  0) 0) |
| [7] |
Stoll BJ, Hansen NI, Adams-Chapman I, et al. Neuro-developmental and growth impairment among extremely low-birth-weight infants with neonatal infection[J]. JAMA, 2004, 292(19): 2357-2365. DOI:10.1001/jama.292.19.2357 (  0) 0) |
| [8] |
Cleminson J, Austin N, McGuire W. Prophylactic systemic antifungal agents to prevent mortality and morbidity in very low birth weight infants[J]. Cochrane Database Syst Rev, 2015(10): CD003850. (  0) 0) |
| [9] |
张金萍, 陈超. 氟康唑预防极低出生体重儿真菌感染有效性和安全性的Meta分析[J]. 中华儿科杂志, 2009, 47(12): 891-897. DOI:10.3760/cma.j.issn.0578-1310.2009.12.004 (  0) 0) |
| [10] |
Leonart LP, Tonin FS, Ferreira VL, et al. Fluconazole doses used for prophylaxis of invasive fungal infection in neonatal intensive care units:a network Meta-analysis[J]. J Pediatr, 2017, 185: 129-135. DOI:10.1016/j.jpeds.2017.02.039 (  0) 0) |
| [11] |
Ericson JE, Kaufman D, Kicklighter SD, et al. Fluconazole prophylaxis for the prevention of candidiasis in premature infants:a Meta-analysis using patient-level data[J]. Clin Infect Dis, 2016, 63(5): 604-610. DOI:10.1093/cid/ciw363 (  0) 0) |
| [12] |
Rios JFDS, Camargos PAM, Corrêa LP, et al. Fluconazole prophylaxis in preterm infants:a systematic review[J]. Braz J Infect Dis, 2017, 21(3): 333-338. (  0) 0) |
| [13] |
Blyth CC, Barzi F, Hale K, et al. Chemoprophylaxis of neonatal fungal infections in very low birthweight infants:efficacy and safety of fluconazole and nystatin[J]. J Paediatr Child Health, 2012, 48(9): 846-851. DOI:10.1111/j.1440-1754.2012.02543.x (  0) 0) |
| [14] |
Jadad AR, Moore RA, Carroll D, et al. Assessing the quality of reports of randomized clinical trials:is blinding necessary?[J]. Control Clin Trials, 1996, 17(1): 1-12. (  0) 0) |
| [15] |
Kicklighter SD, Springer SC, Cox T, et al. Fluconazole for prophylaxis against candidal rectal colonization in the very low birth weight infant[J]. Pediatrics, 2001, 107(2): 293-298. DOI:10.1542/peds.107.2.293 (  0) 0) |
| [16] |
Kaufman D, Boyle R, Hazen KC, et al. Fluconazole prophylaxis against fungal colonization and infection in preterm infants[J]. N Engl J Med, 2001, 345(23): 1660-1666. DOI:10.1056/NEJMoa010494 (  0) 0) |
| [17] |
Kaufman D, Boyle R, Hazen KC, et al. Twice weekly fluconazole prophylaxis for prevention of invasive Candida infection in high-risk infants of < 1000 grams birth weight[J]. J Pediatr, 2005, 147(2): 172-179. DOI:10.1016/j.jpeds.2005.03.036 (  0) 0) |
| [18] |
Manzoni P, Stolfi I, Pugni L, et al. A multicenter, randomized trial of prophylactic fluconazole in preterm neonates[J]. N Engl J Med, 2007, 356(24): 2483-2495. DOI:10.1056/NEJMoa065733 (  0) 0) |
| [19] |
Parikh TB, Nanavati RN, Patankar CV, et al. Fluconazole prophylaxis against fungal colonization and invasive fungal infection in very low birth weight infants[J]. Indian Pediatr, 2007, 44(11): 830-837. (  0) 0) |
| [20] |
吴婕翎, 李文成, 杨杰. 氟康唑预防极低出生体重儿真菌感染[J]. 中国新生儿科杂志, 2009, 24(2): 82-84. DOI:10.3969/j.issn.1673-6710.2009.02.006 (  0) 0) |
| [21] |
Aydemir C, Oguz SS, Dizdar EA, et al. Randomised controlled trial of prophylactic fluconazole versus nystatin for the prevention of fungal colonisation and invasive fungal infection in very low birth weight infants[J]. Arch Dis Child Fetal Neonatal Ed, 2011, 96(3): F164-F168. DOI:10.1136/adc.2009.178996 (  0) 0) |
| [22] |
Kaufman DA, Cuff AL, Wamstad JB, et al. Fluconazole prophylaxis in extremely low birth weight infants and neurodevelopmental outcomes and quality of life at 8 to 10 years of age[J]. J Pediatr, 2011, 158(5): 759-765. DOI:10.1016/j.jpeds.2010.11.002 (  0) 0) |
| [23] |
Benjamin DK Jr, Hudak ML, Duara S, et al. Effect of fluconazole prophylaxis on candidiasis and mortality in premature infants:a randomized clinical trial[J]. JAMA, 2014, 311(17): 1742-1749. DOI:10.1001/jama.2014.2624 (  0) 0) |
| [24] |
Jannatdoust A, Imani V. The effect of prophylactic intravenous fluconazole on the clinical outcome of preterm infants during hospitalization[J]. Int J Women's Health Reprod Sci, 2015, 3(4): 212-216. DOI:10.15296/ijwhr.2015.44 (  0) 0) |
| [25] |
Kirpal H, Gathwala G, Chaudhary U, et al. Prophylactic fluconazole in very low birth weight infants admitted to neonatal intensive care unit:randomized controlled trial[J]. J Matern Fetal Neonatal Med, 2016, 29(4): 624-628. DOI:10.3109/14767058.2015.1013933 (  0) 0) |
| [26] |
康莺歌, 常晶, 姚爱梅. 氟康唑预防极低出生体重儿侵袭性真菌感染的临床观察[J]. 医药论坛杂志, 2017, 38(2): 31-33. (  0) 0) |
| [27] |
Brion LP, Uko SE, Goldman DL. Risk of resistance associated with fluconazole prophylaxis:systematic review[J]. J Infect, 2007, 54(6): 521-529. DOI:10.1016/j.jinf.2006.11.017 (  0) 0) |
| [28] |
Sarvikivi E, Lyytikäinen O, Soll DR, et al. Emergence of fluconazole resistance in a Candida parapsilosis strain that caused infections in a neonatal intensive care unit[J]. J Clin Microbiol, 2005, 43(6): 2729-2735. (  0) 0) |
| [29] |
Yoder BA, Sutton DA, Winter V, et al. Resistant Candida parapsilosis associated with long term fluconazole prophylaxis in an animal model[J]. Pediatr Infect Dis J, 2004, 23(7): 687-688. DOI:10.1097/01.inf.0000128777.22022.47 (  0) 0) |
 2020, Vol. 22
2020, Vol. 22


