2. 上海交通大学医学院附属瑞金医院儿内科, 上海 200025
蓝色橡皮疱痣综合征(blue rubber bleb nevus syndrome, BRBNS)是一种罕见疾病,以多处广泛分布的静脉畸形为特征,主要累及皮肤和胃肠道,其他脏器亦可受累[1]。皮肤病灶通常不引起症状,而消化道病变可导致反复的出血和贫血[2],也是导致患儿入院治疗的最重要因素。此外,其他异常还包括低纤维蛋白原血症、D二聚体增高等[3]。
关于BRBNS的治疗尚未达成共识,通常取决于消化道受累的程度和其他器官受累的程度。目前可用的治疗药物及方法包括皮质类固醇、干扰素-α、激光疗法、硬化剂注射和手术切除。既往研究表明磷酸肌醇3激酶(PI3K)/蛋白激酶B(AKT)/哺乳动物雷帕霉素靶蛋白(mTOR)信号通路可参与细胞异常的生长和增殖,认为该通路和肿瘤发生、血管生成密切相关[4]。而西罗莫司,又称雷帕霉素,是mTOR的特异性抑制剂,在儿童复杂血管畸形中已经显示出良好的治疗效果[5]。国外个案报道发现,经传统方法治疗失败的BRBNS患者,当给予口服西罗莫司治疗后能够明显控制病情[6]。目前国内尚无应用西罗莫司治疗BRBNS患儿消化道损伤的病例,故本文回顾性评估2例合并消化道出血的BRBNS患儿接受西罗莫司药物治疗后的结果,旨在为BRBNS的治疗提供临床支持。
1 资料与方法 1.1 病例分析分析及总结2例以频繁消化道出血为主诉入院的BRBNS患儿的主要临床特征和检查结果,以及给予西罗莫司治疗后的转归,并记录不良反应。
1.2 文献检索通过PubMed医学文献数据库检索国外文献,以“blue rubber bleb nevus syndrome” AND “sirolimus” OR“blue rubber bleb nevus syndrome”AND “rapamycin”为检索词,年龄设定为0~18岁患儿。通过万方、中国知网数据库检索国内文献,关键词为“蓝色橡皮疱痣综合征”与“西罗莫司”或“蓝色橡皮疱痣综合征”与“雷帕霉素”。总结文献中西罗莫司治疗BRBNS的相关情况。
2 结果 2.1 临床资料例1,女,2岁,因间断解黑便半年余入院。外院查血红蛋白波动在55~65 g/L,胃镜检查诊断为“消化道血管瘤”,多次补铁、输血对症治疗,未采取其他措施,故其黑便反复发作。入我院前两个月,患儿输血频率达每月2次。既往史:自出生时右侧面部腮腺区可见一肿物,逐渐增大,外院确诊为“血管瘤”,曾多次行甲氨蝶呤栓塞联合硬化剂和激素治疗,效果不佳,仍逐渐增大,曾行右侧颌面及颈部肿物探查术,以及介入硬化治疗。入院体检:神志清楚,贫血貌,右侧颌面及颈部可见一约6 cm×8 cm大小的肿物,质软,边界不清,无压痛,皮温不高,表面皮肤无异常。下颌处可见一长约8 cm手术疤痕,全身浅表淋巴结无肿大,心、肺、腹未见明显异常,双下肢无水肿。实验室检查提示存在贫血、低纤维蛋白原血症、D二聚体增高,其他指标基本正常,具体见表 1。入院后第3天行胃镜检查提示:全胃黏膜呈贫血性改变,胃体部及胃底部存在多发树莓样血管畸形改变,直径约0.8~1.5 cm(图 1A)。结合体格检查和内镜下表现,患儿确诊为BRBNS。予输血、补充纤维蛋白原、补充铁剂对症治疗。告知家属药物相关不良反应后,在签署知情同意书后家属同意超适应证使用西罗莫司。入院后第4天起开始口服西罗莫司(雷帕鸣,Pfizer Ireland Pharmaceuticals),初始剂量1 mg/d(每日0.066 mg/kg)。入院后第9天在全麻下行经胃镜硬化剂治疗,利用1%聚桂醇栓塞胃镜所见的静脉畸形。随访两年期间,根据体重调整西罗莫司剂量(每日0.05~0.15 mg/kg),使其血药浓度维持在6.5~11.7 ng/mL。用药期间患儿无反复感染,无消化道出血表现,面部肿物较前稍减小,患儿未再接受输血,且血红蛋白始终维持正常(131~138 g/L)。期间多次入院检测,随访血常规及肝、肾功能,以及出凝血指标、甲状腺功能、血脂指标等,除碱性磷酸酶、纤维蛋白降解产物-1、D二聚体一直高于正常,其余指标基本在正常范围以内(表 1)。持续用药1年8个月后,患儿家属自行停药。停药1个月后患儿因出现“黑便、面色苍白”,血红蛋白下降至70 g/L,再次收治我院,予血管瘤硬化剂治疗,并继续口服西罗莫司治疗至今。
| 表 1 患儿实验室检查数据 |
|
|
|
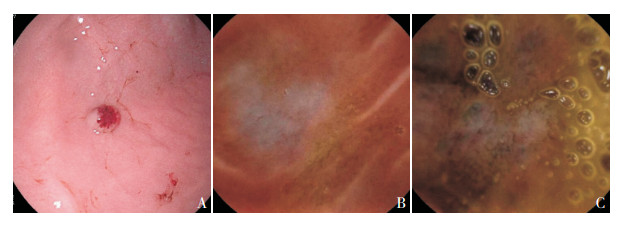
图 1 2例BRBNS患儿的消化内镜检查 A:例1,女,2岁,胃镜显示胃体部多发树莓样血管畸形;例2,男,7岁,胶囊内镜显示空肠(B)、回肠(C)黏膜下紫红色血管畸形。 |
例2,男,7岁,因黑便2月余入院。曾于外院就诊,血红蛋白波动在67~75 g/L。外院行胶囊内镜提示:十二指肠可见一大小1.0 cm×1.5 cm隆起性病变,表面黏膜充血糜烂,周围较长阶段肠黏膜下可见多发性蓝色曲张静脉团,可见红色征,未见活动性出血,回肠末端黏膜淋巴滤泡增生。外院经输血、止血等对症治疗,黑便仍反复发作,输血频率达每月1次。入院体检:神志清楚,精神可,面色苍白,全身浅表淋巴结无肿大,心、肺、腹未见明显异常,双下肢无水肿。实验室检查:提示贫血,其余指标基本正常(表 1)。影像学检查:腹部MR增强结果提示盆腔回肠及其系膜血管-淋巴管瘤;腹部CTA结果提示末端回肠肠壁多发迂曲血管影,考虑患者小肠多发性血管畸形。肠镜:结肠及直肠未见明显异常;胃镜:慢性浅表性胃炎;胶囊内镜:空回肠多发紫红色血管畸形(图 1B、1C)。经家属同意后,给予患儿口服西罗莫司治疗,初始剂量1 mg/d(每日0.034 mg/kg)。之后根据体重调整剂量,其血药浓度维持在2.6~10.3 ng/mL。随访1.5年期间,患儿无消化道出血表现,无反复呼吸道感染、乏力、精神异常等,患儿未再接受输血治疗,且血红蛋白始终维持在正常水平(128~139 g/L)。期间检测血常规、肝肾功能、血脂等未见明显异常,见表 1。
2.2 文献资料总结共检索到26篇关于使用西罗莫司治疗BRBNS的文献报道,其中只有13篇含0~18岁的病例,全部为英文报道[6-18],共26例患儿(表 2)。2例有家族史,其余均为散发。消化道出血为最常见表现,共25例;24例患者出现明显的皮肤静脉畸形;其他器官受累包括关节7例、肌肉3例、中枢神经系统3例、肝脏2例、眼睛2例、脊柱1例、胰腺1例、胸椎1例和肺部1例。内镜下消融、切除病变部位,口服心得安、皮质类固醇等均无法控制BRBNS患儿的反复消化道出血。26例患儿应用西罗莫司治疗后均获成功,消化道出血的频率明显减少,不再依赖输血。药物浓度控制上各研究不一,其中4例在西罗莫司血药浓度 < 5 ng/mL的情况下,病情依然控制较理想;1例因血药浓度过低(< 2.5 ng/mL)而复发。26例患儿使用西罗莫司过程中出现和药物相关的不良反应有:黏膜炎(7例)、粒细胞减少(2例)、口腔溃疡(2例)、轻度胆固醇升高(1例)、血小板减少(1例)、软组织感染(1例)。除软组织感染较严重需要停药以外,其余通过减少剂量、降低药物浓度,不良反应均好转。
| 表 2 文献复习资料 |
|
|
BRBNS是一种罕见的血管异常综合征,以多灶性静脉畸形为特征,常发生在皮肤、软组织及胃肠道中,也可在任何组织中发生。尽管该病被认为是良性血管畸形,但是大的静脉畸形会导致功能障碍或自发性溃疡,可能会引起反复消化道出血、低纤维蛋白原血症和D二聚体水平增高。其发病机制尚不清楚,可能与TEK体细胞嵌合突变有关[19]。TEK编码的蛋白是血管生成素-1的受体,属酪氨酸激酶TIE2家族成员。该受体与配体结合,通过PI3K/AKT/mTOR途径可介导血管的生成和成熟。另外血管内皮生长因子被认为是mTOR的上游刺激物和下游效应物,是血管生成中的关键调节剂。而西罗莫司作为mTOR的特异性抑制剂,可通过控制病灶中的血管生成和内皮细胞活性来治疗BRBNS[20]。
关于BRBNS治疗尚未达成统一,治疗方法的选择与个体症状和所累及的器官有关。BRBNS患者可在儿童时期出现危及生命的消化道大出血并伴有继发性缺铁性贫血。反复的消化道出血、住院输血危害患儿健康并严重影响生活质量。既往研究提示手术治疗[21]和内镜治疗[22]有相对较高的复发率,因此有必要对BRBNS使用抗血管生成的药物治疗。目前使用的药物包括糖皮质激素、普萘洛尔、沙利度胺和干扰素-α,然而尚无证据显示这些药物治疗对患儿的预后有积极影响[23]。另外有报道显示停止使用这些药物可导致复发[24]。
Yuksekkaya等[7]在表现为严重胃肠道出血的BRBNS患儿中首次使用西罗莫司,在随访的20个月中,患儿胃肠道出血停止、贫血改善,且无不良反应。此后陆续有25例BRBNS患儿成功接受了西罗莫司治疗。此次我们报道的2名患儿,均以明显的消化道出血及贫血为主要表现,在口服西罗莫司后有效控制胃肠道出血,通过输血和补充铁剂纠正贫血后,药物治疗期间无需继续输血治疗,且无血细胞减少、脂代谢异常、水肿和反复感染等不良反应。其中1名患儿,治疗前合并有凝血功能异常,即低纤维蛋白原和高D二聚体,经治疗后纤维蛋白原和D二聚体均恢复正常,降低了出血和血栓形成等并发症的风险。在已报道的病例中仅1名患者在使用西罗莫司2个月时因出现软组织感染而停止用药[8],其余患儿耐受良好,少数有轻度不良反应,在减少药物剂量后均恢复正常。基于此,我们认为西罗莫司治疗BRBNS是有效和安全的。
由于BRBNS罕见,很难进行大规模的随机对照临床研究,因此目前BRBNS的治疗尚未达成共识。西罗莫司既往已批准用于13岁以上肾移植儿童以预防器官排斥,BRBNS合并反复消化道出血对患儿的健康和生活质量影响很大,因此在这部分患儿中超适应证使用西罗莫司并通过定期监测血药浓度以调整剂量,可能受益超过其药物风险,但仍需对其长期应用的不良反应如肿瘤进行密切监测。由于目前病例较少,低年龄儿童使用安全性数据缺乏,因此只有在BRBNS严重影响孩子健康的情况下,待向家属充分说明使用药物利弊后,经伦理备案和签署知情同意后方可使用。
| [1] |
Jin XL, Wang ZH, Xiao XB, et al. Blue rubber bleb nevus syndrome:a case report and literature review[J]. World J Gastroenterol, 2014, 20(45): 17254-17259. DOI:10.3748/wjg.v20.i45.17254 (  0) 0) |
| [2] |
Goud A, Abdelqader A, Walters J, et al. Blue rubber bleb nevus syndrome:a rare presentation of late-onset anemia and lower gastrointestinal bleeding without cutaneous manifestations[J]. J Community Hosp Intern Med Perspect, 2016, 6(1): 29966. DOI:10.3402/jchimp.v6.29966 (  0) 0) |
| [3] |
Chen W, Chen H, Shan G, et al. Blue rubber bleb nevus syndrome:our experience and new endoscopic management[J]. Medicine (Baltimore), 2017, 96(33): e7792. DOI:10.1097/MD.0000000000007792 (  0) 0) |
| [4] |
Laplante M, Sabatini DM. mTOR signaling in growth control and disease[J]. Cell, 2012, 149(2): 274-293. DOI:10.1016/j.cell.2012.03.017 (  0) 0) |
| [5] |
Lackner H, Karastaneva A, Schwinger W, et al. Sirolimus for the treatment of children with various complicated vascular anomalies[J]. Eur J Pediatr, 2015, 174(12): 1579-1584. DOI:10.1007/s00431-015-2572-y (  0) 0) |
| [6] |
Salloum R, Fox CE, Alvarez-Allende CR, et al. Response of blue rubber bleb nevus syndrome to sirolimus treatment[J]. Pediatr Blood Cancer, 2016, 63(11): 1911-1914. DOI:10.1002/pbc.26049 (  0) 0) |
| [7] |
Yuksekkaya H, Ozbek O, Keser M, et al. Blue rubber bleb nevus syndrome:successful treatment with sirolimus[J]. Pediatrics, 2012, 129(4): e1080-e1084. DOI:10.1542/peds.2010-3611 (  0) 0) |
| [8] |
Zhang B, Li L, Zhang N, et al. Efficacy and safety of sirolimus in the treatment of blue rubber bleb naevus syndrome in paediatric patients[J]. Clin Exp Dermatol, 2020, 45(1): 79-85. DOI:10.1111/ced.14003 (  0) 0) |
| [9] |
Yokoyama M, Ozeki M, Nozawa A, et al. Low-dose sirolimus for a patient with blue rubber bleb nevus syndrome[J]. Pediatr Int, 2020, 62(1): 112-113. DOI:10.1111/ped.14059 (  0) 0) |
| [10] |
Isoldi S, Belsha D, Yeop I, et al. Diagnosis and management of children with blue rubber bleb nevus syndrome:a multi-center case series[J]. Dig Liver Dis, 2019, 51(11): 1537-1546. DOI:10.1016/j.dld.2019.04.020 (  0) 0) |
| [11] |
Ferrés-Ramis L, Knöpfel N, Salinas-Sanz JA, et al. Rapamycin in the treatment of blue rubber bleb nevus syndrome[J]. Actas Dermosifiliogr, 2015, 106(2): 137-138. DOI:10.1016/j.ad.2014.05.006 (  0) 0) |
| [12] |
Warner B, Butt A, Cairns S. Sirolimus is a successful treatment for recurrent iron deficiency anaemia in blue rubber bleb naevus syndrome[J]. J Pediatr Gastroenterol Nutr, 2015, 60(6): e49-e50. DOI:10.1097/MPG.0000000000000247 (  0) 0) |
| [13] |
Özgönenel B, Martin A. Low-dose sirolimus controls recurrent iron deficiency in a patient with blue rubber bleb nevus syndrome[J]. Pediatr Blood Cancer, 2015, 62(11): 2054-2055. DOI:10.1002/pbc.25590 (  0) 0) |
| [14] |
Gildener-Leapman JR, Rosenberg JB, Barmettler A. Proptosis reduction using sirolimus in a child with an orbital vascular malformation and blue rubber bleb nevus syndrome[J]. Ophthalmic Plast Reconstr Surg, 2017, 33(3S Suppl 1): S143-S146. DOI:10.1097/IOP.0000000000000692 (  0) 0) |
| [15] |
Ünlüsoy Aksu A, Sari S, Eğritaş Gürkan Ö, et al. Favorable response to sirolimus in a child with blue rubber bleb nevus syndrome in the gastrointestinal tract[J]. J Pediatr Hematol Oncol, 2017, 39(2): 147-149. DOI:10.1097/MPH.0000000000000681 (  0) 0) |
| [16] |
Akyuz C, Susam-Sen H, Aydin B. Blue rubber bleb nevus syndrome:promising response to sirolimus[J]. Indian Pediatr, 2017, 54(1): 53-54. DOI:10.1007/s13312-017-0998-1 (  0) 0) |
| [17] |
Kizilocak H, Dikme G, Celkan T. Sirolimus experience in blue rubber bleb nevus syndrome[J]. J PediatrHematol Oncol, 2018, 40(2): 168-169. (  0) 0) |
| [18] |
Wang KL, Ma SF, Pang LY, et al. Sirolimus alternative to blood transfusion as a life saver in blue rubber bleb nevus syndrome:a case report[J]. Medicine (Baltimore), 2018, 97(8): e9453. DOI:10.1097/MD.0000000000009453 (  0) 0) |
| [19] |
Soblet J, Kangas J, Nätynki M, et al. Blue rubber bleb nevus (BRBN) syndrome is caused by somatic TEK (TIE2) mutations[J]. J Invest Dermatol, 2017, 137(1): 207-216. DOI:10.1016/j.jid.2016.07.034 (  0) 0) |
| [20] |
Castillo SD, Vanhaesebroeck B, Sebire NJ. Phosphoinositide 3-kinase:a new kid on the block in vascular anomalies[J]. J Pathol, 2016, 240(4): 387-396. DOI:10.1002/path.4802 (  0) 0) |
| [21] |
Sandhu KS, Cohen H, Radin R, et al. Blue rubber bleb nevus syndrome presenting with recurrences[J]. Dig Dis Sci, 1987, 32(2): 214-219. DOI:10.1007/BF01297111 (  0) 0) |
| [22] |
Ning S, Zhang Y, Zu Z, et al. Enteroscopic sclerotherapy in blue rubber bleb nevus syndrome[J]. Pak J Med Sci, 2015, 31(1): 226-228. DOI:10.12669/pjms.311.5858 (  0) 0) |
| [23] |
Martinez CA, Rodrigues MR, Sato DT, et al. Blue rubber bleb nevus syndrome as a cause of lower digestive bleeding[J]. Case Rep Surg, 2014, 2014: 683684. DOI:10.1155/2014/683684 (  0) 0) |
| [24] |
Zahedi MJ, Darvish Moghadam S, Seyed Mirzaei SM, et al. Blue rubber bleb nevus syndrome as a rare cause of iron deficiency anemia:a case report and review of literature[J]. Middle East J Dig Dis, 2013, 5(4): 235-239. (  0) 0) |
 2020, Vol. 22
2020, Vol. 22


